【题目】(7分)下表为氯化钠、硝酸钾和氢氧化钙在不同温度下的溶解度。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度 / g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
Ca(OH)2 | 0.187 | 0.178 | 0.165 | 0.153 | 0.141 | 0.129 | 0.116 | |
(1)从上表数据能获得的一条信息是 。
(2)20℃时分别往盛有100g水的烧杯中加入上述三种物质各35g,充分溶解后如图所示,则乙烧杯中的溶质是 。要使丙烧杯中的固体完全溶解,可采取的一种措施是 。

(3)在60℃时将100g水配成KNO3的饱和溶液,再将其降温至20℃所得溶液的质量为 。
(4)我们常用熟石灰中和污水中含有的硫酸,现有100 t含硫酸0.49%的废水,该废水含有硫酸的质量
是 t,完全处理这些废水需要氢氧化钙的质量是 t。
参考答案:
【答案】(1)NaCl的溶解度随温度的升高变化不大 (2)NaCl 加水或升高温度
(3)131.6g (4)0.49 0.37
【解析】
试题分析:(1)从上表数据能获得的一条信息是:NaCl的溶解度随温度的升高变化不大或KNO3的溶解度随温度的升高变化较大或Ca(OH)2的溶解度随温度的升高而降低等
(2)根据20℃时三种物质的溶解度,NaCl >KNO3 >Ca(OH)2,所以可判断则乙烧杯中的溶质是NaCl,甲烧杯中的溶质是Ca(OH)2,丙烧杯中的溶质是KNO3,所以结合丙的溶解度随温度变化的趋势,要使丙烧杯中的固体完全溶解,可采取的一种措施是:加水或升高温度
(3)在60℃时将100g水配成KNO3的饱和溶液,再将其降温至20℃,所得溶液为20℃是的饱和溶液,而此时溶解度为31.6g,所以溶液的质量为100g+31.6g=131.6g
(4)根据溶质质量分数的表达式,可得溶质质量=100t×0.49%=0.49t,再根据化学方程式:Ca(OH)2+H2SO4==CaSO4+2H2O中Ca(OH)2与H2SO4的质量关系,不难求出需要氢氧化钙的质量是0.37t
-
科目: 来源: 题型:
查看答案和解析>>【题目】用36%的浓盐酸配制5%的稀盐酸,需要用到的仪器是 ( )
①量筒 ②天平 ③烧杯 ④胶头滴管 ⑤酒精灯 ⑥漏斗 ⑦玻璃棒
A.①③⑦ B.①③④⑦ C.②③⑤⑦ D.③④⑥
-
科目: 来源: 题型:
查看答案和解析>>【题目】小王同学需配制100g 12%的NaOH溶液来制作“叶脉书签”。在配制溶液过程中,下列做法正确的是( )
A.在托盘上垫上纸并称取12g NaOH固体
B.称量时发现指针向右偏转,应调节游码使天平平衡
C.用100mL量简量取88mL水
D.把称取的NaOH固体直接倒入装有88mL水的量筒中溶解
-
科目: 来源: 题型:
查看答案和解析>>【题目】控制变量法是实验探究的重要方法。下列四组对比实验获得的结论正确的是
选项
实验操作
结论
A

呼出的气体全部都是CO2
B
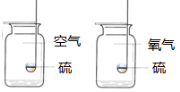
O2含量越高,反应越剧烈
C

铁生锈一定有O2参与
D
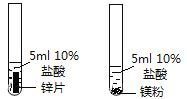
镁的活动性比锌强
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室用30%的双氧水溶液配制100g溶质质量分数为6%的双氧水溶液,需要加入水的质量为( )
A.20g B.80g C.100g D.200g
-
科目: 来源: 题型:
查看答案和解析>>【题目】(8分)下图是两套实验室制取气体的常用装置。
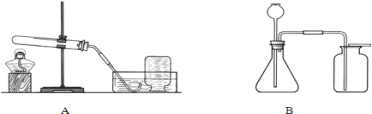
(1)制备CO2应选用的装置是 (填编号),生成CO2的化学方程式为 。
(2)B装置的气密性检查:先用止水夹夹住导管的橡皮管,然后向 中加入水至形成一段水柱,静置,若观察到 ,说明装置不漏气。
(3)集气瓶中气体的检验:往集气瓶里加入 ,振荡,
若 ,说明该气体是CO2。
(4)收集到一瓶二氧化碳后,按下图所示进行实验,观察到的现象是 。
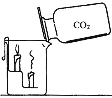
-
科目: 来源: 题型:
查看答案和解析>>【题目】(7分)从铜、氧化铜的混合粉末中回收铜的具体流程如下:
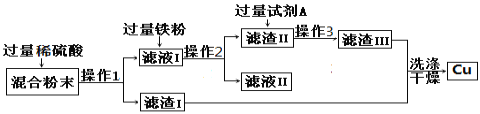
回答下列问题:
(1)操作1是 。
(2)滤液Ⅰ中加入过量铁粉所发生的反应的化学方程式是
。
(3)试剂A的作用是 。
(4)此实验过程中,下列哪些做法会导致回收到的Cu不纯
A.往混合粉末中加入的稀H2SO4不足
B.往滤液Ⅰ中加入铁粉不足
C.往滤渣Ⅱ中加入试剂A不足
(5)请写出铜的一种用途: 。
相关试题

