【题目】如图是某胃药标签的部分内容。小明同学测定该药品中NaHCO3含量的过程如下:取10粒该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7时(已知药品中的其他成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5克,称得反应后烧杯内物质的总质量为64.3克。

请计算:(1)反应完成后生成气体的质量为________ g。
(2)反应后烧杯中溶液的质量和胃药中NaHCO3的质量分数。
参考答案:
【答案】(1)2.2(2)反应后烧杯中溶液的质量为63.5g;胃药中NaHCO3的质量分数为84%
【解析】
(1)每粒0.5 g,10粒该药剂的质量为0.5 g×10=5g。
由质量守恒定律,生成二氧化碳气体的质量为5 g+50 g+11.5 g﹣64.3 g=2.2 g。
(2)设参加反应的碳酸氢钠的质量为x,
NaHCO3+HCl===NaCl+H2O+CO2↑
84 44
x 2.2 g
![]() x=4.2 g
x=4.2 g
反应后烧杯中溶液的质量为4.2 g+50 g+11.5 g-2.2 g=63.5 g。
胃药中NaHCO3的质量分数为![]() ×100%=84%。
×100%=84%。
答:(1)2.2g;(2)反应后烧杯中溶液的质量为63.5 g;胃药中NaHCO3的质量分数为84%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】水受热变成水蒸气的过程中,下列说法中错误的是
A.水分子运动加快 B.水分子之间的间隔变大
C.水分子数目增多了 D.水分子没有变成其它分子
-
科目: 来源: 题型:
查看答案和解析>>【题目】质检部门常采用“盖尔达法”鉴定奶粉的优劣。其原理是:把奶粉中的氮元素转化为NH3,再用一定量的稀硫酸来吸收[2NH3+H2SO4=== (NH4)2SO4],从而计算出奶粉中氮元素的质量分数,确定奶粉是否合格。(奶粉中氮元素的质量分数达到16%为合格)现取某奶粉样品20 g,将其中的氮元素转化为NH3,用100 g溶质质量分数为9.8%的稀硫酸恰好完全反应。
(1)计算产生NH3的质量。
(2)通过计算判断该奶粉是否合格。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为测定某氮肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氮肥样品于烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如下表:

反应前
反应后
烧杯和样品溶液总质量
氯化钡溶液质量
过滤后烧杯和溶液总质量(滤液的损失忽略不计)
45 g
55 g
76.7 g
[化学方程式为(NH4)2SO4+BaCl2===BaSO4↓+2NH4Cl,其他成分能溶于水但不参加反应]
(1)反应共生成BaSO4的质量为__ __g
(2)若所取氮肥样品的质量为15g,试通过计算确定氮肥中硫酸铵的纯度是否与标签相符。(请写出计算过程)
(3)反应前后,溶液中硫元素的质量__ __(填“不变”、“增大”或“减小”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】生铁和足量的稀盐酸充分反应后,总会有一些残渣剩余,残渣的主要成分是
A.铁 B.氯化铁 C.氯化亚铁 D.碳
-
科目: 来源: 题型:
查看答案和解析>>【题目】为测定某Cu﹣Zn合金中铜的质量分数,某同学将10g该合金放入到盛有40g足量稀硫酸的烧杯中,充分反应后,测得烧杯中剩余物的质量为49.9g.
(1)生成氢气的质量为 ;
(2)计算原合金中铜的质量分数.
-
科目: 来源: 题型:
查看答案和解析>>【题目】A、B、C三种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是
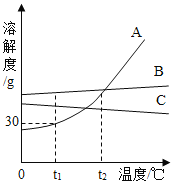
A.t 1 ℃时,A的饱和溶液65g中含有溶剂50g
B.要从B溶液中得到B,通常可采用蒸发溶剂使其结晶的方法
C.在t 2 ℃,A,B两种溶液中溶质的质量分数相同
D.将t 2 ℃A,B,C三种物质的饱和溶液降温至t 1 ℃时,C溶液中溶质的质量分数保持不变
相关试题

