【题目】(5分)某兴趣小组同学探究影响双氧水分解速度的某种因素和验证质量守恒定律实验时,数据记录如下:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9 mL |
Ⅱ | 50.0g | 2% | 0.1g | 16 mL |
Ⅲ | 50.0g | 4% | 0.1g | 31 mL |
(1)本实验中,测量O2体积的装置是 (填编号)。
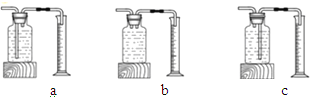
(2)实验结论:在相同条件下,双氧水的浓度越 (选填“大”或“小”),双氧水分解得越快。
(3)小王同学用下图装置进行实验,通过比较 也能达到实验目的。
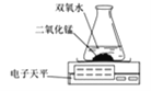
(4)小张同学看到电子天平数据比混合之前数据减小了,他认为该反应不遵守质量守恒定律。你认为他的看
法 (填正确或错误),原因是
参考答案:
【答案】(1)C;(2)大;(3)减少至相同质量时所需要的时间;(4)错误;产生氧气逸出;
【解析】
试题分析:(1)氧气不易溶于水且密度比水小,故应该选择装置C来测定氧气的体积,氧气从短管通入,将水从长管排入量筒中,根据量筒内水的体积得出生成的氧气的体积;
(2)根据表格数据可以得出双氧水的浓度越大,相同时间内产生的氧气体积越大;
(3)反应中生成氧气从溶液中逸出,根据减少至相同质量时所需要的时间也可以看出产生氧气速率的大小;
(4)电子天平数据比混合之前数据减小是因为反应时生成的氧气从溶液中逸出,而质量守恒定律指的是参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,故小张同学的看法是错误的;
-
科目: 来源: 题型:
查看答案和解析>>【题目】(8分)了解物质的组成和结构,有助于认识物质的性质。
(1)下图表示核电荷数为11-17的元素最高和最低化合价。
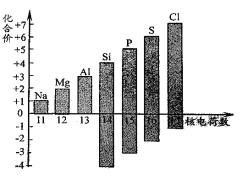
①从图中可以看出,氯元素的最高正价是 。
②若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为 。
③写出图中元素的化合价随着核电荷数递增的一条变化规律 。
(2)在3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O反应中:
①X的化学式为 ;
②HNO3中氮元素的质量分数为 (保留一位小数);
③Cu(NO3)2中铜元素、氧元素的质量比为 ;
④该反应涉及的物质中,直接由原子构成的是 ;水是由 构成。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(6分)小明在实验室里加热31.6g高锰酸钾制取氧气,完全反应后剩余固体质量为28.4g。将剩余固体溶解、过滤、烘干、称量,回收二氧化锰。请计算:
(1)生成氧气的质量为 g。
(2)回收过程中溶解和过滤均用到玻璃棒,它们的作用分别是 、 。
(3)回收得到二氧化锰的质量。(写出计算过程)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质属于纯净物的是
A.合金 B.大理石 C.甲烷 D.铁锈
-
科目: 来源: 题型:
查看答案和解析>>【题目】科学家成功地利用精密仪器从石墨中分离出单层的石墨片,这是目前世界上人工制得的最薄的材料,下列有关石墨片说法错误的是
A.石墨片是一种单质
B.石墨片与C60是同种物质,具有导电性
C.在一定条件下,石墨片可还原氧化铜
D.石墨片在氧气中完全燃烧的产物是CO2
-
科目: 来源: 题型:
查看答案和解析>>【题目】为探究空气的组成,小明用下图A所示装置进行实验。
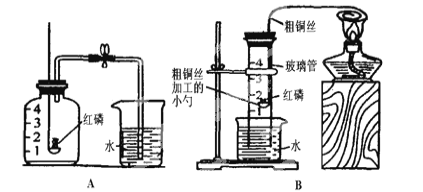
(1)实验时,取下橡胶塞,点燃红磷后迅速伸入集气瓶中并旋紧橡胶塞,这时看到的现象是:_______________,该反应的符号表达式为_____________。
(2)小明又设计了如上图B所示的改进装置,其优点是:___(只需写一点)。从理论上分析,玻璃管内液面最终将上升至__处(填“1”、“2”、“3”、“4”),但实测结果液面往往偏低,其原因可能是:_______(只需写一条)。
(3)从课本镁条燃烧实验小明得到启发,于是他用镁代替红磷做起了这个实验,实验完毕,冷却后进入集气瓶中水的体积远大于总容积的1/5,若装置气密性良好,则可能原因是: _ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列词语或俗语的有关化学原理解释中不合理的是
A.釜底抽薪——燃烧需要可燃物
B.钻木取火——使可燃物的着火点升高
C.真金不怕火烧——金的化学性质不活泼
D.没有金刚钻,不揽瓷器活——金刚石硬度大
相关试题

