【题目】下面是实验室常用的仪器
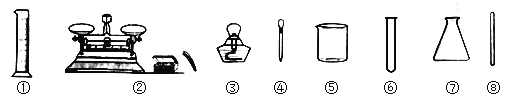
请回答下列的问题:
(1)可直接加热的有__________ (填序号)。
(2)滴加少量液体用__________ (填序号)。
(3)用仪器①能否量取8.68ml溶液__________ (填“能”或“否”)。
(4)过滤时玻璃仪器除了用到⑧外,还需用到漏斗及以上的__________ (填仪器名称)。
(5)活性炭的作用是____________。
(6)过滤操作中玻璃棒的作用是__________。
(7)小东到学校实验室用漏斗过滤后,滤液仍然浑浊,请你帮其分析原因。________________(写出一个原因)
参考答案:
【答案】 ⑥ ④ 否 烧杯 吸附 引流 滤纸破损或液面高于滤纸边缘等等
【解析】(1)可以直接加热的仪器是试管;
(2)用来吸取和滴加少量液体的仪器是胶头滴管;
(3)图中量筒的精确度到0.1mL,不能用来量取8.68mL溶液;
(4)过滤时玻璃仪器除了用到⑧外,还需用到漏斗和可作为滤液承接器的仪器是烧杯;
(5)活性炭疏松多孔,具有很强的吸附性;
(6)过滤操作中玻璃棒的作用是引流;
(7)过滤后,滤液仍然浑浊,原因可能是滤液面高于滤纸边沿、滤纸破损、承接滤液的烧杯不干净等。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学离不开实验,以下是实验室部分仪器或装置如图所示,请回答下列问题:

(1)B仪器的名称是_________________。
(2)若要组装一套二氧化碳的发生装置,可选择图中的_________________(填仪器下方的字母,下同),收集装置可选用图中的________________,写出实验室制取二氧化碳的化学方程式____________________,用该发生装置还可以制取的气体是__________(填一种)。
(3)若用氯酸钾制取氧气,发生装置除需A、C、E以外,还需要另外增加的仪器是_________。写出用氯酸钾制取氧气的化学方程式______________________________________,用图H
所示装置收集氧气,氧气应从________________(填“a”或“b”)端导入。
(4)CO2能与NaOH发生反应。
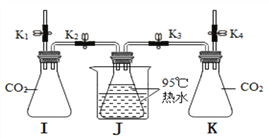
[实验过程]检查装置气密性,如图所示连接好装置,进行实验。
序号
操作步骤
实验现象
Ⅰ
打开弹簧夹K1,关闭弹簧夹K2、K3、K4。将20mL水注入锥形瓶I中,关闭弹簧夹K1,振荡瓶J,打开弹簧夹K2。
无明显现象
Ⅱ
关闭弹簧夹K2,打开弹簧夹K4,将20mL 稀NaOH溶液注入锥形瓶K中,关闭弹簧夹K4,振荡瓶J,打开弹簧夹K3。
锥形瓶J中的热水剧烈沸腾
[实验分析]锥形瓶J的热水剧烈沸腾的原因是____________________________________。
[实验反思]有观点认为只需要进行实验操作Ⅱ,即可说明CO2与NaOH发生反应.你对该观点的看法是_______(选填“赞同”或“不赞同”),理由是_____________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程见如图:
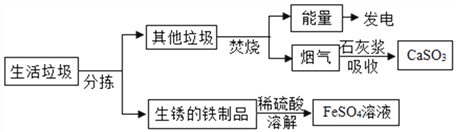
资料1:垃圾焚烧产生的烟气中含有SO2等有害气体。
资料2:FeSO4容易被空气中的O2氧化。
资料3:FeSO4的溶解度随温度的升高而升高。
资料4:氢氧化钙微溶于水。
回答下列问题:
(1)工业上用石灰浆除SO2而不是澄清石灰水的原因是___________________________。
(2)溶解步骤中同时发生的三个化学反应方程式为:Fe+Fe2(SO4)3=3FeSO4、Fe+H2SO4=FeSO4+H2↑、________________。
(3)将所得FeSO4溶液在氮气环境中蒸发浓缩、__________、过滤,得到FeSO4晶体,其中氮气的作用是________________。
(4)政府倡导垃圾分类,其好处是(写一点):_______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】探究燃烧条件的实验装置如下图所示。
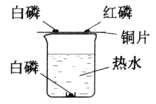
(1)由该实验得出,可燃物燃烧的条件是:
①与氧气接触;②__________________。
(2)实验中发生反应的化学方程式为________________,
(3)若使水中白磷燃烧,可往水中通人 _______________
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室制取气体所需装置如下图所示.
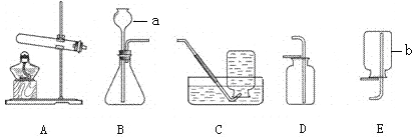
(1)实验仪器a、b的名称是a______、b_______.
(2)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_____(填序号),其反应的化学方程式是______.
﹙3﹚用高锰酸钾制取氧气,其反应的化学方程式是______。试管口应放_______________。 实验结束,停止加热前要先将导管移出水面,目的是__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在实验室里加热30g氯酸钾(KClO3)和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4g。请计算:(1)生成氧气的质量为________。 (2)原混合物中氯酸钾和二氧化锰的质量为________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室有一瓶长期放置的氢氧化钠固体,某兴趣小组同学欲对该固体变质情况进行探究。
Ⅰ.固体的成分分析
【提出问题】该瓶氢氧化钠固体是否变质,变质情况如何?
【查阅资料】①氢氧化钠在空气中容易变质但不会转化为NaHCO3;
②CaCl2溶液的pH=7。
③碱石灰是CaO和NaOH的混合物
【提出猜想】猜想Ⅰ:固体未变质,只有NaOH
猜想Ⅱ:固体全部变质,只有Na2CO3
猜想Ⅲ:固体部分变质,是NaOH 和Na2CO3 的混合物
【原因分析】氢氧化钠在空气中变质的原因是_______________(用化学方程式表示)。
【进行实验】小聪同学取少量样品于烧杯中,用足量水溶解,再向溶液中滴入几滴酚酞试液,溶液变红,由此他得出猜想Ⅰ正确,但其他同学很快予以否定,否定的理由是________________,为了进一步得出结论,组内其他三位同学分别取小聪实验后的溶液于试管中,进行如下表所示实验。
同学
小钱
小徐
小陆
实验操作
加入适量氢氧化钙溶液
加入过量氯化钙溶液
逐滴加入稀盐酸至过量
【实验结论】小钱、小徐的实验中都观察到有白色沉淀生成且溶液仍是红色,于是他们都得出猜想Ⅲ正确。
【反思评价】(一)老师指出,仅凭小钱的实验操作和现象无法确定猜想Ⅲ正确,理由是__________________。
(二)根据小徐的结论推测小陆实验现象是_________________________________。
Ⅱ 固体中各成分含量
【提出问题】如何测定变质的氢氧化钠固体中碳酸钠的质量分数?
【进行实验】化学小组同学设计了如下实验装置。
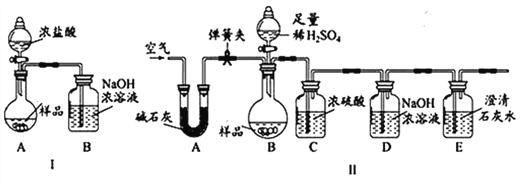
(一)小陆同学认为通过测定装置 I中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组内同学通过讨论认为不可以,其理由可能是 _______________________;
(二)小钱同学在大家讨论的基础上,设计了装置II。请分析:装置II中A的作用_____________;若无装置C,对测定结果造成的影响是_____________(填“偏大”、“偏小”或“无影响”);E装置的作用是_______________________________。
【实验结论】称取10g样品于圆底烧瓶中,实验结束后,测得装置D增重2.2g,请你计算出样品中Na2CO3质量分数为____________。(写出计算过程)
【反思评价】(一)实验室中的氢氧化钠应密封保存,除了因为空气中有二氧化碳,还因为___________。
(二)若将上述5g氢氧化钠固体全部溶解在45g水中,得到的溶液中氢氧化钠质量分数______10%(填“大于”、“小于”或“等于”)。
相关试题

