【题目】某化学实验小组对“影响石灰石与盐酸反应速率的因素——盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与。
【进行实验】
室温下,选用20 mL不同溶质质量分数的盐酸(4%和6%)分别与1 g颗粒状或块状的石灰石进行实验(固定夹持仪器略去)。
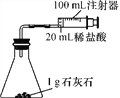
(1)石灰石与盐酸反应的化学方程式为____________________________________________________。
(2)按上图装置进行实验,在装药品前应检查该装置的气密性。开始实验时,应将20 mL稀盐酸________(填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
【处理数据】
(3)实验小组进行实验后,获得的相关实验数据如下表所示:
实验 编号 | 盐酸溶质质 量分数(均取 20 mL) | 石灰石固 体形状 (均取1 g) | 二氧化碳的 体积(mL)(均 收集前30 s 的气体) |
a | 4% | 颗粒 | 64.0 |
b | 4% | 块状 | 40.4 |
c | 6% | 颗粒 | 98.2 |
d | 6% | 块状 | 65.3 |
①要比较不同溶质质量分数的盐酸对反应速率的影响,可选择的实验编号是________(写一组),由此可得到的结论是____________________________。
②从上述实验中得出石灰石的颗粒大小对反应速率影响的结论是____________________。
【拓展延伸】
(4)下表是实验时记录生成的二氧化碳气体体积和对应的时间的一组实验数据(每间隔4 s读数一次):
时间/s | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
气体 体积/ mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
从上表数据可以分析得出,到20 s后反应速率逐渐变_______,其主要原因是_____________________。
参考答案:
【答案】 CaCO3+2HCl===CaCl2+H2O+CO2↑ 快速 a和c(或b和d) 盐酸溶质质量分数越大,反应速率越快 石灰石颗粒越小,反应速率越快 慢 随着反应的不断进行,盐酸中溶质的质量分数逐渐减小
【解析】(1)石灰石的主要成分是碳酸钙,与盐酸反应的化学方程式为CaCO3+2HCl===CaCl2+H2O+CO2↑;(2)开始实验时,应将20 mL稀盐酸快速推入锥形瓶中,以保证盐酸能全部推入锥形瓶中;如果缓慢推入,因生成二氧化碳在,装置内压强增大,不易将盐酸全部推入。(3) a和c(或b和d) 都只有盐酸的浓度不同,其它影响反应速率的因素都相同,所以可比较不同溶质质量分数的盐酸对反应速率的影响; (4).根据反应所需要的时间,可知盐酸溶质质量分数越大,反应速率越快; (5). 石灰石颗粒越小,与盐酸接触越充分,反应速率越快; (6). 到20 s后反应速率逐渐变慢 ,原因是随着反应的不断进行,溶液中的溶质越来越少,盐酸中溶质的质量分数逐渐减小,使反应物接触不充分,反应速率就慢了。
-
科目: 来源: 题型:
查看答案和解析>>【题目】有关氧气的说法,正确的是( )
A. 带火星的木条一定能在含有氧气的集气瓶中复燃
B. 工业上可用分离液态空气的方法制氧气属于分解反应
C. 木炭在氧气中的燃烧实验,要把红热的木炭迅速放入集气瓶底部
D. 无色氧气变成淡蓝色的液氧的变化属于物理变化
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列灭火方法不合理的是
A.炒菜时油锅不慎着火,可用水扑灭
B.森林发生火灾,可砍掉部分树木,形成隔离带
C.堆放杂物的纸箱着火,用水浇灭
D.不慎碰到酒精灯,酒精在桌面上燃烧,立即用湿抹布扑盖
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室在进行双氧水制备氧气实验时,某同学不小心将硫酸铜溶液滴加到试管中,发现立即有大量气泡产生,该同学就此对“硫酸铜对过氧化氢溶液的分解是否也有催化作用”的课题进行研究,以下是探究的主要过程:
【提出猜想】硫酸铜可以作过氧化氢溶液的催化剂。
【实验方案】常温下取两瓶H2O2溶液,其中一瓶加入一定量的硫酸铜(另外一瓶不加),测量各生成一瓶(相同体积)O2所需要的时间。
【进行实验】如图所示为进行实验的装置图,此实验中B处宜采用的气体收集方法是____________。
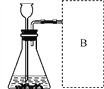
【实验记录】
实验编号
1
2
反应物
6%的H2O2
6%的H2O2
反应物的量/mL
2
2
加入物质名称
不加任何物质
1 g CuSO4
时间/s
270
40
【得出结论】由该实验过程可知硫酸铜溶液对双氧水分解具有催化作用,则该实验过程发生反应的化学方程式为________________________。
【实验反思】实验结束后,小明又对硫酸铜溶液中哪种微粒对双氧水分解产生催化作用产生兴趣(该溶液中有Cu2+、SO
 和H2O),并进行猜想:①可能是水分子;②可能是________;③可能是Cu2+。
和H2O),并进行猜想:①可能是水分子;②可能是________;③可能是Cu2+。小明将此猜想与同学小芳进行讨论,小芳立即否决了猜想①,原因是________________________。
【查阅资料】Na+、NO
 对双氧水的分解没有催化作用,据此小明在实验室里选择了两种试剂进行了实验探究,它们分别为________和________。
对双氧水的分解没有催化作用,据此小明在实验室里选择了两种试剂进行了实验探究,它们分别为________和________。 -
科目: 来源: 题型:
查看答案和解析>>【题目】某研究性学习小组的同学为探究金属镍(Ni,银白色金属)和铜的活动性顺序,进行了一系列实验活动。请你一起参与他们的活动,并回答有关问题。
探究活动一:金属镍和铜的活动性顺序
实验方案
实验现象
实验结论
将金属镍加入到盛有硫酸铜溶液的试管中
溶液的颜色变浅,有______色固体析出
镍比铜的金属活动性强
若在生成物中Ni为+2价,则该反应的化学方程式为________________________。
实验过程中,小组同学还发现试管中有无色气体产生的“异常”现象,十分好奇,于是继续进行探究活动。
探究活动二:无色气体的成分是什么?
【猜想假设】A.氢气 B.氧气 C.二氧化硫 D.二氧化碳 E.一氧化碳
【分析推理】小明认为无色气体不可能是二氧化碳或一氧化碳,理由是___________________。
小红根据二氧化硫能够形成酸雨的事实,推测二氧化硫与二氧化碳的化学性质相似。小组同学认为小红的观点合理,于是将收集到的气体通入____________中,发现溶液________,证明无色气体不是二氧化硫。
综上所述,小组同学认为,无色气体可能是氢气,或者是氧气。
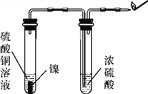
【设计方案】为确定气体成分,小组同学设计了如下实验方案:
用如图所示装置进行实验,先______________,然后将燃着的木条放在尖嘴处,发现气体燃烧并发出淡蓝色火焰,证明无色气体可能是氢气。
该实验方案中浓硫酸的作用是________________。
【评价与反思】小组同学认为,还可以补充一个实验,验证无色气体中含有氢元素,从而进一步证明无色气体可能是氢气。他们应补充的实验是__________________________________________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质是由离子构成的是
A.氯化钠 B.氮气 C.汞 D.磷
-
科目: 来源: 题型:
查看答案和解析>>【题目】把下列物质分别放入适量水中,充分搅拌,能够得到溶液的是
A.石灰石 B.冰 C.植物油 D.酒精
相关试题

