【题目】某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如下图所示。(结果保留两位小数)
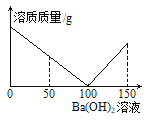
(1)参加反应的Ba(OH)2质量共有 g。当滴加Ba(OH)2溶液50g时,烧杯内溶液的pH 7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数(写出答题过程,结果保留0.01%)。
(3)在下图中画出产生沉淀质量与滴加Ba(OH)2溶液的质量关系。

(4)滴加Ba(OH)2溶液至150g时,所得溶液的溶质质量分数为 (结果保留0.01%)。
参考答案:
【答案】(1)3.42;<;(2)3.92%;(3)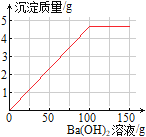 ;(4)0.87%
;(4)0.87%
【解析】对失去标签的稀硫酸浓度进行测定。根据所学知识和题中信息知,(1)参加反应的Ba(OH)2质量共有3.42%×100g=3.42 g。当滴加Ba(OH)2溶液50g时,此时硫酸过量,溶液呈酸性,烧杯内溶液的pH<7。
(2)解∶设该硫酸溶液的溶质质量分数为x
H2SO4+Ba(OH)2=BaSO4↓+2H2O
98 171
50g×x 3.42g
![]() =
=![]() ,x=3.92%。
,x=3.92%。
(3)产生沉淀质量与滴加Ba(OH)2溶液的质量关系图∶
(4)解∶设生成硫酸钡质量为x
H2SO4+Ba(OH)2=BaSO4↓+2H2O
171 233
3.42g x
![]() =
=![]() ,x=4.66g。
,x=4.66g。
滴加Ba(OH)2溶液至150g时,所得溶液的溶质质量分数为∶
![]() ×100%=0.87%。
×100%=0.87%。
点睛∶灵活应用质量守恒定律和正确书写化学方程式是顺利完成本题的重要保证。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图的实验常用仪器回答有关问题。
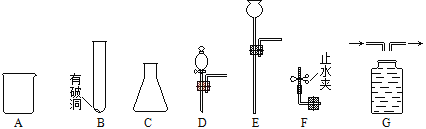
(1)仪器A的名称______________。
(2)若用过氧化氢制备氧气并控制反应速率,应选用上述仪器中的_____(填序号),其化学反应方程式为______。
(3)若用Zn和稀硫酸制备氢气并使反应随时发生或停止,应选仪器_____(填序号),其反应方程式为____。
①用充满水的G收集H2,请将图G补画完整。
②为了获得纯净的硫酸锌晶体,可先加入过量的________或________除去制H2后溶液中过量的酸,过滤,______,降温结晶,得到硫酸锌晶体。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小明拿起家中的水壶准备煮水时,发现壶内有些褐色的固体。为了探究其成分,与兴趣小组同学查阅资料后获知这些褐色的固体是水垢,它可能是因为水中含有Ca(HCO3)2和Mg(HCO3)2等可溶性物质在加热时生成了CaCO3和Mg(OH)2。
(1)含有较多Ca(HCO3)2的水称_____(填“硬水”或“软水”),加热时发生反应的化学方程式为__________。
(2)小明认为本市属喀斯特地貌,以石灰岩为主,该水垢的成分只有CaCO3;但小白不同意,认为也可能只有Mg(OH)2,还可能______________。
(3)小明为了证明自己的猜想,设计如下实验方案:
实验操作
现 象
结 论
①取少量水垢于试管中,加入过量的_______。
观察到现象_________,
反应的化学方程式__________。
水垢中有CaCO3
②向①反应后的试管中滴加2-3滴NaOH溶液
观察到现象__________。
水垢中没有Mg(OH)2,
我的猜想成立
(4)小白不认可小明的结论,认为他的实验操作有缺陷,原因是_________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】五水合硫酸铜(化学式:CuSO4·5H2O)也被称作硫酸铜晶体,俗称蓝矾或胆矾。具有催吐、祛腐、治风痰壅塞、癫痫、牙疳、口疮、痔疮、肿毒的功效并且有一定的副作用。
(1)五水合硫酸铜中由_______种元素组成,原子个数比:S:O:H=_______________。
(2)五水合硫酸铜中硫酸铜的质量分数___________%;将25g五水合硫酸铜放入100g水中充分搅拌后完全溶解,所得溶液的溶质质量分数为________________%。(结果保留0.1%)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列关系曲线不能正确反映其对应变化关系的是( )
A.
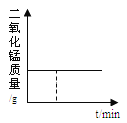 加热KClO3和MnO2固体混合物
加热KClO3和MnO2固体混合物B.
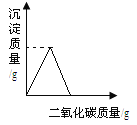 向Ca(OH)2溶液中通入CO2至过量
向Ca(OH)2溶液中通入CO2至过量C.
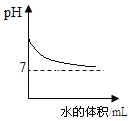 向一定浓度的NaOH溶液中加水稀释
向一定浓度的NaOH溶液中加水稀释D.
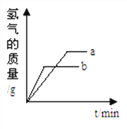 将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al
将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al -
科目: 来源: 题型:
查看答案和解析>>【题目】根据如图中A、B、C三种物质(均不含结晶水)的溶解度曲线,回答下列问题:
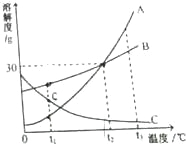
(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 。
(2)t2℃时,向100水中加入20A物质,充分溶解后,所得溶液是 (填“饱和”或“不饱和”)溶液。
(3)将t3℃时等质量A、B的饱和溶液分别降温至t2℃,对所得溶液的叙述正确的是 (填序号)。
①溶质质量:A>B
②溶剂质量:A<B
③溶质质量分数:A=B
-
科目: 来源: 题型:
查看答案和解析>>【题目】A﹣J及X均为初中化学所学的物质,它们相互转化的关系如图所示(部分生成物未标出).其中C为常见建筑材料的主要成分,F为蓝色沉淀,H为不溶于稀硝酸的白色沉淀,I和X为常见的金属单质,E为蓝色溶液,J为浅绿色溶液,B、D、E、G、J的溶液中只含一种溶质.
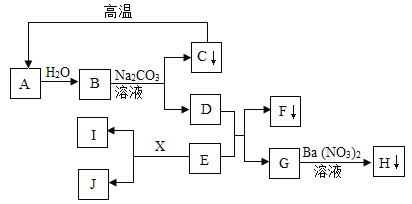
据此,请回答下列问题:
(1)物质H的化学式为_____
(2)写出下列化学方程式:B+Na2CO3→C+D_______________________________。
(3)D+E→F+G的基本反应类型_________________。
相关试题

