【题目】空气对人类十分重要,某兴趣小组计划对空气成分进行探究,以下是他们的实验设计方案:
空气→除去二氧化碳和水蒸气→除去氧气→氮气
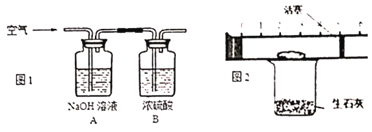
(1)除去二氧化碳和水蒸气:(如图1)
①装置A中发生反应的化学方程式______。
②装置A、B的顺序能否调换______(填“能”或“不能”)。
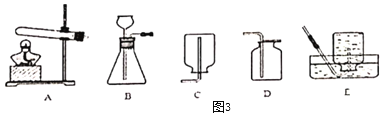
(2)除去氧气:(如图2)
烧杯上方玻璃容器中是经过图1收集的气体样品,容器内装有过量的白磷,实验开始前活塞处在5厘米处(活塞可以左右滑动且装置气密性良好),实验开始时向烧杯中加入适量的水。如图进行实验,试回答:(白磷的着火点为40℃,燃烧的现象与产物与红磷燃烧相同)。
①向烧杯中的生石灰加入水的作用是______。
②白磷燃烧的反应属于基本反应类型中的______反应。
③实验结束恢复至常温,活塞应停在______(填数字)厘米附近。
(3)拓展延伸:实验室制取氮气(如图3)
查阅资料:I氮气的密度和空气十分接近,难溶于水;
II重铬酸铵(NH4)2Cr2O7是一种桔黄色的固体粉末,在加热后能够分解生成氮气、水、三氧化二铬。
①实验室获得氮气应该选择的发生装置和收集装置分别是______、______(填字母序号)。
②重铬酸铵受热分解的化学方程式为______。
③实验室用装置B和E组合可以制取的常见气体是______(填化学式)。
参考答案:
【答案】2NaOH+CO2=Na2CO3+H2O 不能 反应放热使温度达到白磷的着火点 化合 4 A E (NH4)2Cr2O7![]() Cr2O3+4H2O+N2↑ O2、H2
Cr2O3+4H2O+N2↑ O2、H2
【解析】
(1)①装置A中氢氧化钠和二氧化碳反应生成碳酸钠和水,故反应的化学方程式写为:2NaOH+CO2=Na2CO3+H2O。
②装置A、B的顺序不能调换,这是因为调换后无法除去水蒸气,故填不能。
(2)①向烧杯中的生石灰加入水的作用是:氧化钙和水反应生成氢氧化钙,放热,能使温度升高至白磷着火点,故填反应放热使温度达到白磷的着火点。
②白磷与氧气在点燃的条件下反应生成五氧化二磷,属于化合反应,故填化合。
③实验结束恢复至常温,由于原子约占空气总体积的五分之一,因此活塞应停在4厘米附近,故填4。
(3)①实验室获得氮气需要加热,应该选择的发生装置是A;氮气的密度和空气十分接近,不能用排空气法收集,难溶于水,可以用排水法收集,即用E装置收集,故填A;E。
②重铬酸铵受热分解生成氮气、水、三氧化二铬,故反应的化学方程式写为:(NH4)2Cr2O7![]() Cr2O3+4H2O+N2↑。
Cr2O3+4H2O+N2↑。
③实验室用装置B和E组合可以制取的常见气体是氧气、氢气等,这是因为利用过氧化氢溶液和二氧化锰制取氧气时不需要加热,可以用B装置收集,氧气不易溶于水,可以用排水法收集,利用稀硫酸和锌制取氢气时不需要加热,可以用B装置收集,氢气不溶于水,可以用排水法收集,故填O2、H2。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是某种饮料标签的部分信息,请回答下列问题:
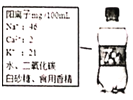
(1)取该饮料少许于试管中滴入紫色石蕊试液,会发现试液______(填现象),其原因是______(用化学方程式解释)。
(2)饮料瓶的材料是PET,化学式为(C10H8O4)。PET中氢原子与氧原子的个数比是______(填最简整数比),碳元素的质量分数为______。
(3)白砂糖在一定条件下可转化为葡萄糖(C6H12O6),葡萄糖在酶的作用下又可以发生如下反应:C6H12O6
 2X+2CO2↑,则X的化学式为______。
2X+2CO2↑,则X的化学式为______。 -
科目: 来源: 题型:
查看答案和解析>>【题目】“西气东输“是我国重要的能源战略之一,“气”指的是天然气,回答下列问题:
(1)天然气中常加入少量具有特殊刺激性气味的乙硫醇(C2H5SH),便于及时发现天然气是否泄漏。天然气的主要成分是______(填物质名称)。
(2)乙硫醇完全燃烧生成二氧化碳、二氧化硫和水,其化学方程式为______。
(3)天然气第一次通过管道输送到用户时,需先在管道内注满氮气,目的是______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】元素周期表是学习和研究化学的重要工具,请分析图中的信息并回答下列问题。

(1)位于第三周期VIA族的元素是______(填元素符号),氟元素位于周期表中的第______周期ⅦA族。
(2)表中与氮元素化学性质相似的元素是______。
(3)如图所示是电解水的验装置,若水分子用“
 ”来表示,请画出气体a的图示______。
”来表示,请画出气体a的图示______。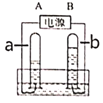
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图表示稀硫酸和氢氧化钠溶液发生反应时烧杯中溶液的pH随加入液体体积的变化曲线,请回答下列问题:
(1)烧杯中盛放的液体是______(填字母:A.稀硫酸B.氢氧化钠溶液),烧杯中发生反应的微观实质是______。
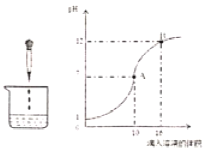
(2)曲线上A点表示______,B点时溶液中的离子有______(填离子符号)
(3)小强完成上述实验几天后发现,忘记盖上盛放氢氧化钠溶液试剂瓶的瓶塞。小强设计了如下实验两个方案来检验氢氧化钠溶液是否变质以及变质的程度
实验方案
实验步骤
实验现象
实验结论
方案一
取少量溶液于试管中,滴加几滴稀盐酸
没有气体产生
没有变质
方案二
取少量溶液于试管中,滴加几滴氢氧化钙溶液
① ______
已经变质
②小东认为方案一的实验设计不严谨,其原因是:______。请写出方案二中反应的化学方程式______。
③如果要确定氢氧化钠溶液是部分变质还是完全变质,以下方案合理的是______(填字母,已知氯化钙溶液呈中性)
A.另取溶液少许,加入适量氢氧化钙溶液,过滤,再向滤液中加入酚酞
B.另取溶液少许,加入足量的氯化钙溶液,过滤,再向滤液中加入酚酞
C.另取溶液少许,加入少量的氯化钙溶液,过滤,再向滤液中加入酚酞
-
科目: 来源: 题型:
查看答案和解析>>【题目】味精的鲜味来自于“谷氨酸钠”(C5H8NO4Na),如图是某味精标签的部分信息,请回答下列问题:

(1)该味精中至少含有______(填数字)种元素。
(2)称取5g味精配制成50g溶液,如图是配制过程,正确的操作顺序是______(填字母),图④中玻璃棒的作用是______。

A.①③②⑤④B.③②①④⑤C.②③①⑤④D.②①③④⑤
(3)同学们欲测定味精中氯化钠的含量是否符合标签信息,向所配制的50g溶液中加入足量的硝酸银溶液,充分反应后过滤,将沉淀洗涤、烘干、称量,得到固体2.87g。求该味精中的氯化钠的含量是否属实。(写出解题过程)
提示:Ⅰ味精中的谷氨酸钠易溶于水,不与AgNO3反应,其余成分忽略不计;
IINaCl与AgNO3溶液能发生复分解反应。
(4)在其它操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,所配溶液中氯化钠的质量分数将______(填“偏大”、“偏小”或“无影响”,下同),所测定的味精中NaCl的质量分数将______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是金元素在元素周期表中的信息示意图。从图中获取的信息正确的是

A.金元素属于非金属元素
B.一个金原子的中子数为197
C.一个金原子的核外电子数为118
D.一个金原子中粒子总数为276
相关试题

