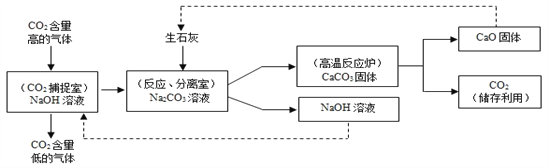
【题目】大气中CO2含量不断升高,使全球气候问题日趋严重。科学家们正在努力尝试通过下列途径减少CO2的排放:利用NaOH溶液来“捕捉”CO2,并将CO2储存或利用,流程如图。
下列有关该过程的叙述正确的是 ( )
该过程可实现CO2零排放
该过程中只有1种物质可以循环利用
C.分离室中分离物质的操作是蒸发
D.该过程至少发生了4个化学反应
参考答案:
【答案】D
【解析】A、由反应的流程图可知,在二氧化碳捕捉室中的氢氧化钠将大部分的二氧化碳吸收掉了,但还有少量的二氧化碳排放到了空气中,错误;B、由反应的流程图可知,氧化钙和氢氧化钠均可循环利用,错误;C、通过分离室分别得到了固体和液体,故分离室中分离物质的操作是过滤,错误;D、该过程反应的反应有:氢氧化钠和二氧化碳反应生成碳酸钠和水、氧化钙与水反应生成氢氧化钙、氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠、高温时碳酸钙分解生成氧化钙和二氧化碳,正确。故选D。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某种镁矿石的主要成分是碳酸镁,还含有较多的脉石(SiO2)和少量石灰石。下图是利用该镁矿石制备七水硫酸镁(MgSO4·7H2O)的工艺流程:
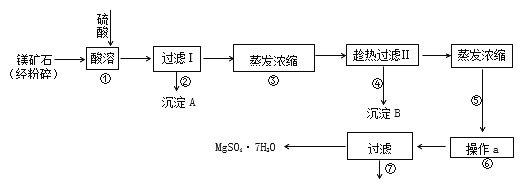
已知 CaSO4和MgSO4的溶解度曲线如下图所示:
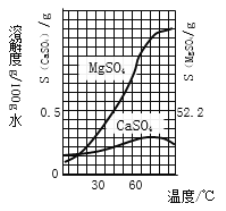
根据以上信息回答下列问题:
⑴写出步骤①中碳酸镁与硫酸发生反应的化学方程式________________________。
⑵上述流程中多次用到了过滤操作,实验室过滤时需要用到的玻璃仪器是玻璃棒、烧杯和_______。
⑶沉淀A的成分是SiO2和部分硫酸钙,过滤I后得到的滤液中的溶质除了MgSO4还有___________。
⑷步骤④趁热过滤的作用是____________________________________。
⑸步骤⑥的操作a名称是___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】生活与化学密切相关。食盐、酒精、水、铁粉、食醋是生活中常见的物质,请按下列要求填空。
(1)鉴别酒精和水,最简便可行的方法是_________________。
(2)以上物质中,可用于清除水垢的是__________,可用作食品干燥剂的是__________,可用作调味剂和防腐剂是__________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是
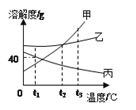
A. t2℃时,甲、乙两种物质的溶解度相等
B. 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>丙>甲
C. 甲的溶解度随温度的升高而增大
D. t1℃时,丙的饱和溶液中溶质的质量分数为28.6%
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列属于人体必需微量元素的是
A.H B.Zn C.Ca D.O
-
科目: 来源: 题型:
查看答案和解析>>【题目】某兴趣小组利用下列装置进行气体的制取实验,请回答下列问题.
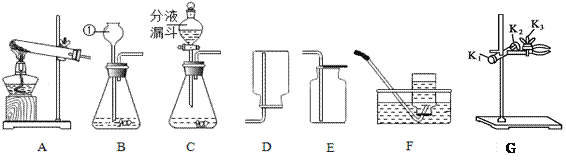
(1)写出标号①仪器的名称___________.
(2)用高锰酸钾制取和收集较纯净的氧气,选择的装置组合是___(填字母)写出反应的化学方程式______________________________,实验后发现制得的氧气不纯,可能的原因是_________________________.(答一点即可)
(3)如图G,要调节夹持试管的铁夹的松紧,应调节旋钮___(填“K1”“K2”或“K3”)。
(4)实验室制取二氧化碳的化学方程式______________________,与B相比,C作为制取二氧化碳的发生装置,优点是_______________,验证二氧化碳收集满的方法是______________________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】鸡蛋主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3,里面覆盖一层蛋壳膜。我校兴趣小组的同学为此开展了以下探究活动:
【提出问题1】鸡蛋白中主要的营养成分是______ ;
【查阅资料】
a、CaCO3灼烧分解生成氧化钙和一种无毒的氧化物。
b、蛋壳中的其它成分不参加反应。
c、NaHCO3+HCl= NaCl + H2O +CO2↑,Ba(OH)2+CO2=BaCO3↓+H2O,
d、已知仪器a装有10%的稀盐酸,其他成分均不与HCl反应,装置内试剂均足量。
【提出问题2】蛋壳中的CaCO3含量是多少呢?小华拟将该蛋壳放在空气中充分灼烧完成测定;小明拟通过蛋壳与稀盐酸反应完成测定。请你参与他们的探究。
【设计方案】他们分别称取12.0g蛋壳设计了以下不同的实验方案:
小华的方案:
称取12.0g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16g。则:减少的质量是______ (填化学式)的质量,经计算得蛋壳中的CaCO3的质量分数为______ 。
(3)小明的方案:小明设计了如下图所示的实验装置。
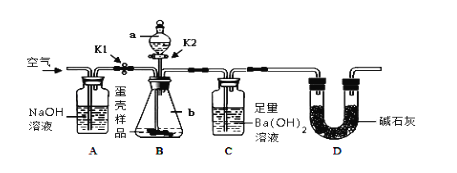
【实验步骤】
①按上图连接好装置后,并______ ;
②向B装置中加入蛋壳样品后,先通入空气一会儿;
③接下来的实验操作是______ ,直到______ 为止(填实验现象);
④再通入空气一会儿,至装置C中不再产生沉淀为止;
⑤将装置C中的固液混合物过滤、洗涤、烘干后称量其质量;
⑥重复上述实验。
【实验数据】重复实验,3次数据记录如下:
实验次数
实验1
实验2
实验3
装置C中沉淀质量(g)
19.68
19.75
19.67
【实验分析及数据处理】
①上述数据能否用托盘天平称量______ 。(填“能”或“不能”)
②若无A装置,直接通入空气,则测定结果将______ 。(填“偏大”、“偏小”或“不变”)D装置的作用是___
③实验重复3次的目的是______ 。
④请利用3次实验数据的平均值,计算该蛋壳中的CaCO3质量分数______ 。
【实验反思】
下列各项措施中,能提高小明测定准确度的是______ (填序号)。
Ⅰ.在装置A、B之间增加盛有浓硫酸的洗气瓶
Ⅱ.缓缓滴加稀盐酸
Ⅲ.在装置B、C之间增加盛有饱和NaHCO3的洗气瓶
IV.直接称量装置C反应前后的质量
相关试题

