Ⅰ.探究浓硫酸的某些性质
(1)称量E的质量;按照图示连接装置,检查装置的气密性。简述检验发生装置气密性的方法__________________________________________________________
___________________________________________________________________。
(2)将m g铁碳合金样品放入A中,再加入适量的浓硫酸。仪器A的名称为______。未点燃酒精灯前,A、B均无明显现象,其原因是:________________________
____________________________________________________________________。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象。
写出A中碳发生反应的化学方程式______________________________________。
B中的现象是 。
(4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式 (只写一个)_________________________________________________________。
(5)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是______________________________________________________。
Ⅱ.测定铁的质量分数
(6)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。铁碳合金中铁的质量分数为________________________________________(写表达式),
(7)某同学认为上述方法较复杂,使用右图所示的装置和其他常用实验仪器测定某些数据即可。为了快速准确的计算出铁的质
- 答案
一. 选择题:(3分×16=48分)
题 号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
答 案
D
C
A
A
C
D
A
D
C
B
D
D
B
A
C
C
二.(本题共14分)
17:Ⅰ.(4分,每空1分)(1)AEF;(2)BDE ;AF;(3)F>A>C>B>E。
Ⅱ.(10分)本题答案有开放性,合理即可给分。
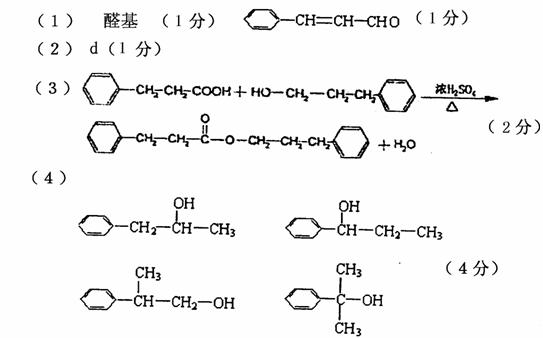
⑴①C(或Fe) (1分) ②
⑵CuO(Fe2O3等)(1分)
⑶①CaC2+2H2O=Ca(OH)2+C2H2↑ ;(2分) ②麦芽糖;(1分)
⑷①Na2CO3+CO2+H2O=2NaHCO3 ;(2分) ②红褐色固体。(1分)
三.(本题共20分)
18.(10分)(1)高氯酸 (1分) (2)离子键和非极性键 (1分)
(3)2I-+ClO-+H2O=I2+Cl-+2OH- (2分)
(4)2H++2e- = H2↑ (2分) 0.71g (2分)
(5)2H2(g)+O2(g)=2H2O(g) ΔH=-4QkJ/mol (2分)
19.(10分)
(1)③④⑥(2分) (2)Ca(OH)2 或 Ba(OH)2(2分)
(3)2Na + 2H2O = 2Na++ 2OH- + H2↑(2分)
(4)氧化还原:2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑ (2分)
非氧化还原:AlCl3 + 4NaOH = NaAlO2 +3NaCl +2H2O (2分)
或Al(OH)3 + NaOH = NaAlO2 + 2H2O
或Al2O3 + 2NaOH = 2NaAlO2 + H2O
(其它合理答案酌情给分)
四. (本题共9分) (每空1分)
20.Ⅰ(1)关闭分液漏斗的活塞,在B中加水至浸没长导管口,用酒精灯微热(或用手热),长导管口有气泡冒出,停止加热,长导管内形成一段水柱,说明装置的气密性良好。
(2)圆底烧瓶; 常温下,Fe在浓硫酸中钝化,碳不与浓硫酸反应
(3)C+2H2SO4(浓)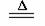 CO2↑+2SO2↑+2H2O; 品红溶液逐渐褪色
CO2↑+2SO2↑+2H2O; 品红溶液逐渐褪色
(4)2Fe3++Fe=3Fe2+(或Fe+2H+=Fe2++H2↑)
(5)铁碳在酸溶液中形成原电池
Ⅱ(6)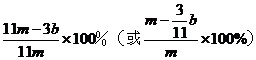 (7)C
(7)C
五.(本题共9分) 21.