15.(10分)国家环保总局于
一、滴定原理
①酸化的水样以硝酸汞[Hg(NO3)2]进行滴定时,生成难电离的氯化汞,滴定到终点时,过量的汞离子与指示剂二苯卡巴腙生成蓝紫色的二苯卡巴腙的汞络合物指示终点。
②饮用水中各种物质在通常的浓度下滴定时不发生干扰,但水的色质及高价铁、六价铬、硫化物对实验有干扰。
二、试剂
①配制氯化钠标准溶液和硝酸汞溶液,并用氯化钠标准溶液标定硝酸汞溶液
②配制氢氧化铝悬浊液、30%过氧化氢溶液及1%对苯二酚溶液等
三、 滴定
①水样加入氢氧化铝悬浊液振荡过滤
②若水样中有可溶性硫化物,需加氢氧化钠调至中性或弱碱性后,加入30%过氧化氢
③若水样含高铁离子或铬酸盐,可加2mL新配制的对苯二酚溶液
- 答案
1
2
3
4
5
6
7
8
D
B
C
A
C
D
D
C
9
10
11
12
13
14
╆╆╆╆╆
╆╆╆╆╆
CD
D
D
CD
B
AD
~~~~~
~~~~~
15.每空均2分,共10分
(1)吸附水中有色物质(脱色);(2)S2-+H2O2=S+2OH―(或:S2-+H2O2+2H+=S↓+2H2O);(3)将水样可能含有的高铁离子及铬酸盐还原;(4)偏低
(5)V1×2c×35.5×1000/V=71000CV1/V
16.(8分)
(1)第三周期第VIIA族 (2分)
(2) 2SO2(g)+O2(g) 2SO3(g)
△H=-196.6 kJ・mol-1 (2分)
2SO3(g)
△H=-196.6 kJ・mol-1 (2分)
(3)Al3++3AlO2-+6H2O=4Al(OH)3↓ (2分) (4) H2O (2分)
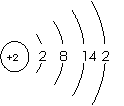 |
17.(10分)
(1) (2分)
(2)2FeCl2+Cl2===2FeCl3 (2分)
(3)2Al+2OH-+2H2O=2AlO2-+3H2↑(2分)
(4)阳极:6O2--12e-=3O2↑;阴极:4Al3++12e-=4Al (每空1分)
(5)错误!未找到引用源。 (2分)
18.⑴S2- + H2O HS- +OH- HS- + H2O
HS- +OH- HS- + H2O H2S +OH-(可不写)
H2S +OH-(可不写)
⑵2.7×10-3 ⑶172.5 ⑷使BaSO4得到充分的还原(或提高BaS的产量)
①②为吸热反应,炭和氧气反应放热维持反应所需高温
19.(12分)
(1)D(2分)
(2)Cu(1分)
(3)H2(1分);①随着反应进行生成铝离子浓度增大,水解程度增大,产生H+的浓度增大,②该反应放热,升高温度反应加快,③铜与铝构成原电池,加快铝溶解。(3分)
(4)A、B、D (3分)
(5)A(1分),电解质性质(合理解答同样给分)(1分)
20.(共10分)
(1)解: 2SO2(g) + O2(g)  2SO3(g)
2SO3(g)
起始浓度/ mol・L-1 0.050 0.030 0
平衡浓度/ mol・L-1 (0.050-0.040) (0.030-0.040/2) 0.040
= 0.010 = 0.010
所以,K =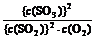 =
= 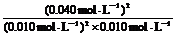 = 1.6×103 mol・L-1。(不带单位计算也得分)
= 1.6×103 mol・L-1。(不带单位计算也得分)
(SO2)
=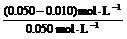 ×100%
= 80% 。
×100%
= 80% 。
(2)B、C。 (3)SO2+H2O+Na2SO3=2NaHSO3。
(4)抑制Fe2+、Fe3+的水解,防止Fe2+被氧化成Fe3+。
21.(12分)
解:(1)6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O (2分)
(2)n(Fe)=×2=0.035 mol n(SO42-)==0.045 mol
n(OH-)=3×n(Fe3+)-2×n(SO42-)=3×0.035 mol-2×0.045 mol=0.015 mol (3分)
盐基度=×100%= ×100%=14.29% (2分)
(3)n(H2O)=
=0.054 mol
化学式: Fe35(OH)15(SO4)45・54H2O (3分)

