21.(12分)A、B、C是中学化学中常见的三种短周期元素。已知①A元素原子最外层电子数是次外层电子数的2倍。②B元素最高正价与负价的代数和为2。③C元素有多种化合价,且常温下C元素的单质与某种一元碱溶液反应,可得到两种含C元素的化合物。④B、C两种元素质子数之和是A元素质子数的4倍。
( 1 ) 写出A、B、C三种元素的名称:A B C
( 2 ) 写出C的单质和强碱溶液反应的离子方程式 。
(3)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种常见的漂白性物质。则X的分子式 。分子中B、C原子间的化学键的类型为 。(填“极性键”或“非极性键”)X与水反应的化学方程式 。
(4)A、B两种元素可形成一种硬度比金刚石还大的化合物Y。在化合物Y中,A、B两原子以单键相结合,且每个原子的最外层均达到8个电子的稳定结构。则Y的化学式为 , Y的硬度比金刚石硬度大的原因是 。
- 答案
一、选择题
1D,
二、填空题
21.(12分)
(1)A:碳 B:氮 C:氯 (各1分)
(2)Cl2+2OH-=Cl-+ClO-+H2O(2分)
(3)NCl3 (1分)极性键(1分) NCl3+ 3H2O=NH3+3HClO (2分)
(4)C3N4 (1分)因为N的原子半径比C的原子半径小,键长更短,所以C3N4的硬度比金刚石硬度大。(2分)
三、实验题
22.(12分) (1)c (1分)
(2)①(Ⅰ)饱和碳酸氢钠溶液; (Ⅱ)吸收未反应的NH3(答“防止倒吸”或“吸收CO2”不给分));
(Ⅲ)过滤 (每空1分,共3分)
②(Ⅰ)a、NH3, b、CO2; (每空1分,共4分)
(Ⅱ)增大气体与溶液接触面积,提高CO2吸收率; (2分)
(3)用碳酸氢铵与适量饱和食盐水反应。(或往烧碱溶液中通入过量CO2 ;往饱和Na2CO3 溶液中通入过量CO2 等。其他合理方法均可) (2分)
四、推断题
|

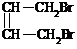 +2NaOH→
+2NaOH→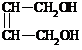 +2NaBr (2分)
+2NaBr (2分)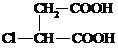 (5分)
(5分)