18.(8分)某化工厂按如下步骤进行生产:①以煤为燃料煅烧石灰石;②用饱和Na2CO3溶液吸收步骤①中产生的CO2 (转化为Na2HCO3);③使步骤①中产生的CaO跟水反应;④消石灰跟Na2CO3溶液反应。
(1)生产过程中没有涉及到的化学反应类型是______________________________
(2)该厂生产过程中涉及的物质有:①煤②纯碱③小苏打(NaHCO3)④烧碱⑤二氧化碳⑥消石灰.下列叙述中正确的是_________
A.起始原料是①② B.起始原料是②⑥
C.最终产品是④⑤ D.最终产品是③④
(3)该厂生产过程的优点可能有__________
①排放的气体对大气无污染. ②生产过程中的部分产品可作为起始原料使用. ③无高温作业
(4)写出④反应的反应方程式_______________________
- 答案
一、选择题
题号
1
2
3
4
5
6
7
8
9
10
答案
A
B
D
B
C
B
C
B
A
C
二、选择题
题号
11
12
13
14
15
16
答案
D
B
BC
AD
BC
AB
三、填空、简答和计算
17.H+、Mg2+、Fe3+;S2-、I-;Fe2+ S。
18.(1)置换反应;(2) AD;(3) ①②
19. KClO3 ,Cl2, 1∶1, 5∶1, 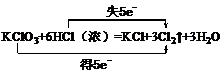
20.(1)Fe+CuSO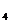 ==FeSO
==FeSO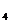 +Cu (2)2CO+O
+Cu (2)2CO+O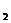 ==2CO
==2CO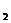
(3) 2KClO3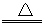 2KCl+3O2↑(4)CuO+ H2
2KCl+3O2↑(4)CuO+ H2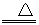 Cu+H2O (5) CuO+ CO
Cu+H2O (5) CuO+ CO 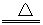 Cu+ CO2
Cu+ CO2
21.氧化产物可能为O2,还原产物可能为H2O.
22. (1)Cl2 ,NH3 (2)6e- (3)213:28 (4)34
23.解:设
MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O
87 2×36.5 71
m
m1=
MnO2%=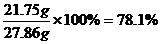
答:这种软锰矿石中MnO2的百分含量为78.1%;被氧化的HCl为

