1.下列叙述错误的是 ( )
A.1mol任何物质都含有约6.02×1023个原子
B.
C.在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类
D.物质的量是国际单位制中七个基本物理量之一
2.下列关于摩尔质量的叙述正确的是 ( )
A.摩尔质量是1 mol物质的质量
B.以g・mol-1为单位时,在数值上摩尔质量与相对分子质量或相对原子质量相等
C.水的摩尔质量等于NA个水分子的相对分子质量之和
D.单位物质的量的物质所具有的质量叫摩尔质量
3.
A.0.1mol B.0.2mol C.6.02x1022个 D.1.204x1023
4.下列叙述中,正确的是 ( )
A.同质量的H2与Cl2含有的分子数同样多
B.SO42- 的摩尔质量是
C.阿伏加德罗常数恰好为6.02×1023mol-1
D.二氧化碳的摩尔质量是
5.l g N 中含有n个N
中含有n个N 分子,则阿伏加德罗常数N
分子,则阿伏加德罗常数N 可以表示为
( )
可以表示为
( )
A.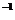 B.28n mol
B.28n mol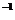 C.
C.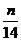 mol
mol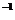 D.
D.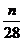 mol
mol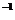
6.某元素1个原子的质量为a g,1 个
A.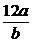 B.
B.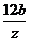 C.
C.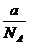 D.a・NA
D.a・NA
7.下列物质中原子数最多的是 ( )
A.
C.0.8mo1NH3 D.
8.在反应 3Cl2+6KOH = 5KCl+KClO3+3H2O 中,氧化剂与还原剂的物质的量之比为( )
A.1:5 B.2:
9.等物质的量的钠、镁、铝与足量稀H2SO4反应生成的氢气的物质的量之比是 ( )
A.1:1:1 B.1:2:
10. 将
A.0.1 mol B.1 mol
C.10 mol D.100 mol
11.已知NA表示阿伏加德罗常数。下列说法中不正确的是 ( )
A.醋酸的摩尔质量与NA个醋酸分子的质量在数值上相等
B.
C.NA个氧分子和NA个氢分子的质量比为8:1
D.0.5NA氯分子的质量为
12.若某氖原子质量是a g,
A.氖元素的相对原子质量一定是
C.Wg该氖原子的物质的量一定是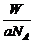 mol D.Wg该氖原子所含质子数是10W/a
mol D.Wg该氖原子所含质子数是10W/a
13.把0.5molNa投入过量的a g水中得到m g溶液;把0.5mol Mg投入到过量的a g盐酸中得到m′g溶液,则m与m′的关系为 ( )
A.m>m′ B.m<m′ C.m=m′ D.无法确定
14.完全中和
A.该酸的摩尔质量为
C.
15.Na、Mg、Al、Fe四种金属中的两种组成的混合物
A.Na B.Mg C.Al D.Fe
16.(6分)
H2SO4的摩尔质量是______________,
17.(7分)1个
(2)铝的相对原子质量为27,则其摩尔质量为_________,若阿伏加德罗常数取
6.02×1023mol-1,则可估算一个铝原子的质量约为_______________g.
18.(5分)(1)1molNa、1molNa+和1molOH-所含电子的物质的量分别为_____、_____、______
(2)4.6gNa与足量的水反应,反应中钠失电子数为__________
19.(6分)下列物质中,物质的量最大的是________,含分子个数最多的是________,含原子个数最多的是________,质量最大的是________。
A.
E.27mL水
20.(6分) 有A、B、C三种一元碱,它们的分子量之比为3:5:7,如果把7mol A、5mol B、3molC混合均匀,取混合碱
21.(8分)已知
28、 据题意有 A+B====C+D
16 20 W 4.5
根据质量守恒定律W=16+20-4.5=31.5(g)。由上述数据可以看出当15gB与8g A反应时,B过量,应用A的质量进行求算:设此时生成的C为xg,
A+B====C+D
x=15.75(g)
所以C的摩尔质量为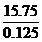 =126(g/mol)
=126(g/mol)
22.(12分)有一块锌片插入足量CuSO4溶液中,锌片质量减轻了
(1)参加反应的锌的物质的量。
(2)析出铜的物质的量。
(3)生成ZnSO4的物质的量及质量。
(4)溶液的质量是增加了还是减少了。