【题目】W、X、Y、Z、N、M六种主族元素,它们在周期表中位置如图所示,下列说法不正确的是
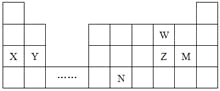
A. 原子半径:Y>Z>W
B. 单质的还原性:X>Y
C. 溴与元素M同主族,最高价氧化物的水化物的酸性比M的强
D. 元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料
参考答案:
【答案】C
【解析】A. 同周期元素原子半径随着核电荷数增大而减小,所以原子半径Y>Z,同主族元素原子半径随着原子序数增大而增大,所以原子半径Z>W,总之,原子半径:Y>Z>W,故A正确;B. 单质的氧化性:Y>X,所以单质的还原性:X>Y,故B正确;C. 非金属性:溴<M,所以最高价氧化物的水化物的酸性M比溴的强,故C不正确;D. 元素N为锗,位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料,故D正确。故选C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】有一无色未知溶液中检验出有Ba2+、Ag+,同时又测得其酸性很强.某学生还要鉴定此溶液中是否大量存在①Cu2+ ②Al3+ ③Cl﹣ ④NO3﹣ ⑤NH4+ ⑥CO32﹣⑦Na+ ⑧Mg2+ ⑨Fe3+,而事实上有部分离子不用鉴定就能加以否定,你认为不必鉴定的是
A. ③⑤⑥⑨ B. ①③⑥⑨ C. ③④⑦⑧⑨ D. ①②⑨
-
科目: 来源: 题型:
查看答案和解析>>【题目】某固体可能含有NH4+、Cu2+、Na+、Cl-、CO32-、SO42-中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况)。
下列说法正确的是
A. 该固体中一定含有NH4+、CO32-、SO42-、Na+ B. 该固体中一定没有Cu2+、Cl-、Na+
C. 该固体中只含有NH4+、CO32-、SO42-、Cl- D. 根据以上实验,无法确定该固体中有Na+
-
科目: 来源: 题型:
查看答案和解析>>【题目】向BaCl2溶液中通入SO2将溶液分置于两支试管中,向一份中加入NaOH溶液,出现白色沉淀A,另一份通入少量Cl2 , 产生白色沉淀B,试回答下列问题:
(1)若不考虑SO2与水的反应向BaCl2溶液中通入SO2无明显现象,“无明显现象”可能是“不反应”,也可能是“反应但无现象”.此处应为 , 原因是 .
(2)沉淀A的化学式为 , 该沉淀能否溶于稀盐酸? .
(3)写出生成沉淀B的离子方程式: .
(4)生成2.33 g沉淀B,需消耗标准状况下的Cl2mL. -
科目: 来源: 题型:
查看答案和解析>>【题目】298K时,合成氨反应的热化学方程式为:N2(g)+3H2(g)
 2NH3(g);△H=﹣92.4kJ/mol,在该温度下,取1mol N2和3mol H2放在密闭容器内反应.下列说法正确的是( )
2NH3(g);△H=﹣92.4kJ/mol,在该温度下,取1mol N2和3mol H2放在密闭容器内反应.下列说法正确的是( )A. 在有催化剂存在的条件下,反应放出的热量为92.4 kJ
B. 有无催化剂该反应放出的热量都为92.4 kJ
C. 若再充入1 mol H2,到达平衡时放出的热量应为92.4 kJ
D. 反应放出的热量始终小于92.4 kJ
-
科目: 来源: 题型:
查看答案和解析>>【题目】在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)
 C(g)+D(g)已达到平衡状态
C(g)+D(g)已达到平衡状态①混合气体的压强 ②混合气体的密度 ③ B的物质的量浓度 ④ 混合气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值 ⑦混合气体的总质量 ⑧混合气体的总体积 ⑨C、D的分子数之比为1∶1
A. ①②③④⑤⑥⑦⑧ B. ①③④⑤ C. ①②③④⑤⑦ D. ①③④⑤⑧⑨
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图及描述,回答下列问题:
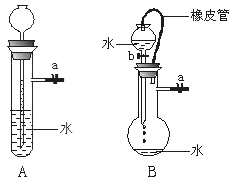
(1)关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示.试判断:A装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) , 判断理由: .
(2)关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶.试判断:B装置是否漏气?(填“漏气”、“不漏气”或“无法确定”) , 判断理由: .
相关试题

