
【题目】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。
(1)X、Y、Z、W、R均是1-18号元素,原子序数依次增大。X是所有元素中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R电子层数相同,R与Y最外层电子数相同,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相同。请回答下列问题:
①W的原子结构示意图__,R离子的电子式__。
②X与Y元素可形成一种常用的消毒剂,其结构式为_。
③Y、Z、W、R形成的简单离子半径由大到小顺序为__(用化学符号表示)。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置__。
②关于铷的下列说法中正确的是__(填序号)。
a.与水反应比钠更剧烈
b.在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的还原性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
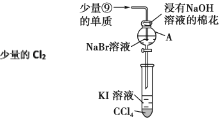
①棉花中浸有NaOH溶液的作用是__(用离子方程式表示)
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到__;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是__。
【答案】
![]() H-O-O-H S2->O2->Na+>Al3+ 第五周期IA族 abcd Cl2+2OH-=H2O+Cl-+ClO- 出现分层,上层几乎呈无色,下层呈紫红色 过量的Cl2也会氧化I-生成I2
H-O-O-H S2->O2->Na+>Al3+ 第五周期IA族 abcd Cl2+2OH-=H2O+Cl-+ClO- 出现分层,上层几乎呈无色,下层呈紫红色 过量的Cl2也会氧化I-生成I2
【解析】
X、Y、Z、W、R均是1-18号元素,原子序数依次增大。X是所有元素中原子半径最小的元素,X为H元素,Y原子最外层电子数是次外层电子数的3倍,Y为O元素,Z、W、R电子层数相同,R与Y最外层电子数相同,R为S元素,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相同,Z为Na元素、W为Al元素。
(1)①W为Al,Al的原子序数为13,其原子结构示意图为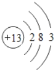 ;R为S,硫离子带有2个负电荷,其电子式为
;R为S,硫离子带有2个负电荷,其电子式为![]() ;
;
②H、O形成的双氧水具有强氧化性,能够杀菌消毒,双氧水为共价化合物,其结构式为H-O-O-H;
③Y、Z、W、R形成的简单离子分别为O2-、Na+、Al3+、S2-,电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,则离子半径:S2->O2->Na+>Al3+;
(2)①铷是37号元素,原子结构中有5个电子层,最外层电子数为1,则位于第五周期第IA族;
②a.铷排在钠的下方,活泼性强于铷,铷与水反应比钠更剧烈,故a正确;
b.依据氧化钠性质可知,氧化铷为碱性氧化物,在空气中易吸收水生成氢氧化铷和与二氧化碳反应生成碳酸铷,故b正确;
c.依据过氧化钠与水反应生成氢氧化钠和氧气,可知:Rb2O2与水能剧烈反应并释放出O2,故c正确;
d.铷金属性强于钠,所以单质铷有极强的还原性,故d正确;
e.铷金属性强于钠,所以RbOH的碱性比同浓度的NaOH强,故e错误;
综上所述答案为abcd;
(3)①棉花中浸有的NaOH溶液可吸收氯气,防止氯气扩散到空气中,发生的离子反应为Cl2+2OH-=Cl-+ClO-+H2O;
②溴与KI反应生成碘,碘易溶于四氯化碳,充分振荡、静置,可观察到溶液分层,上层几乎无色,下层呈紫红色;由于过量的Cl2也会氧化I-生成I2,所以要控制氯气的加入量。


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】立方烷(C8H8)外观为有光泽的晶体。其八个碳原子对称地排列在立方体的八个角上。以下相关说法错误的是
A. 立方烷在空气中可燃,燃烧有黑烟产生
B. 立方烷一氧代物1种、二氯代物有3种、三氯代物也有3种
C. 立方烷是苯(C6H6)的同系物、也是苯乙烯(C6H5-CH=CH2)的同分异构体
D. 八硝基立方烷完全分解可能只产生二氧化碳和氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】花椒毒素(Ⅰ)是白芷等中草药的药效成分,也可用多酚A为原料制备,合成路线如下:

回答下列问题:
(1)①的反应类型为_____________________;B分子中最多有_________个原子共平面。
(2)C中含氧官能团的名称为______________________;③的“条件a”为____________________。
(3)④为加成反应,化学方程式为__________________________________。
(4)⑤的化学方程式为__________________________________。
(5)芳香化合物J是D的同分异构体,符合下列条件的J的结构共有_________种,其中核磁共振氢谱为五组峰的J的结构简式为_________________。(只写一种即可)。
①苯环上只有3个取代基;②可与NaHCO3反应放出CO2;③1mol J可中和3mol NaOH。
(6)参照题图信息,写出以 为原料制备
为原料制备 的合成路线(无机试剂任选) :______________
的合成路线(无机试剂任选) :______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)电动汽车上用的铅蓄电池是以一组充满海绵状态铜的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解液。放电时总反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
①写出放电时负极的电极反应式:__。
②铅蓄电池放电时,溶液的pH将_(填增大、减小或不变);当外电路上有0.5mol电子通过时,溶液中消耗H2SO4的物质的量为__。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。其正极反应方程式为___;若将负极材料改为CH4,写出其负极反应方程式__。

(3)法国格勒诺布尔(Grenoble)约瑟夫﹒傅立叶大学的研究小组发明了第一块可植入人体为人造器官提供电能的葡萄糖生物燃料电池,其基本原理是葡萄糖和氧气在人体中酶(蛋白质)的作用下发生反应:C6H12O6+6O2![]() 6CO2+6H2O(酸性环境)。下列有关该电池的说法正确的是__。
6CO2+6H2O(酸性环境)。下列有关该电池的说法正确的是__。
A.该生物燃料电池不能在高温下工作
B.该电池负极的电极反应式为:C6H12O6+6H2O-24e-=6CO2↑+24H+
C.消耗1mol氧气时转移4mol电子,H+向负极移动
D.提高葡萄糖生物燃料电池的效率,可使其在将来为更多可植入医疗设备提供电能
(4)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂—碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中___作正极,负极的电极反应为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )

A. Mg 电极是该电池的正极
B. H2O2在石墨电极上发生氧化反应
C. 石墨电极附近溶液的pH 增大
D. 溶液中Cl-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在体积为10L的密闭容器中,3molX和1molY进行反应:2X(g)+Y(g)![]() Z(g),经2min达到平衡,生成0.6mol Z,下列说法正确的是( )
Z(g),经2min达到平衡,生成0.6mol Z,下列说法正确的是( )
A.以X浓度变化表示的反应速率为0.01 mol/(L·s)
B.将容器体积变为20L,Z的平衡浓度为原来的![]()
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某晶体的晶胞结构为正三棱柱(如图所示),这种晶体中A、B、C三种微粒数目之比为( )

A. 1∶4∶2 B. 3∶9∶4
C. 2∶9∶4 D. 3∶8∶4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com