【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)单质铜及镍都是由________键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1958 kJ/mol、INi=1753 kJ/mol,ICu>INi的原因是_____________________。
(2)某镍白铜合金的立方晶胞结构如图所示。
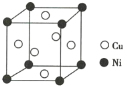
①晶胞中铜原子与镍原子的数量比为________。
②合金的密度为d g/cm3,晶胞参数a=________nm。
【答案】金属 铜失去的是全充满的3d10电子,镍失去的是4s1电子 3:1 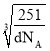 ×107
×107
【解析】
(1)单质铜及镍都是由金属键形成的晶体,Cu、Ni失去一个电子后形成的Cu+、Ni+电子排布式分别为[Ar]3d10、[Ar]3d84s1,Cu+的3d轨道全充满,达到稳定状态,所以Cu的第二电离能相对较大;
(2)①Cu原子位于面心,Cu原子个数为6×![]() =3,Ni原子位于晶胞的顶点,Ni原子个数为8×
=3,Ni原子位于晶胞的顶点,Ni原子个数为8×![]() =1,故镍白铜合金中Cu与Ni的数量比为3:1;
=1,故镍白铜合金中Cu与Ni的数量比为3:1;
②合金中含有3个Cu,1个Ni,晶胞密度为d g/cm3,则![]() =d·(a×10-7cm)3,解得a=
=d·(a×10-7cm)3,解得a=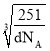 ×107 nm。
×107 nm。

