
【题目】短周期W、X、Y、Z、Q五种元素的原子序数依次递增,W和Z位于同一主族。已知W的氢化物可与Q单质在光照条件下反应生成多种化合物,且Y、Q形成一种共价化合物,X的最高价氧化物对应的水化物可与Y单质反应产生常见的还原性气体单质E。下列说法正确的是
A.X、Y、Q对应简单离子的半径逐渐减小
B.工业上可用电解X、Q元素组成的化合物的饱和溶液制备Q单质
C.Y、Q形成的化合物是非电解质
D.工业用W与Z的最高价氧化物反应制取Z单质,同时得到W的最高价氧化物
【答案】B
【解析】
短周期W、X、Y、Z、Q五种元素的原子序数依次递增,已知W的氢化物可与Q单质在光照条件下反应生成多种化合物,W的氢化物应该为烃,则W为C元素,Q为Cl元素;W和Z位于同一主族,则Z为Si元素;Y、Q形成一种共价化合物,X的最高价氧化物对应的水化物可与Y单质反应产生常见的还原性气体单质E。则X是Na,Y为Al元素;气体单质E为H2,据此解答。
根据上述分析可知:W为C,X是Na,Y是Al,Z是Si,Q是Cl元素。
A. X是Na,Y是Al,二者形成的阳离子核外电子排布是2、8,具有2个电子层;Q是Cl,形成的离子核外电子排布是2、8、8,离子核外电子层数越多,离子半径越大;当离子核外电子层数相同时,离子的核电荷数越大,离子半径越小,所以离子半径大小关系为:Q>X>Y,A错误;
B. Cl2在工业上可用电解饱和NaCl溶液的方法制取,反应方程式为:2NaCl+2H2O![]() Cl2↑+H2↑+2NaOH,B正确;
Cl2↑+H2↑+2NaOH,B正确;
C. Y、Q形成的化合物AlCl3是盐,属于共价化合物,在水溶液中完全电离产生Al3+、Cl-,因此属于电解质,C错误;
D. C与SiO2在高温下发生置换反应产生Si单质,同时得到CO气体,反应方程式为2C+SiO2 ![]() Si+2CO↑,CO不是C元素的最高价氧化物,D错误;
Si+2CO↑,CO不是C元素的最高价氧化物,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是( )
A.硅胶、生石灰、氯化钙等都是食品包装袋中常用的干燥剂
B.厕所清洁剂、食用醋、肥皂水、厨房清洁剂四种溶液的pH逐渐增大
C.酒精能使蛋白质变性,预防新冠肺炎病毒使用的酒精纯度越高越好
D.使用氯气对自来水消毒时,氯气会与自来水中的有机物反应,生成的有机氯化物可能对人有害
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼及其合金在冶金、环保和航天等方面有着广泛的应用。
(1)Mo可被发烟硝酸及氢氟酸氧化为MoO2F2和MoOF4(少量),硝酸本身被还原为NO2,则该反应中氧化剂与还原剂的物质的量之比为_________。
(2)已知:2Mo(s)+3O2(g)=2MoO3(s) △H1;
2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g) △H2;
MoS2(s)+2 O2(g)=Mo(s)+2SO2(g) △H3
则△H3=_________(用含△H1、△H2的代数式表示)
(3)电氧化法提纯钼的原理:将辉钼矿(MoS2)放入装有食盐水的电解槽中,用惰性电极电解,MoS2被氧化为MoO42-和SO42-
①辉钼矿应放入电解槽的_________(填“阴极区”或“阳极区”)。
②阴极的电极反应式为___________________________。
(4)碳酸钠作固硫剂并用氢还原辉钼矿的原理为MoS2(s)+4H2(g)+2Na2CO3(s) ![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H,实验测得平衡时的有关变化曲线如图所示。
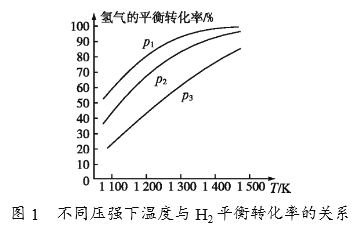
①由图1可知,该反应△H______(填“>”或“<”)0,p1、p2、p3由大到小的顺序为_______________________。
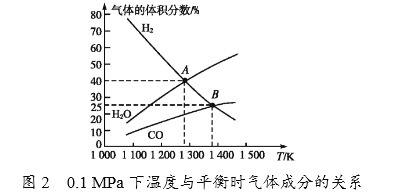
②由图2可知,A点时H2的平衡转化率为____________。
③B点对应的平衡常数K=__________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(MPa)2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯的结构简式可用![]() 来表示,下列关于苯的叙述中正确的是
来表示,下列关于苯的叙述中正确的是
A. 苯主要是以石油为原料而获得的一种重要化工原料
B. 苯中含有碳碳双键,所以苯属于烯烃
C. 苯分子中6个碳碳化学键完全相同
D. 苯可以与溴水、高锰酸钾溶液反应而使它们褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校同学设计实验以MgCl2卤液(主要含MgCl2) 为原料制取活性MgO。回答下列问题:
(1)甲组设计下列装置制取氨气和二氧化碳。
①用生石灰和浓氨水制取NH3可选用的装置是_______(填“A”“B”或“AB”)。
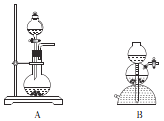
②若用石灰石和稀盐酸制取CO2,反应的离子方程式为_________________________。
(2)乙组利用甲组制备的NH3和CO2制取3MgCO3·Mg(OH)2·3H2O。
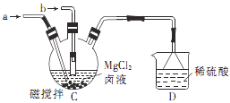
①接口b处通入的气体是_________________(填化学式)。
②装置D的作用是______________________________________。
③生成3MgCO3·Mg(OH)2·3H2O的化学方程式为____________________。
(3)丙组灼烧3MgCO3·Mg(OH)2·3H2O制活性MgO时,所需的硅酸盐质仪器除酒精灯和坩埚外,还需要______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香兰素是重要的香料之一,它可由丁香酚经多步反应合成。
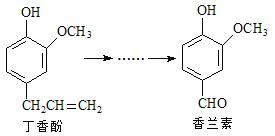
有关上述两种化合物的说法正确的是
A. 常温下,1mol丁香酚只能与1molBr2反应
B. 丁香酚不能使FeCl3溶液发生显色反应
C. 1mol香兰素最多能与3mol氢气发生加成反应
D. 香兰素分子中至少有12个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1)。
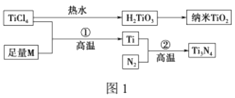
图中的M是短周期金属元素,M的部分电离能如表:
I1 | I2 | I3 | I4 | I5 | |
电离能/(kJ/mol) | 738 | 1451 | 7733 | 10540 | 13630 |
请回答下列问题:
(1)Ti的基态原子外围电子排布式为________________。
(2)M是________(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为____。
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示。化合物甲的分子中采取sp2方式杂化的碳原子有________个,化合物乙中采取sp3方式杂化的原子3对应的元素的电负性由大到小的顺序为________________。
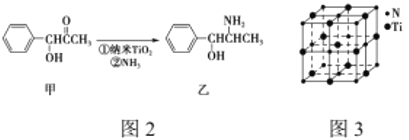
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为________________g/cm3 (NA为阿伏加德罗常数的值,只列计算式)。该晶体中与氮原子距离相等且最近的氮原子有________个。
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据:
离子晶体 | NaCl | KCl | CaO |
晶格能/(kJ/mol) | 786 | 715 | 3401 |
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰电池比普通的锌锰干电池性能优越,能提供较大的电流并连续放电,其构造如图所示。电池反应方程式为 2MnO2+Zn+2H2O=2MnO (OH)+Zn (OH)2。下列说法不正确的是
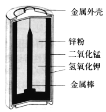
A.电池使用过程中,电解质的碱性增强
B.锌粉是该电池的负极
C.MnO2 电极的电极反应式:MnO2+eˉ+H2O=MnO(OH)+OHˉ
D.当电池使用时,OHˉ移向电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是目前最有效工业固氮的方法,解决数亿人口生存问题。回答下列问题:
(1)科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。

由图可知合成氨反应![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g)的H=___ kJ·mol-1。该历程中反应速率最慢的步骤的化学方程式为___。
NH3(g)的H=___ kJ·mol-1。该历程中反应速率最慢的步骤的化学方程式为___。
(2)工业合成氨反应为:N2(g)+3H2(g)![]() 2NH3(g),当进料体积比V(N2):V(H2)=1:3时平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
2NH3(g),当进料体积比V(N2):V(H2)=1:3时平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:

①500℃时,反应平衡常数Kp(30MPa)___ Kp(100MPa)。(填“<”、“=”、“>”)
②500℃、30MPa时,氢气的平衡转化率为___(保留2位有效数字),Kp=___(MPa)-2(列出计算式)。
(3)科学家利用电解法在常温常压下实现合成氨,工作时阴极区的微观示意如图,其中电解液为溶解有三氟甲磺酸锂和乙醇的惰性有机溶剂。

①阴极区生成NH3的电极方程式为___。
②下列说法正确的是___(填标号)。
A.三氟甲磺酸锂的作用是增强导电性
B.该装置用金(Au)作催化剂目的是降低N2的键能
C.选择性透过膜可允许N2和NH3通过,防止H2O进入装置
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com