【题目】如图所示,常温下通电5 ![]() 后,发现铜电极的质量增加,试回答:
后,发现铜电极的质量增加,试回答:

(1)电源电极![]() 的名称为________(填“正极”或“负极”)。
的名称为________(填“正极”或“负极”)。
(2)电解池![]() 中阳极的电极反应式是____________。
中阳极的电极反应式是____________。
(3)若![]() 溶液的体积是200
溶液的体积是200 ![]() ,则当铜电极的质量增加2. 16
,则当铜电极的质量增加2. 16 ![]() 时
时![]() 中溶液的
中溶液的![]() ____________ (忽略电解前后溶液体积的变化),若要使电解后的溶液恢复到与电解前完全相同的状态,则应加入____________(填物质的种类及数量)。
____________ (忽略电解前后溶液体积的变化),若要使电解后的溶液恢复到与电解前完全相同的状态,则应加入____________(填物质的种类及数量)。
(4)已知电解前,电解池B中铜银两电极的质量相等,通电一段时间后,当铜银两电极的质量差为2.16 ![]() 时,电解池A中生成的气体最多为________
时,电解池A中生成的气体最多为________![]() 。
。
参考答案:
【答案】 负极 ![]()
![]()
![]() 13 0.02
13 0.02 ![]()
![]() 0.01
0.01
【解析】(1)通电5 ![]() 后,Cu电极质量增加,是因为Ag+在阴极上放电而析出,即Cu电极是阴极,则Ag电极为阳极,所以电源电极X是负极,电极Y是正极;
后,Cu电极质量增加,是因为Ag+在阴极上放电而析出,即Cu电极是阴极,则Ag电极为阳极,所以电源电极X是负极,电极Y是正极;
(2)Ag电极为电解池B的阳极,电极反应式为Ag-e-=Ag+;
(3)当铜电极的质量增加2. 16g时,即析出n(Ag)=0.02mol,则转移电子n(e-)=0.02mol,根据电子转移守恒可得,在电解池A中,左边阴极析出氢气n(H2)=0.01mol,右边阳极析出氯气n(Cl2)= 0.01mol,而溶液中将增加n(OH-)=0.02mol,所以c(OH-)= 0.02mol/0.2L =0.1mol/L,pH=13,所以要使电解后的溶液恢复到与电解前完全相同的状态,则需要通入0.02mol的HCl气体;
(4)通电前,电解池B的铜、银两电极质量相等,设为mg,设通电过程中转移电子xmol,则Cu电极质量增加,是因为析出了108xg的Ag,而Ag电极质量减小,是因为溶解掉108xg的Ag,当铜银两电极的质量差为2.16g时,即(m+108x)g-(m-108x)g=2.16g,x= n(e-) =0.01mol,则电解池A中产生n(H2)=0.005mol,产生n(Cl2)=0.005mol,所以产生气体最多为0.01mol。
-
科目: 来源: 题型:
查看答案和解析>>【题目】有一无色溶液,可能含有Fe3+、K+、Al3+、Mg2+、NH
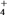 、Cl-、SO
、Cl-、SO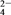 、HCO
、HCO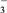 、MnO
、MnO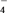 中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量的Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是( )
中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量的Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是( )A. 肯定有Al3+、Mg2+、NH
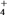 、Cl- B. 肯定有Al3+、Mg2+、HCO
、Cl- B. 肯定有Al3+、Mg2+、HCO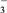
C. 肯定有K+、HCO
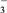 、MnO
、MnO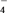 D. 肯定有Al3+、Mg2+、SO
D. 肯定有Al3+、Mg2+、SO
-
科目: 来源: 题型:
查看答案和解析>>【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_______(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是_______;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是_______。
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是_______。在分液操作中,应充分振荡,然后静置,待分层后______(填标号),以下略。
A.直接将含碘苯溶液从分液漏斗上口倒出
B.直接将含碘苯溶液从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将含碘苯溶液从下口放出
D.先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关组成细胞化合物的说法,不正确的是
A. 蛋白质水解的终产物是氨基酸 B. 组成淀粉的基本单位是葡萄糖
C. RNA的单体是脱氧核糖核苷酸 D. 核酸是由许多核苷酸分子连接而成的
-
科目: 来源: 题型:
查看答案和解析>>【题目】占细胞干重最多的化学元素是( )
A. C B. H C. O D. N
-
科目: 来源: 题型:
查看答案和解析>>【题目】用干燥洁净的铂丝蘸取某试样灼烧时,焰色反应为黄色,下列判断正确的是( )
A.该试样一定是钠的化合物B.该试样一定含有钠元素
C.该试样一定是金属钠D.不能确定该试样中是否含有钠元素
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列排列顺序正确的是( )
A.热稳定性:H2O>HF>H2SB.非金属性:Cl>S>Si
C.最高正化合价:F>N>CD.酸性:H2CO3>H3PO4>H2SO4
相关试题

