
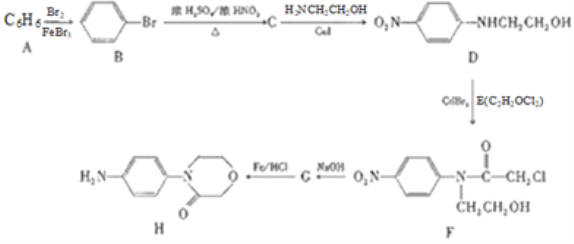
【题目】H是合成预防静脉血栓形成(![]() )的原料药利伐沙班中间体,其合成路线如图:
)的原料药利伐沙班中间体,其合成路线如图:
已知: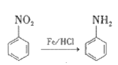
(1)A的化学名称为_________________,C中含有官能团的名称为__________________。
(2)C→D的反应类型为__________________。
(3)G的结构简式为______________________。
(4)D→F的化学方程式为__________________________________________________。
(5)满足下列条件的D的同分异构体有_______________种(不考虑立体异构),其中核磁共振氢谱有6组峰且峰面积之比为4:2:1:1:1:1的结构简式为____________________(写一种)。
①苯环上有3个取代基;②两个氨基直接和苯环相连;③可以和![]() 溶液反应;④
溶液反应;④![]() 该物质与足量钠反应产生
该物质与足量钠反应产生![]() ;
;
(6)已知:![]() ,以C为原料合成
,以C为原料合成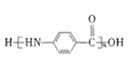 的合成路线为____________________________________________(其他试剂任选)。
的合成路线为____________________________________________(其他试剂任选)。
【答案】苯 溴原子、硝基 取代反应 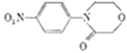
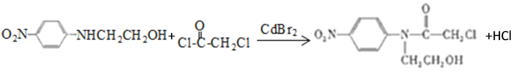 6
6 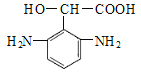 、
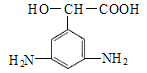
、
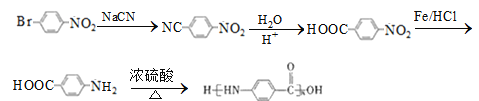
【解析】
由流程图可知,A为苯 ![]() ,在溴化铁的催化作用下苯与液溴发生取代反应生成B溴苯,在浓硫酸的作用下溴苯与浓硝酸发生硝化反应生成C,由D的结构简式可知,C的结构简式为
,在溴化铁的催化作用下苯与液溴发生取代反应生成B溴苯,在浓硫酸的作用下溴苯与浓硝酸发生硝化反应生成C,由D的结构简式可知,C的结构简式为![]() ,C与H2NCH2CH2OH发生取代反应生成D,D与E发生取代反应生成F,由D与F的结构简式、结合E的分子式可知,E的结构简式为
,C与H2NCH2CH2OH发生取代反应生成D,D与E发生取代反应生成F,由D与F的结构简式、结合E的分子式可知,E的结构简式为![]() ,根据已知信息反应知,G发生还原反应生成H,则G为
,根据已知信息反应知,G发生还原反应生成H,则G为 ,F在NaOH存在下反应生成G,据此分析解答。
,F在NaOH存在下反应生成G,据此分析解答。
(1)A的化学名称为苯,C为![]() ,含有官能团的名称为溴原子、硝基;
,含有官能团的名称为溴原子、硝基;
(2)C为![]() ,C与H2NCH2CH2OH反应时,-NHCH2CH2OH取代了C中的溴原子生成D,故C与H2NCH2CH2OH发生取代反应生成D;
,C与H2NCH2CH2OH反应时,-NHCH2CH2OH取代了C中的溴原子生成D,故C与H2NCH2CH2OH发生取代反应生成D;
(3)G的结构简式为 ;
;
(4)D与E发生取代反应生成F,故D→F的化学方程式为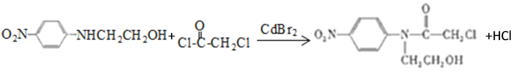 ;
;
(5)满足下列条件的D的同分异构体,①苯环上有3个取代基;②两个氨基直接和苯环相连;③可以和![]() 溶液反应,说明有一个羧基;④
溶液反应,说明有一个羧基;④![]() 该物质与足量钠反应产生
该物质与足量钠反应产生![]() ,说明还有一个羟基,则另一个取代基为
,说明还有一个羟基,则另一个取代基为![]() ;当两个氨基位于邻位时,
;当两个氨基位于邻位时,![]() 有2种取代方式;当两个氨基位于对位时,
有2种取代方式;当两个氨基位于对位时,![]() 有1种取代方式;当两个氨基位于间位时,
有1种取代方式;当两个氨基位于间位时,![]() 有3种取代方式,则符合条件的同分异构体共6种;其中核磁共振氢谱有6组峰且峰面积比为4:2:1:1:1:1的结构简式为
有3种取代方式,则符合条件的同分异构体共6种;其中核磁共振氢谱有6组峰且峰面积比为4:2:1:1:1:1的结构简式为 、
、 ;
;
(6)根据已知信息反应可知,![]() 与NaCN反应生成
与NaCN反应生成![]() ,
,![]() 在酸性条件下反应生成
在酸性条件下反应生成![]() ,
,![]() 发生还原反应生成
发生还原反应生成![]() ,
,![]() 再发生缩聚反应生成
再发生缩聚反应生成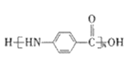 ,故合成路线为:
,故合成路线为: 。
。


科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。某同学以含铜废料(主要成分是 CuO、MgO、MnO、SiO2及少量的杂质)为主要原料制备CuCl的主要流程如下:
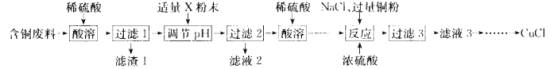
已知:①CuCl难溶于水和乙醇 ,在潮湿的空气中易被氧化;
②在水溶液中存在平衡 :CuCl(白色)+2Cl-![]() [CuCl3]2-(色无溶液)。
[CuCl3]2-(色无溶液)。
③几种金属氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物 | 开始沉淀的 pH | 完全沉淀的 pH |
Mg(OH)2 | 8. 4 | 10. 8 |
Cu(OH)2 | 4.2 | 6. 7 |
Mn(OH)2 | 7. 8 | 8. 8 |
问答下列问题:
(1)滤渣1 的主要成分是 _________________(写化学式,下同)。
(2)“调pH”所用粉末状试剂 X 是_____________;pH的调节范闱为____________。
(3)“反应”发生 Cu2+ +Cu+6Cl-=2[CuCl3]2-,表明已完全反应的现象是_______________。
(4)向“滤液3” 加大量的水,过滤可得 CuCl。所得沉淀需再用乙醇洗涤.并在低温下干燥,其原因是___________。
(5)产品纯度的测定,步骤如下:称取mg试样置于锥形瓶中,加入直径 4 ~ 5 mm 玻璃珠适量,并加入 10 mL FeCl3溶液,摇动至样品全部溶解后(CuCl+FeCl3=CuCl2+FeCl2),再加入50 mL,水和2滴邻菲罗啉指示剂,立刻用c mol L-1 的硫酸高铈[Ce(SO4)2]标准溶液滴定(Fe2++Ce4+=Fe3++Ce3+)'滴至终点时共消耗硫酸高铈标准溶液V mL。
①锥形瓶中加入玻璃珠的作用是____________________。
②样品中 CuCl 的质量分数为_____(列出表达式即可 , 用含(c、m、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PMMA骨水泥的成分为聚甲基丙烯酸甲酯,结构简式为 ,其单体丙的制备原理如图所示,下列说法中错误的是
,其单体丙的制备原理如图所示,下列说法中错误的是

A.丙所含的官能团有碳碳双键、酯基
B.可以用饱和碳酸氢钠溶液鉴别甲、乙、丙
C.丙与聚甲基丙烯酸甲酯互为同系物
D.甲+乙→丙的反应类型为取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、M均为短周期主族元素,X与W、M形成的化合物XW2、XM4均为重要的溶剂,25℃时,浓度均为0.1moL·L-1的上述元素的最高价氧化物对应的水化物溶液的pH随原子序数的变化如图所示.
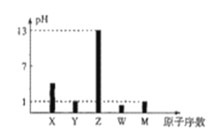
回答下列问题:
(1)M在元素周期表中的位置为___________________.
(2)W可与Z形成化合物Z2W2,写出该物质的电子式:___________________________.
(3)写出一个能说明W与M非金属性强弱的离子方程式:__________________________.
(4)Z的单质可以与X的最高价氧化物反应生成一种盐和黑色固体单质,若每转移1mol电子,恢复至室温时该反应放出QkJ热量,写出该反应的热化学方程式:________________________________________.
(5)M的单质为有毒气体,且在工业上用途广泛,常用Y的简单氢化物检验其运输管道是否漏气,漏气时的现象为产生白烟,该反应中氧化剂与还原剂的物质的量之比为___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是__________(填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________。
(4
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________(填物质化学式);呈两性的氢氧化物是_________(填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予了锂离子电池领域做出巨大贡献的三位科学家。某锂离子电池![]() 为负极,
为负极,![]() 为正极,锂盐有机溶液作电解质溶液,电池反应为
为正极,锂盐有机溶液作电解质溶液,电池反应为![]() 则下列有关说法正确的是
则下列有关说法正确的是
A.金属锂的密度、熔点和硬度均比同族的碱金属低
B.该锂离子电池可用乙醇作有机溶剂
C.电池放电时,Li+从正极流向负极
D.电池充电时,阳极的电极反应式为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com