【题目】二氧化锰是化学工业中常用的氧化剂和催化剂。我国主要以贫菱锰矿(有效成分为![]() )为原料,通过热解法进行生产。
)为原料,通过热解法进行生产。
(1)碳酸锰热解制二氧化锰分两步进行:
i.![]()
ii. ![]()
①反应i的化学平衡常数表达式![]() ___________。
___________。
②焙烧![]() 制取
制取![]() 的热化学方程式是_________________。
的热化学方程式是_________________。
(2)焙烧(装置如图1)时持续通入空气,并不断抽气的目的是________________。
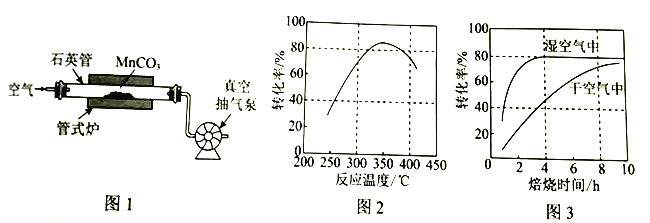
(3)在其他条件不变时,某科研团队对影响![]() 转化率的生产条件进行了研究,结果如图2、图3所示。
转化率的生产条件进行了研究,结果如图2、图3所示。
①图2是在常压(![]() )下的研究结果,请在图2中用虚线画出
)下的研究结果,请在图2中用虚线画出![]() 下
下![]() 转化率与反应温度的关系图______。
转化率与反应温度的关系图______。
②常压下,要提高![]() 的转化率,应选择的生产条件是____________焙烧
的转化率,应选择的生产条件是____________焙烧![]() 。
。
③图3中,焙烧![]() 时,
时,![]() 的转化率:干空气<湿空气,原因是______________。
的转化率:干空气<湿空气,原因是______________。
【答案】![]()
![]() 保持
保持![]() 的浓度,降低
的浓度,降低![]() 的浓度,使平衡正向移动,提高碳酸锰的转化率
的浓度,使平衡正向移动,提高碳酸锰的转化率 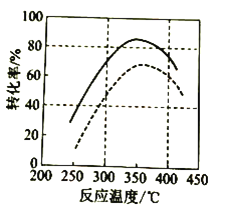 湿空气中,
湿空气中,![]() 左右 干空气中没有催化剂,反应速率比湿空气中慢,
左右 干空气中没有催化剂,反应速率比湿空气中慢,![]() 时未达到平衡。
时未达到平衡。
【解析】
(1)考查平衡常数表达式以及盖斯定律;
(2)焙烧时持续通入空气,并不断抽气的目的可以从![]() 的平衡正向移动入手;
的平衡正向移动入手;
(3)增压![]() 平衡逆向移动。未达到平衡的某个时间点物质的转化率大小比较可以从反应速率入手。
平衡逆向移动。未达到平衡的某个时间点物质的转化率大小比较可以从反应速率入手。
(1)①固体不写进平衡常数表达式,故K=![]() ;
;
②热化学方程式i扩大倍数2,再加上方程式ii,可得到焙烧![]() 制取
制取![]() 的热化学方程式
的热化学方程式![]() ;
;
(2)焙烧时持续通入空气,并不断抽气分离出CO2,![]() 的平衡会正向移动,故答案为:保持
的平衡会正向移动,故答案为:保持![]() 的浓度,降低
的浓度,降低![]() 的浓度,使平衡正向移动,提高碳酸锰的转化率;
的浓度,使平衡正向移动,提高碳酸锰的转化率;
(3)①增压![]() 平衡逆向移动,相同温度条件下物质转化率降低,则作图为:
平衡逆向移动,相同温度条件下物质转化率降低,则作图为:
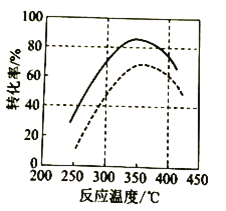 ;
;
②结合图2和图3,湿空气中,![]() 左右,焙烧
左右,焙烧![]() 的转化率较高;
的转化率较高;
③8h时干空气中未达到平衡,物质的转化率大小可以通过比较反应速率得到,故答案为:干空气中没有催化剂,反应速率比湿空气中慢,![]() 时未达到平衡。
时未达到平衡。

