【题目】下列图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色试验均为黄色。
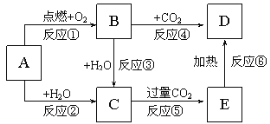
回答下列问题:
(1)写出化学式:A___,D___。
(2)以上反应中不属于氧化还原反应的有___(填序号)。
(3)反应③的离子方程式:___。氧化剂为___;氧化产物为___。
(4)向D溶液中通入CO2反应的化学方程式:____。
【答案】Na Na2CO3 ⑤⑥ 2Na2O2+2H2O=4Na++4OH-+O2↑ Na2O2 O2 Na2CO3+H2O+CO2=2NaHCO3
【解析】
焰色反应为黄色的是钠元素,则A是金属钠,钠在氧气中燃烧生成过氧化钠,过氧化钠与二氧化碳反应生成碳酸钠和氧气,过氧化钠与水反应生成氢氧化钠和氧气,金属钠与水发生置换反应生成氢氧化钠和氢气,氢氧化钠溶液吸收足量的二氧化碳可生成碳酸氢钠,碳酸氢钠热稳定性较差,受热分解转化为碳酸钠。所以,A是钠,B是过氧化钠,C是氢氧化钠,D是碳酸钠,E是碳酸氢钠。以此进行分析解答。
(1)根据以上分析,A为Na,D为Na2CO3,
答案为:Na;Na2CO3;
(2)上述6个反应中①、②、③、④或有单质参加反应,或有单质生成,反应中有元素化合价的变化,这四个反应属于氧化还原反应,则⑤ ⑥两个反应中没有元素化合价的变化,不属于氧化还原反应,
答案为:⑤⑥;
(3)反应③为过氧化钠和水反应生成氢氧化钠和氧气,离子方程式:2Na2O2+2H2O=4Na++4OH-+O2↑;该反应中Na2O2既做氧化剂又做还原剂,氧化产物为氧气。
答案为:2Na2O2+2H2O=4Na++4OH-+O2↑;Na2O2;O2;
(4)向碳酸钠溶液中通入CO2生成碳酸氢钠,反应的化学方程式:Na2CO3+H2O+CO2=2NaHCO3,
答案为:Na2CO3+H2O+CO2=2NaHCO3。

