【题目】一定条件下,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是

A. a、b、c、d、e中,c最稳定
B. b→a+c反应的活化能为反应物能量减生成物能量
C. b→a+d反应的热化学方程式为:3ClO-(aq)=ClO3-(aq)+2Cl-(aq)ΔH=+116 kJ·mol-1
D. 一定温度下,Cl2与NaOH溶液反应生成的产物有a、b、d,溶液中a、b、d的浓度之比可能为11∶1∶2
参考答案:
【答案】D
【解析】根据氯元素的化合价,a、b、c、d、e依次代表Cl-、ClO-、ClO2-、ClO3-、ClO4-。A项,物质能量越低越稳定,由图可得a、b、c、d、e中,a最稳定,c最不稳定,故A错误;B项,反应物能量-生成物能量=-ΔH,依据图中数据无法判断b→a+c反应的活化能,故B错误;C项,a为Cl-、b为ClO-、d为ClO3-,B→A+D的化学方程式为3ClO-=ClO3-+2Cl-,结合曲线提供的数据,反应热为:ΔH=64kJmol-1+2×0kJmol-1-3×60kJmol-1=-116kJmol-1,故C错误;D项,氧化还原反应遵循电子守恒,Cl2与NaOH溶液反应生成的产物有a(Cl-)、b(ClO-)、d(ClO3-),氯元素化合价由0价将为-1价、升为+1价和+5价,由电子守恒得:n(Cl-)=n(ClO-)+5n(ClO3-),当溶液中a、b、d的浓度之比为11:1:2时上述电子守恒式成立,故D正确。
-
科目: 来源: 题型:
查看答案和解析>>【题目】新型锂-空气电池具有能量密度高的优点,可以用作新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过。下列说法正确的是
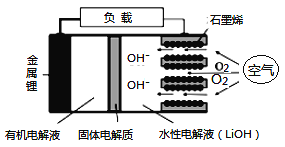
A. Li+穿过固体电解质向正极移动而得到LiOH溶液
B. 放电时,当外电路中有1 mol e-转移时,水性电解液离子总数增加NA
C. 应用该电池电镀铜,阴极质量增加64 g,理论上将消耗11.2 L O2
D. 放电时,负极反应式:Li-e-+OH-=LiOH
-
科目: 来源: 题型:
查看答案和解析>>【题目】有10 g Na2O2、Na2O、Na2CO3、NaOH的混合物与200 g质量分数为3.65%的盐酸恰好反应,蒸干溶液,最终得固体NaCl质量为
A. 11.7 g B. 5.85 g
C. 8 g D. 15.5 g
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列反应吸收热量的是( )
A. 氧化钙与水反应B. 焦炭制水煤气
C. 酸碱中和反应D. 钠与水反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关物质分类的叙述正确的是
A.CaCl2、NaOH、HCl、O2四种物质都属于化合物
B.溶液、浊液、胶体都属于混合物
C.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
D.CO2、CO等非金属氧化物均属于酸性氧化物
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列实验方案能达到目的的是( )
A. 用品红溶液检验SO2
B. 用焰色反应鉴别KNO3和KCl
C. 用澄清石灰水鉴别MgCl2溶液和NaHCO3溶液
D. 用丁达尔效应区分FeCl3溶液和Fe2(SO4)3溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】浓度均为0.1mol/L体积均为Vo的HX、HY溶液,分别加水稀释至体积V,pH随V的变化关系如下图所示。下列叙述不正确的是

A. HX的酸性比HY的弱,且HY是强酸
B. NaX溶液中存在关系:c(X-)+c(HX)=c(Na+)
C. 相同温度下,电离常数K(HX):a=b
D.
 ,若同时微热两种溶液(不考虑HX、HY和H2O的挥发),则
,若同时微热两种溶液(不考虑HX、HY和H2O的挥发),则 减小
减小
相关试题

