【题目】用固体NaOH配制物质的量浓度溶液时,下列操作会导致溶液浓度偏高的是( )
A. 在烧杯中溶解时,有少量液体溅出 B. 样品中含有少量Na2O杂质
C. 容量瓶使用前未干燥 D. 定容时仰视视容量瓶刻度线
参考答案:
【答案】B
【解析】A、有少量液体溅出,造成容量瓶中溶质物质的量减少,所配溶液的浓度偏低,故A错误;B、样品中含有少量Na2O杂质,则Na2O溶于水后生成NaOH使溶质的物质的量偏多,所以会导致溶液中溶质的物质的量浓度偏高,故B正确;C、容量瓶是否干燥,对实验无影响,故C错误;D、定容时,仰视刻度线,所配溶液体积增大,浓度偏低,故D错误。
-
科目: 来源: 题型:
查看答案和解析>>【题目】白磷与氧气可发生如下反应:P4+5O2 = P4O10。已知断裂下列化学键需要吸收的能量分别为:E(P—P) = a kJ·mol-1、E(P—O) = b kJ·mol-1、E(P=O) = c kJ·mol-1、E(O=O) = d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )
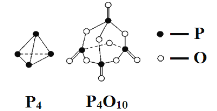
A.-(6a-12b-4c+5d)kJ·mol-1
B.-(-6a+12b+4c-5d)kJ·mol-1
C.-(-4a+6b+4c-5d)kJ·mol-1
D.-(4a-6b-4c+5d)kJ·mol-1
-
科目: 来源: 题型:
查看答案和解析>>【题目】草酸钴用途广泛,可用于指示剂和催化剂制备。一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4·2H2O工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物
Fe(OH)3
Fe(OH)2
Co(OH)2
Al(OH)3
Mn(OH)2
完全沉淀的pH
3.7
9.6
9.2
5.2
9.8
(1)浸出过程中加入Na2SO3的目的是将_____________还原(填离子符号)以便固体溶解。该步反应的离子方程式为 (写一个)。
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,氯元素被还原为最低价。该反应的离子方程式为 。
(3)利用平衡移动原理分析:加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是 。
(4)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液Ⅱ中加入萃取剂的作用是 ;使用萃取剂适宜的pH=____(填序号)左右:
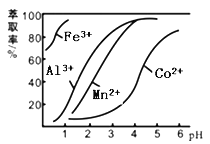
A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)= 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的少量乙烯的操作方法是( )
A.混合气体通过盛水的洗气瓶
B.混合气体通过装有过量溴水的洗气瓶
C.混合气体和过量H2混合
D.混合气体通过酸性KMnO4溶液 -
科目: 来源: 题型:
查看答案和解析>>【题目】I、现有含CaO杂质的CaC2试样。设计以下实验,测定CaC2试样的纯度。(反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑),请从下图中选用适当的装置,完成该实验。
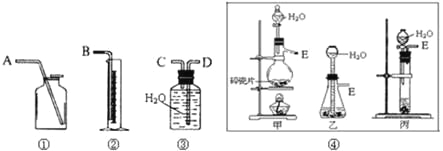
(1)制取C2H2最好选④中的 装置(填“甲”“乙”或“丙”),所选用装置的连接顺序是 (填各接口A~E的顺序)。
(2)若实验时称取的试样为1.4g,产生的乙炔在标准状况下的体积为448mL,此试样中CaC2的质量分数为 。(保留3为有效数字)

II、某同学在实验室从如图标签的试剂瓶中取少许钠进行燃烧实验,实验后 发现还有少许黑色固体生成。从反应物及实验操作猜测:
该黑色物质可能为碳与另一种氧化物组成的混合物。
根据题意和图示回答下面问题:
(1)装置图⑤中A的名称 。
(2)此氧化物可能是 或 (写化学式)。
(3)对黑色固体物质的组成作如图⑥所示研究
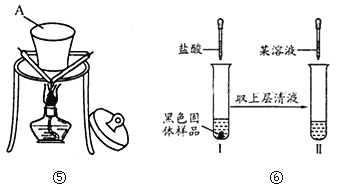
①实验I中加入盐酸溶液的目的是 。
②仅通过实验II,用最简步骤能快速确定黑色氧化物的组成,请完善该设计。(限选试剂:稀盐酸、KSCN溶液、10%H2O2溶液)
实验操作
预期现象与结论
相关离子方程式
取少量实验I中的澄清溶液,加入试剂
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列说法中正确的是
A. 6.8g固体KHSO4与3.9g固体Na2O2中阴离子数目相同
B. 常温下铁、铜均不溶于浓硫酸,说明常温下铁、铜与浓硫酸均不反应
C. 离子化合物中只含离子键
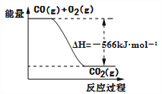
D. 已知:2CO(g)+O2(g)=2CO2(g);ΔH=-566kJ·mol-1,下图可表示由CO生成CO2的反应过程和能量关系
-
科目: 来源: 题型:
查看答案和解析>>【题目】在NaCl、MgCl2、MgSO4形成的混合溶液中,c(Na+)=0.1mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.2mol/L,则c(SO42-)为 ( )
A. 0.15 mol/L B. 0.10 mol/L C. 0.25 mol/L D. 0.20 mol/L
相关试题

