【题目】A、B、C、D、E是中学化学中五种常见元素,有关信息如下:
元素 | 有关信息 |
A | 最高价氧化物对应的水化物与其氢化物反应生成离子化合物 |
B | 地壳中含量最多的元素 |
C | 单质须保存在煤油中 |
D | 单质与NaOH溶液反应可用于生产漂白液 |
E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
请回答下列问题:
(1)A的氢化物分子的电子式是 , 其最高价氧化物对应的水化物与其氢化物反应的离子方程式: .
(2)B,C组成的某种化合物和B的某种氢化物反应可生成B的单质,则B、C组成的该化合物所含有的化学键为 .
(3)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法及现象是: , 证明存在该阳离子.
参考答案:
【答案】
(1)![]() ;NH3+H+=NH4+
;NH3+H+=NH4+
(2)离子键、共价键
(3)取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生)
【解析】解:A元素最高价氧化物对应的水化物与其氢化物反应生成离子化合物,则A为H元素;B是地壳中含量最多的元素,则B为O元素;单质C须保存在煤油中,则C为Na;D的单质与NaOH溶液反应可用于生产漂白液,则D为Cl元素;E的单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏,则E为Fe.(1)A的氢化物分子为NH3 , 电子式是 ![]() ,其最高价氧化物对应的水化物与其氢化物反应的离子方程式:NH3+H+=NH4+ , 所以答案是:
,其最高价氧化物对应的水化物与其氢化物反应的离子方程式:NH3+H+=NH4+ , 所以答案是: ![]() ;NH3+H+=NH4+; (2)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,应是过氧化钠与水反应生成氢氧化钠与仪器,过氧化钠中含有离子键、共价键,
;NH3+H+=NH4+; (2)B、C组成的某种化合物和B的某种氢化物反应可生成B的单质,应是过氧化钠与水反应生成氢氧化钠与仪器,过氧化钠中含有离子键、共价键,
所以答案是:离子键、共价键;(3)A、D的氢化物相互反应,产生白色固体为NH4Cl,该固体中阳离子为NH4+ , 检验方法为:取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生),
所以答案是:取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生).
-
科目: 来源: 题型:
查看答案和解析>>【题目】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和C原子最外层只有一个电子,C燃烧时的焰色反应是黄色,C的单质在高温下与B的单质充分反应可以产生淡黄色固态化合物,A单质与D单质可以发生化合反应,且反应条件可以是点燃或者光照,试根据以上叙述回答:
(1)写出B、D的元素名称:BD .
(2)写出化学方程式:C+B= ,
(3)C元素离子的离子结构示意图
(4)写出A2B、C2B2的电子式、 . -
科目: 来源: 题型:
查看答案和解析>>【题目】天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、CO32-、HCO3-、Br-等离子。火力发电燃煤排放的含有SO2的烟气可利用海水脱硫,其工艺流程如下所示:

下列说法错误的是:
A.含SO2的烟气若不经过海水脱硫直接排放可造成酸性降雨
B.“氧化”是利用氧气将H2SO3、HSO3-、SO32-等氧化生成SO42-
C.“反应、稀释”时加天然海水的目的是中和、稀释经氧化后海水中生成的酸
D.“排放”出来的海水中SO42-的物质的量浓度与进入吸收塔的天然海水相同
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质不能通过常温下的化合反应获取的是
A. NaHCO3 B. H2SiO3 C. FeCl3 D. FeCl2
-
科目: 来源: 题型:
查看答案和解析>>【题目】碘元素在下列物质中以单质存在的是
A. 碘酒 B. 海带 C. 含碘食盐 D. 人工降雨剂
-
科目: 来源: 题型:
查看答案和解析>>【题目】《科学美国人》评出的2016年十大创新技术之一是碳呼吸电池, 电池原理如右图所示,则下列有关说法正确的是
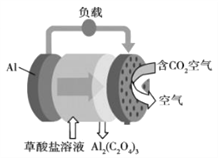
A. 该装置将电能转变为化学能
B. 正极的电极反应为C2O42- -2e-
 2CO2
2CO2 C. 每生成1mol Al2(C2O4)3,有6mol电子流过负载
D. 随着反应进行,草酸盐浓度不断变小
-
科目: 来源: 题型:
查看答案和解析>>【题目】2,3 二甲基丁烷中“二”表示的含义是
A.取代基的数目B.取代基的种类C.主链碳的数目D.主链碳的位置
相关试题

