【题目】水合肼(N2H4·H2O)又名水合联氨,无色透明,是具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂。利用尿素法生产水合肼的原理为:CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl。
实验1:制备NaClO溶液。(已知:3NaClO![]() 2NaCl+NaClO3)
2NaCl+NaClO3)
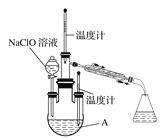
(1)如图装置Ⅰ中烧瓶内发生反应的化学方程式为___________。

(2)用NaOH固体配制溶质质量分数为30%的NaOH溶液时,所需玻璃仪器除量筒外还有__________(填字母)。
a.烧杯 b.容量瓶 c.玻璃棒 d.烧瓶
(3)图中装置Ⅱ中用冰水浴控制温度的目的是__________ 。
实验2:制取水合肼。
(4)图中充分反应后,____________(填操作名称)A中溶液即可得到水合肼的粗产品。若分液漏斗滴液速度过快,部分N2H4·H2O会参与A中反应并产生大量氮气,降低产品产率。写出该过程反应生成氮气的化学方程式 ________。
实验3:测定馏分中水合肼的含量。
(5)称取馏分3.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250 mL溶液,移出25.00 mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.15 mol·L-1的碘的标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。
①滴定时,碘的标准溶液盛放在 ________(填“酸式”或“碱式”)滴定管中。
②下列能导致馏分中水合肼的含量测定结果偏高的是 _________(填字母)。
a.锥形瓶清洗干净后未干燥 b.滴定前,滴定管内无气泡,滴定后有气泡
c.读数时,滴定前平视,滴定后俯视 d.盛标准液的滴定管水洗后,直接装标准液
③实验测得消耗I2溶液的平均值为20.00mL,馏分中水合肼(N2H4·H2O)的质量分数为 _________。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O a c 防止NaClO受热分解,影响水合肼的产率 蒸馏 N2H4·H2O+2NaClO=N2↑+3H2O+2NaCl 酸式 d 25%
MnCl2+Cl2↑+2H2O a c 防止NaClO受热分解,影响水合肼的产率 蒸馏 N2H4·H2O+2NaClO=N2↑+3H2O+2NaCl 酸式 d 25%
【解析】
(1)装置Ⅰ中烧瓶内浓盐酸与二氧化锰共热反应生成氯化锰、氯气和水;
(2)配制30%NaOH溶液时,用天平称量一定质量的氢氧化钠固体,在烧杯中加水溶解,并用玻璃棒搅拌;
(3)由题给信息可知,次氯酸钠受热易分解生成氯化钠和氯酸钠,降温可以防止NaClO受热分解;
(4)N2H4H2O具有强还原性,若分液漏斗滴液速度过快,部分N2H4·H2O与次氯酸钠反应;
(5)①碘的标准溶液具有氧化性,可以腐蚀橡皮管;
②依据操作不当对标准溶液体积的 影响分析解答;
③由方程式N2H4·H2O+2I2=N2↑+4HI+H2O可得如下关系N2H4·H2O—2I2,由此计算N2H4·H2O的物质的量和质量分数。
(1)装置Ⅰ中烧瓶内浓盐酸与二氧化锰共热反应生成氯化锰、氯气和水,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)配制30%NaOH溶液时,用天平称量一定质量的氢氧化钠固体,在烧杯中加水溶解,并用玻璃棒搅拌,需要玻璃仪器有烧杯、玻璃棒,故答案为:ac;
(3)由题给信息可知,次氯酸钠受热易分解生成氯化钠和氯酸钠,图中装置Ⅱ中用冰水浴控制温度可以防止NaClO受热分解,影响水合肼的产率,故答案为:防止NaClO受热分解,影响水合肼的产率;
(4)由反应方程式示可知,加热蒸馏三颈烧瓶内的溶液可得到水合肼的粗产品;N2H4H2O具有强还原性,若分液漏斗滴液速度过快,部分N2H4·H2O与次氯酸钠反应生成氮气、氯化钠和水,反应的化学方程式为N2H4H2O+2NaClO=N2↑+3H2O+2NaCl,故答案为:蒸馏;N2H4H2O+2NaClO=N2↑+3H2O+2NaCl;
(5)①碘的标准溶液具有氧化性,可以腐蚀橡皮管,应盛放在酸式滴定管中,故答案为:酸式;
②a.锥形瓶清洗干净后未干燥,不影响水合肼的物质的量,对实验结果无影响,故错误;
b.滴定前,滴定管内无气泡,滴定后有气泡会导致碘的标准溶液体积偏小,所测结果偏小,故错误;
c.读数时,滴定前平视,滴定后俯视会导致碘的标准溶液体积偏小,所测结果偏小,故错误;
d.盛标准液的滴定管水洗后,直接装标准液会稀释碘的标准溶液,导致碘的标准溶液体积偏大,所测结果偏高,故正确;
d正确,故答案为:d;
③由方程式N2H4·H2O+2I2=N2↑+4HI+H2O可得如下关系N2H4·H2O—2I2,则3.0g馏分中n(N2H4·H2O)=![]() n(I2)×10=
n(I2)×10=![]() ×0.15 mol·L-1×20×10—3L×10=0.015 mol,则馏分中水合肼(N2H4·H2O)的质量分数为
×0.15 mol·L-1×20×10—3L×10=0.015 mol,则馏分中水合肼(N2H4·H2O)的质量分数为![]() ×100%=25%,故答案为:25%。
×100%=25%,故答案为:25%。

