【题目】某温度下,在一个2 L的恒容密闭容器中,加人4mol A和2mol B进行反应:3A(g)+2B(g) ![]() 4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
A.该反应的化学平衡常数表达式是K=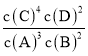
B.此时,B的平衡转化率是20%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加C,B的平衡转化率不变
参考答案:
【答案】D
【解析】
反应前后压强之比为5:4,故反应后气体总物质的量变为4.8mol,结合生成1.6molC,可推知D为气体,C为固体或液体。
A. 由![]() ,因C为非气体,则不能出现在K的表达式中,则化学平衡常数
,因C为非气体,则不能出现在K的表达式中,则化学平衡常数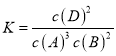 ,故A错误;
,故A错误;
B. 生成1.6molC时,反应的B的物质的量为0.8mol,则B的平衡转化率为![]() ,故B错误;
,故B错误;
C.由于温度没变,化学平衡常数不变,故C错误;
D. 由于C为非气体,增加C对平衡没影响,B的平衡转化率不变,故D正确;
故选D。
-
科目: 来源: 题型:
查看答案和解析>>【题目】对于反应:4CO(g)+2NO2(g)=4CO2(g)+N2(g)△H=-1200KJ/mol,温度不同(T2>T1)其他条件相同时,下列图像正确的是

A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图示与对应的叙述符合的是( )
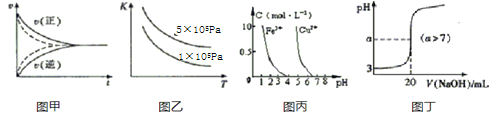
A.图甲实线、虚线分别表示某可逆反应未使用催化剂和使用催化剂的正、逆反应速率随时间的变化
B.图乙表示反应2SO2(g)+O2(g)
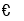 2SO3(g)的平衡常数K与温度和压强的关系
2SO3(g)的平衡常数K与温度和压强的关系C.据图丙,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH=4左右
D.图丁表示常温下向20mL0.001mol/L的醋酸溶液中滴加0.001mol/L的NaOH溶液,溶液的pH随NaOH溶液体积的变化关系
-
科目: 来源: 题型:
查看答案和解析>>【题目】某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示。据图判断正确的是 ( )
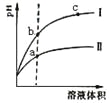
A.Ⅱ为盐酸稀释时pH变化曲线
B.a点Kw的数值比c点Kw的数值大
C.b点溶液的导电性比c点溶液的导电性强
D.b点酸的总浓度大于a点酸的总浓度
-
科目: 来源: 题型:
查看答案和解析>>【题目】A、B、X、Y、Z、W六种短周期主族元素,A是地壳中含量最多的金属元素,短周期主族元素中B的原子半径最大,X、Y、Z、W元素在周期表中的相对位置如图所示,其中Z元素原子最外层电子数是电子层数的2倍。请回答下列问题:
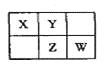
(1)W的最高价氧化物化学式是________________;Z的原子结构示意图为______。
(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为_____________。
(3) AW3可用于净水,其原理是_____________。(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应。下列措施中既能提高反应速率,又能提高原料转化率的是__________________。
a.升高温度
b.加入催化剂
c.将X的简单气态氢化物及时移离
d.增大反应体系的压强
(5)标准状况下,2.24L X的简单气态氢化物被100 mL l mol L-1X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)_______________________________。
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成两种无毒气体而除去,写出用WY2(沸点9.9℃)氧化除去CN-的离子方程式____________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶胞结构如图所示。下列说法中错误的是( )
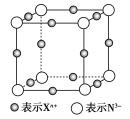
A.晶体中每个Xn+周围有2个等距离且最近的N3-
B.该晶体中阳离子与阴离子的个数比为3︰1
C.n=1
D.Xn+的核外电子数为18
-
科目: 来源: 题型:
查看答案和解析>>【题目】对可逆反应2A(s)+3B(g)
 C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( ) ①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①②B.④C.③D.④⑤
相关试题

