碱式碳酸铜和氯气都是用途广泛的化工原料。
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl−)制备碱式碳酸铜,其制备过程如下:

已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
开始沉淀pH | 4.2 | 5.8 | 1.2 |
完全沉淀pH | 6.7 | 8.3 | 3.2 |
①氯酸钠的作用是 ;
②反应A后调节溶液的pH范围应为 。
③第一次过滤得到的产品洗涤时,如何判断已经洗净? 。
④造成蓝绿色产品中混有CuO杂质的原因是 。
(2)某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。
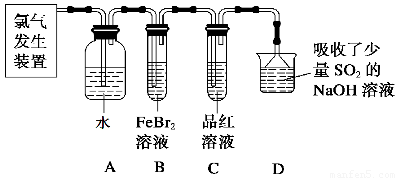
①实验室用二氧化锰和浓盐酸加热制取氯气,所用仪器需要检漏的有 。
②若C中品红溶液褪色,能否证明氯气与水反应的产物有漂白性,说明原因 。此时B装置中发生反应的离子方程式是___________ _____。
③写出A溶液中具有强氧化性微粒的化学式 。若向A溶液中加入NaHCO3粉末,会观察到的现象是 。
参考答案:
(1)①将Fe2+氧化成Fe3+并最终除去②3.2-4.2③取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净④ 反应B的温度过高
(2)①分液漏斗 ②不能证明 因为Cl2也有氧化性,此实验无法确定是Cl2还是HClO漂白
2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2
③ Cl2 HClO ClO- 有无色气体产生 (1分 )
【解析】
试题分析:(1)该化学工艺流程的目的用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl−)制备碱式碳酸铜。必须除去废液Fe2+、Fe3+,结合题给数据分析,需先将Fe2+氧化为Fe3+才能与Cu2+分离开。由题给流程图分析,刻蚀废液加入氯酸钠经反应A将Fe2+氧化为Fe3+,结合题给数据知加入试剂调节pH至3.2-4.2,Fe3+转化为氢氧化铁沉淀经过滤除去,滤液中加入碳酸钠经反应B生成碱式碳酸铜,过滤得产品。①由上述分析知,氯酸钠的作用是将Fe2+氧化成Fe3+并最终除去;②反应A后调节溶液的pH的目的是将铁离子转化为氢氧化铁沉淀而除去,pH范围应为3.2-4.2;③第一次过滤得到的产品为氢氧化铁,表面含有氯离子等杂质离子。洗涤时,判断已经洗净的方法是取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净;④碱式碳酸铜受热分解生成氧化铜,造成蓝绿色产品中混有CuO杂质的原因是反应B的温度过高。(2)① 实验室用二氧化锰和浓盐酸加热制取氯气为固液加热制气体的装置,所用仪器需要检漏的有分液漏斗;② 若C中品红溶液褪色,不能证明氯气与水反应的产物有漂白性,原因是 因为Cl2也有氧化性,此实验无法确定是Cl2还是HClO漂白;C中品红溶液褪色,说明装置B中氯气已过量,此时B装置中亚铁离子和溴离子均已被氧化,发生反应的离子方程式是2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 ;③ 氯气与水反应生成盐酸和次氯酸,该反应为可逆反应,次氯酸为弱酸,则A溶液中具有强氧化性微粒的化学式Cl2 HClO ClO- ;若向A溶液中加入NaHCO3粉末,盐酸和碳酸氢钠反应生成氯化钠、水和二氧化碳,会观察到的现象是有无色气体产生。
考点:以化学工艺流程为载体考查物质的分离提纯等实验基本操作,考查氯气的制备和性质。

