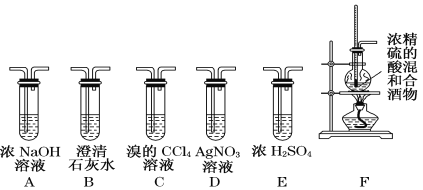
【题目】实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成SO2、CO2、水蒸气等无机物。某研究性学习小组欲用下图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型。回答下列问题:
(1) 写出制备乙烯反应的化学方程式:_____________,实验中,加热F装置时使液体温度迅速升至170℃。从平衡移动原理的角度解释浓硫酸的作用____________。
(2)写出F中生成有机副产物(醚)的化学方程式:____________ 。
(3)为实现上述实验目的,装置的连接顺序为F→________________→D。(各装置限用一次)
(4)当C中观察到溶液褪色时,表明单质溴能与乙烯反应;若D中_______,表明C中发生的是取代反应;若D没有出现前面所描述的现象时,表明C中发生的是_______反应。
【答案】CH3CH2OH![]() CH2===CH2↑+H2O 浓硫酸作催化剂加快反应速率,作吸水剂使平衡向生成乙烯方向移动, CH3CH2OH + CH3CH2OH
CH2===CH2↑+H2O 浓硫酸作催化剂加快反应速率,作吸水剂使平衡向生成乙烯方向移动, CH3CH2OH + CH3CH2OH ![]() CH3CH2OCH2CH3 + H2O (注明1400C更好) A→B→E→C 有浅黄色沉淀生成 加成
CH3CH2OCH2CH3 + H2O (注明1400C更好) A→B→E→C 有浅黄色沉淀生成 加成
【解析】
(1)实验室制备乙烯所用的原料为乙醇,浓硫酸作催化剂、脱水剂,反应条件是加热到170℃,据此写出反应的化学方程式;浓硫酸具有吸水性,能吸收反应生成的水,使平衡正向移动;
(2)乙醇在浓硫酸做催化剂作用下发生分之间脱水生成乙醚;
(3)根据实验目的及题干信息,应该先用氢氧化钠溶液除去SO2、CO2,再用澄清石灰水检验杂质是否除尽,然后用浓硫酸干燥乙烯,再用溴的四氯化碳溶液检验乙烯的性质,用D检验是否有溴化氢生成从而判断乙烯与溴的反应类型;
(4)溴与乙烯若发生反应则C中溴的四氯化碳褪色,若发生加成反应,D中无溴离子,不会产生溴化银沉淀,若发生取代反应,则生成溴化氢,溴化氢与硝酸银反应生成溴化银黄色沉淀,据此解答。
(1)乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,反应的化学方程式为:CH3CH2OH![]() CH2===CH2↑+H2O,浓硫酸作催化剂加快反应速率,作吸水剂使平衡向生成乙烯方向移动;
CH2===CH2↑+H2O,浓硫酸作催化剂加快反应速率,作吸水剂使平衡向生成乙烯方向移动;
因此,本题正确答案是:CH3CH2OH![]() CH2===CH2↑+H2O;浓硫酸作催化剂加快反应速率,作吸水剂使平衡向生成乙烯方向移动;
CH2===CH2↑+H2O;浓硫酸作催化剂加快反应速率,作吸水剂使平衡向生成乙烯方向移动;
(2)乙醇在浓硫酸做催化剂作用下发生分之间脱水生成乙醚,化学方程式:CH3CH2OH + CH3CH2OH![]() CH3CH2OCH2CH3 + H2O;
CH3CH2OCH2CH3 + H2O;
因此,本题正确答案是:CH3CH2OH![]() CH3CH2OCH2CH3 + H2O;
CH3CH2OCH2CH3 + H2O;
(3)为得到纯净的乙烯,应用NaOH溶液除去SO2、CO2,(并用石灰水检验是否除尽),然后用浓硫酸干燥;乙烯与单质溴之间可能发生加成反应,也可能发生取代反应,若是取代反应,则会有HBr生成,HBr与AgNO3溶液反应会产生浅黄色沉淀,所以装置连接顺序为:F→A→B→E→C→D,
因此,本题正确答案是:A→B→E→C;
(4)溴与乙烯若发生反应则C中溴的四氯化碳褪色,若发生取代反应,则生成溴化氢,溴化氢与硝酸银反应生成溴化银黄色沉淀,若发生加成反应,D中无溴离子,不会产生溴化银沉淀;
因此,本题正确答案是:有浅黄色沉淀生成;加成。

