【题目】能正确表示下列反应的离子方程式是( )
A. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O==HClO+HSO3-
B. 0.1mol/LNH4Al(SO4)2溶液与0.2mol/LBa(OH)2溶液等体积混合: Al3++2SO42-+2Ba2++4OH- =2BaSO4+AlO2-+ 2H2O
C. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO![]() + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
D. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H+ +2I-=2Fe2+ +I2 +3H2O
参考答案:
【答案】D
【解析】A项,次氯酸钠溶液具有氧化性,亚硫酸氢根离子具有还原性,二者发生氧化还原反应,离子方程式为:ClO-+SO2+H2O=SO42-+Cl-+2H+,故A错误;B项,NH4Al(SO4)2与Ba(OH)2物质的量之比1:2,离子方程式为:NH4++Al3++2SO42-+2Ba2++4OH-=Al(OH)3↓+2BaSO4↓+NH3H2O,故B错误;C项,高锰酸钾具有强的氧化性,能氧化氯离子,所以不能用盐酸酸化,一般用稀硫酸酸化,故C错误;D项,Fe2O3可溶于氢碘酸,Fe3+具有氧化性能氧化I-,反应的离子方程式为:Fe2O3+2I-+6H+=2Fe2++3H2O+I2,故D正确。
-
科目: 来源: 题型:
查看答案和解析>>【题目】设NA为阿伏加德罗常数,下列叙述正确的是
①lmolCH3CH2C(CH3)3所含甲基个数为4NA
②2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA
③1.0L1.0mol/LCH3COOH溶液中,CH3COOH分子数为NA
④8.8g乙酸乙酯中含共用电子对数为1.4NA
⑤标准状况下,22.4L乙醇完全燃烧后生成CO2的分子数为2NA
⑥常温常压下,17g甲基(一14CH3)所含的中子数为9NA
⑦标准状况下,11.2L氯仿中含有C—Cl键的数目为1.5NA
⑧lmolC15H32分子中含碳碳键数目为14NA
A.①③⑤⑦ B.①②④⑧ C.②③⑥⑧ D.①②⑥⑧
-
科目: 来源: 题型:
查看答案和解析>>【题目】透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶.制备它的一种配方中含有下列四种物质:
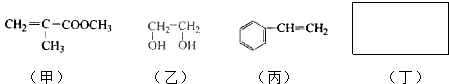
填写下列空白:
(1)甲中不含氧原子的官能团是;下列试剂能与甲反应而褪色的是(填标号)
a.Br2/CCl4溶液 b.石蕊溶液 c.酸性KMnO4溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:
(3)通过下列转化可以得到乙(其中A、B均为有机物):乙醇 A
A 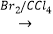 B
B 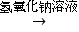 乙
乙
A的分子式是 , 写出B→乙的化学方程式 .
(4)已知: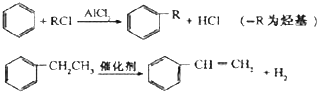
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是 .
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110.丁与FeCl3溶液作用显现特征颜色,且丁分子中烃基上的一氯取代物只有一种.则丁的结构简式为 . -
科目: 来源: 题型:
查看答案和解析>>【题目】现有金属单质A、B和气体甲、乙、丙以及物质D、E、F、G、H。它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
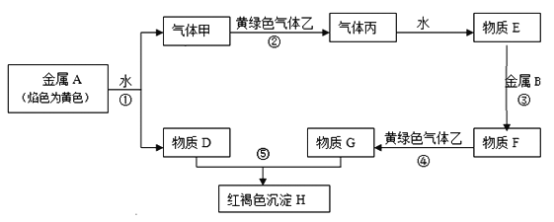
请回答下列问题:
(1)丙的化学式是________________。
(2)写出下列反应的化学方程式,是离子反应的写离子方程式:
反应①_______;反应②________;反应⑤__________。
(3)将0.4gD和1.06g
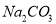 混合并配成溶液,向溶液中滴加0.1
混合并配成溶液,向溶液中滴加0.1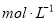 稀盐酸。在下面坐标系中画出能正确表示加入盐酸的体积和生成
稀盐酸。在下面坐标系中画出能正确表示加入盐酸的体积和生成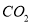 的物质的量的关系图像__________。
的物质的量的关系图像__________。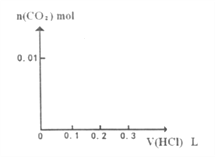
-
科目: 来源: 题型:
查看答案和解析>>【题目】利用海水可以提取溴和镁,提取过程如下:
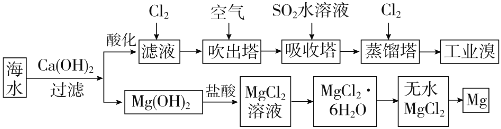
(1)提取溴的过程中,经过2次
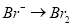 转化的目的是__________,吸收塔中发生反应的离子方程式是
转化的目的是__________,吸收塔中发生反应的离子方程式是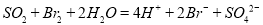 ,蒸馏塔中发生反应的离子方程式是____________。
,蒸馏塔中发生反应的离子方程式是____________。(2)从
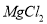 溶液中得到
溶液中得到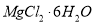 晶体的主要操作是__________、_________、过滤、洗涤、干燥。由无水氯化镁得到镁的化学方程式是__________。
晶体的主要操作是__________、_________、过滤、洗涤、干燥。由无水氯化镁得到镁的化学方程式是__________。(3)据上述流程,将
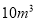 海水中溴元素(海水中
海水中溴元素(海水中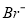 离子含量为
离子含量为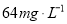 )转化为工业溴,整个流程中至少需要标准状况下
)转化为工业溴,整个流程中至少需要标准状况下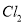 的体积为_________L(忽略
的体积为_________L(忽略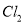 溶解)。
溶解)。 -
科目: 来源: 题型:
查看答案和解析>>【题目】某芳香烃A是有机合成中非常重要的原料,通过质谱法测得其最大质荷比为118;其核磁共振氢谱中有5个峰,峰面积之比为1:2:2:2:3;其苯环上只有一个取代基.以下是以A为原料合成高分子化合物F、I的路线图,试回答下列问题:
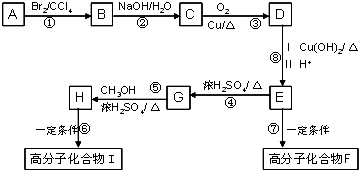
(1)A的结构简式为;
(2)E中的官能团名称是;
(3)G的结构简式为;
(4)反应②、④的反应类型分别是 , ;
(5)反应③的化学方程式:;
(6)反应⑥、⑦生成的高分子化合物的反应原理是否相同?;
(7)符合以下条件的C的同分异构体有种(不考虑立体异构) a、苯环上有两个取代基 b、苯环上的一氯代物有两种
c、加入三氯化铁溶液显色 d、向1mol该物质中加入足量的金属钠可产生1mol氢气. -
科目: 来源: 题型:
查看答案和解析>>【题目】某工厂的废金属屑中主要成分为Cu和Fe,此外还含有少量
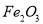 ,该厂用上述废金属屑制取新型高效水处理剂
,该厂用上述废金属屑制取新型高效水处理剂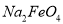 (高铁酸钠)等产品,过程如下:
(高铁酸钠)等产品,过程如下:I. 向废金属屑中加入稀
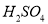 ,充分反应后,剩余两种固体单质和溶液;
,充分反应后,剩余两种固体单质和溶液;II. 向I所得固体中继续加入足量稀
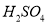 ,过滤后,向所得固体中加入硫酸酸化的
,过滤后,向所得固体中加入硫酸酸化的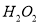 ,固体溶解得
,固体溶解得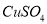 溶液;
溶液;III. ……
(1)步骤I所得溶液中加入KSCN溶液无明显现象,用离子方程式解释其可能的原因______________________________________。步骤I所得溶液中滴加NaOH溶液,看到的现象是________,涉及的化学反应方程式是_________、_______________。向I所得固、液混合物中通入过量氯气,并不断搅拌,充分反应后,溶液中的金属阳离子是(填写离子符号)____________。
(2)步骤II中
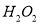 在酸性条件下氧化了铜,获得
在酸性条件下氧化了铜,获得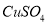 溶液。参加反应的
溶液。参加反应的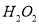 与Cu的物质的量之比为____________。
与Cu的物质的量之比为____________。(3)步骤I所得溶液经进一步处理可制得
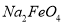 ,流程如下:
,流程如下:
写出由
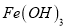 制取
制取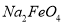 的离子反应方程式______________________。
的离子反应方程式______________________。
相关试题

