
【题目】 Kx[Cu(C2O4)y]·zH2O (水合草酸铜(Ⅱ)酸钾)是一种化工原料,实验室制备少量水合草酸铜酸钾并测定样品的组成,实验步骤如下:
I制备CuO
用图1所示装置将溶液混合后,小火加热至蓝色沉淀变黑色生成CuO,煮沸5~10分钟。稍冷却后全部转移至图2装置过滤,并用蒸馏水洗涤沉淀2~3次。
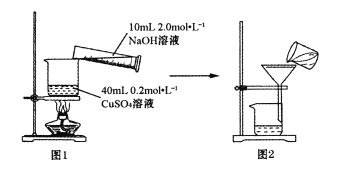
(1)①指出图2装置中操作中的错误___________,图2操作需用蒸馏水洗涤沉淀2~3次,其目为___________。
②检验沉淀洗涤干净的方法为___________。
Ⅱ制备KHC2O4和K2C2O4混合溶液
称取3.0g H2C2O4·2H2O放入250mL烧杯中,加入40mL蒸馏水,微热(温度低于80℃)溶解。稍冷后分数次加入2.2g无水K2CO3,充分反应后生成含KHC2O4和K2C2O4的混合物。
(2)该步骤中所得混合物中n(KHC2O4):n(K2C2O4)=____________。(取整数)
Ⅲ制备水合草酸铜酸钾晶体
将KHC2O4和K2C2O4混合溶液水浴微热,再将CuO连同滤纸一起加入到该溶液中,充分反应至CuO沉淀全部溶解,取出滤纸后,加热浓缩、冷却结晶、过滤,用乙醇淋洗,自然晾干,称量得到样品2.9760g(电子天平称量)。
(3)①步骤Ⅲ中KHC2O4的作用是__________。
②用乙醇淋洗而不用水的优点是__________。
③溶解CuO沉淀时,连同滤纸一起加人到溶液中的目的是__________。
Ⅳ测定水合草酸铜酸钾晶体的成分
取少量制得的样品配成溶液。用标准酸性髙锰酸钾溶液滴定![]() 、用标准EDTA溶液(PAR为指示剂)滴定Cu2+,经计算样品中n(Cu):n(
、用标准EDTA溶液(PAR为指示剂)滴定Cu2+,经计算样品中n(Cu):n(![]() )=1:2,假设制备样品的过程中Cu2+无损耗。
)=1:2,假设制备样品的过程中Cu2+无损耗。
(4)水合草酸铜(Ⅱ)酸钾晶体的化学式为__________。
【答案】过滤时转移固液混合物没有通过玻璃棒引流 除去沉淀表面吸附的可溶性杂质离子 取少量最后一次洗涤流出液于试管中,滴入BaCl2溶液,若无白色沉淀生成,则已经洗涤干净 2:1 加快CuO的溶解(或酸性环境促进CuO的溶解) 减少水合草酸铜酸钾的溶解损耗,加快晶体表面水分挥发 防止CuO的损耗 K2[Cu(C2O4)2]·3H2O
【解析】
本实验的目的是制备少量水合草酸铜酸钾并测定样品的组成;首先利用硫酸铜和氢氧化钠溶液制取氢氧化铜沉淀,加热使其分解得到CuO;然后H2C2O4·2H2O和无水K2CO3制备KHC2O4和K2C2O4混合溶液;然后将KHC2O4和K2C2O4混合溶液水浴微热,再将CuO连同滤纸一起加入到该溶液中,充分反应,经系列操作得到样品;最后测定水合草酸铜酸钾晶体的成分。
(1)①图2装置中操作中的错误为:过滤时转移固液混合物没有通过玻璃棒引流;为除去沉淀表面吸附的可溶性杂质离子,需要用蒸馏水洗涤沉淀2~3次;;
②得到的CuO固体表面可能附着有硫酸钠,可以通过检验硫酸根来确定沉淀是否洗涤干净,具体方法为:取少量最后一次洗涤流出液于试管中,滴入BaCl2溶液,若无白色沉淀生成,则已经洗涤干净;
(2)3.0g H2C2O4·2H2O的物质的量为![]() ≈0.0238mol,2.2g无水K2CO3的物质的量为
≈0.0238mol,2.2g无水K2CO3的物质的量为![]() ≈0.0159mol,则根据碳元素守恒可得:n(KHC2O4)+n(K2C2O4)=0.0238 mol,根据K元素守恒可得n(KHC2O4)+2n(K2C2O4)=(0.0159×2)mol,联立解得n(KHC2O4)=0.0158mol,n(K2C2O4)=0.0080mol,所以n(KHC2O4):n(K2C2O4)=2:1;
≈0.0159mol,则根据碳元素守恒可得:n(KHC2O4)+n(K2C2O4)=0.0238 mol,根据K元素守恒可得n(KHC2O4)+2n(K2C2O4)=(0.0159×2)mol,联立解得n(KHC2O4)=0.0158mol,n(K2C2O4)=0.0080mol,所以n(KHC2O4):n(K2C2O4)=2:1;
(3)①KHC2O4可以电离出氢离子,加快CuO的溶解;
②用乙醇淋洗可以减少水合草酸铜酸钾的溶解损耗,同时乙醇易挥发可以加快晶体表面水分挥发;
③滤纸上附着有CuO,连同滤纸一起加人到溶液中可以减少CuO的损耗;
(4)已知样品中n(Cu):n(![]() )=1:2,所以y=2,根据电荷守恒可知x=2,所以根据n(K2C2O4)=0.0080mol,可知n(K2[Cu(C2O4)2]·zH2O)=0.0080mol,样品质量为2.9760g,所以有
)=1:2,所以y=2,根据电荷守恒可知x=2,所以根据n(K2C2O4)=0.0080mol,可知n(K2[Cu(C2O4)2]·zH2O)=0.0080mol,样品质量为2.9760g,所以有![]() =0.0159mol,解得z=3,所以水合草酸铜(Ⅱ)酸钾晶体的化学式为K2[Cu(C2O4)2]·3H2O。
=0.0159mol,解得z=3,所以水合草酸铜(Ⅱ)酸钾晶体的化学式为K2[Cu(C2O4)2]·3H2O。


 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案科目:高中化学 来源: 题型:
【题目】若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是( )
A.0.2mol/LNH4HCO3溶液(pH>7):c(![]() )>c(
)>c(![]() ),c(H2CO3)>c(NH3H2O)
),c(H2CO3)>c(NH3H2O)
B.0.2mol/L氨水:0.2mol/L>c(OH-)+ c(NH3H2O)
C.向0.1mol/LNH4HCO3溶液中通入CO2至溶液pH=7:c(![]() )=c(
)=c(![]() )+c(
)+c(![]() )
)
D.pH=2的盐酸与pH=12的氨水等体积混合:c(![]() )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案不能达到预期目的的是
实验方案 | 实验目的 | |
A | 向两支试管中分别加入 | 探究 |
B | 取 | 配制8%的 |
C | 将 | 比较 |
D | 测同温同浓度 | 比较硫和硅两元素非金属性强弱 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某晶体的晶胞结构为正三棱柱(如图所示),这种晶体中A、B、C三种微粒数目之比为( )

A. 1∶4∶2 B. 3∶9∶4
C. 2∶9∶4 D. 3∶8∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国学者最近研发一种新型铝—石墨烯电池,其负极是金属铝,正极是石墨烯(Cn)薄膜,电解质为阳离子(EMI+)与阴离子(![]() )组成的离子液体,该电池的工作原理如图。已知能量密度是指一定质量物质中储存能量的大小。下列说法错误的是
)组成的离子液体,该电池的工作原理如图。已知能量密度是指一定质量物质中储存能量的大小。下列说法错误的是
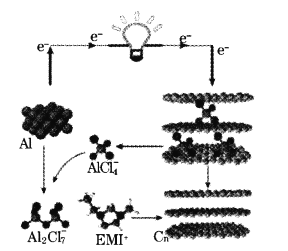
A.该铝电极电池比锂电极电池的能量密度低
B.石墨烯电极的比表面积大,充放电性能优于石墨电极
C.充电时,有机阳离子(EMI+)向铝电极移动
D.放电时,负极的电极反应式为2Al+7Clˉ-6eˉ=Al2Cl![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2A为二元弱酸。室温下,下列指定溶液中微粒物质的量浓度关系正确的是(忽略溶液混合引起的体积变化)( )
A.0.1mol/LH2A溶液:c(H2A)>c(HA-)>c(A2-)>c(H+)
B.0.1mol/LNaHA溶液(pH<7):c(Na+)>c(HA-);c(H2A)>c(A2-)
C.0.1mol/LNaHA溶液和0.1mol/LNaOH溶液等体积混合:c(OH-)=c(H+)+c(HA-)+2c(H2A)
D.0.1mol/LNaHA溶液(pH<7)和0.1mol/LH2A溶液等体积混合:c(Na+)>c(HA-)+2c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10 mL 0.2 mol/L的KIO3溶液中逐渐加入NaHSO3粉末,生成的I2的物质的量随所加NaHSO3的物质的量变化如图所示,下列说法不正确的是( )

A.A点对应的I2的物质的量为1.0×10-3 mol
B.oa : ab = 4 : 1
C.当溶液中的n(I2) = 5×10-4 mol时,加入NaHSO3的物质的量可能为2.5×10-3 mol或5.5×10-3 mol
D.由ab段反应可知,氧化性I2 >![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型漂白剂结构如图所示,其中W.Y.Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列说法正确的是
![]()
A.非金属性:X>W>Y
B.Y的最高价氧化为对应的水化物为三元酸
C.可利用W与X、Y形成的化合物热还原制备单质Y
D.该漂白剂中仅有X均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于价电子排布式为3s23p4的粒子的描述正确的是( )
A. 它的原子核外有三种形状不同的电子云
B. 它的原子核外电子共有16种不同的运动状态
C. 它可与H2反应生成常温时的液态化合物
D. 该原子的轨道表示式为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com