【题目】实验室需要配制240 mL 0.8 mol·L-1的NaOH溶液,请回答下列问题:
(1)称取NaOH固体______g。
(2)在配制该溶液过程中,需经过称量、溶解、转移溶液、定容等操作,下列图示对应的操作规范是______。根据图示,除称量外还缺少的操作步骤依次是___________、__________。
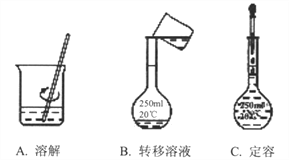
(3)在配制过程中,若其他操作都正确,下列操作会引起NaOH溶液浓度偏低的是__________。
A.称量好的固体放置一段时间后进行溶解操作
B.溶液未冷却至室温即转移到容量瓶中
C.容量瓶水洗后未干燥
D.转移溶液时不慎有少量溶液滴出瓶外
E.定容时不小心有蒸馏水滴出瓶外
【答案】8.0 A 洗涤 摇匀 AD
【解析】
(1)依据m=cVM计算需要溶质的质量;
(2)配制一定物质的量浓度溶液一般步骤为:计算、称量、溶解并冷却、移液、洗涤、定容、摇匀等,结合溶解、移液、定容的正确操作解答;
(3)分析操作对溶质的物质的量和溶液体积的影响,依据c=n/V进行误差分析。
(1)实验室需要配制240 mL 0.8 mol·L-1的NaOH溶液,需要250mL容量瓶,则需称取NaOH固体的质量是0.25L×0.8mol/L×40g/mol=8.0g。
(2)配制一定物质的量浓度溶液一般步骤为:计算、称量、溶解并冷却、移液、洗涤、定容、摇匀等,所以缺少的步骤为:洗涤、摇匀;
搅拌时玻璃棒沿着一个方向进行,故A正确;
移液时应用玻璃棒引流,故B错误;
定容时,胶头滴管不能伸入到容量瓶内,故C错误;
答案选A。
(3)A.称量好的固体放置一段时间后进行溶解操作,导致部分氢氧化钠与空气中二氧化碳反应,氢氧化钠物质的量偏小,溶液浓度偏低,故A选;
B.溶液未冷却至室温即转移到容量瓶中,冷却后溶液体积偏小,溶液浓度偏高,故B不选;
C.容量瓶水洗后未干燥,对溶液体积和溶质的物质的量都不产生影响,溶液浓度不变,故C不选;
D.转移溶液时不慎有少量溶液滴出瓶外,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故D选;
E.定容时不小心有蒸馏水滴出瓶外,对溶液体积和溶质的物质的量都不产生影响,溶液浓度不变,故E不选;
答案选AD。

