
【题目】溴苯是一种化工原料,实验室制备溴苯的一种装置图如图所示:
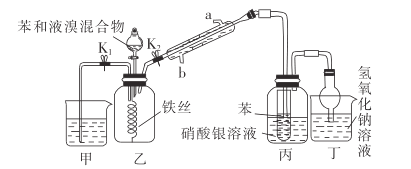
(1)盛装苯和液溴混合物的仪器名称是___________,冷凝水应从_____________(填“a”或“b”)口进入;实验开始时,打开________________(填“![]() ”或“
”或“![]() ”,下同),关闭_________________。
”,下同),关闭_________________。
(2)乙装置中发生反应的化学方程式为________________________________。
(3)丁装置中球形干燥管的作用是_____________________________。
(4)丙装置中的现象是________________________________。
(5)若实验时,实验室无液溴,但有溴水,则如何操作才能继续让该实验做成功?_______。
【答案】分液漏斗 b K2 K1 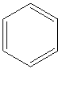 +Br2
+Br2![]()
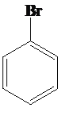 +HBr、2Fe+3Br2=2FeBr3 防止倒吸 小试管中有气泡冒出,液体变成棕黄色,有白雾出现,广口瓶内溶液中有浅黄色沉淀生成 将苯与溴水混合,将溴水中的溴萃取到苯中,再加Fe进行催化反应
+HBr、2Fe+3Br2=2FeBr3 防止倒吸 小试管中有气泡冒出,液体变成棕黄色,有白雾出现,广口瓶内溶液中有浅黄色沉淀生成 将苯与溴水混合,将溴水中的溴萃取到苯中,再加Fe进行催化反应
【解析】
苯和液溴在Fe作催化剂的条件下发生取代反应,生成溴苯和溴化氢,由于该反应放热,苯、液溴易挥发,用冷凝的方法可以减少挥发,装置丙的目的是防止因HBr易溶于水而引起倒吸,通过检验Br-的存在证明这是一个取代反应。
(1)根据装置,盛有苯和液溴的装置叫做分液漏斗;冷凝水应从下口进入,即b口,因为从上口流入,冷却水很快的流出冷凝管,蒸汽冷却效果较差;实验开始时,应将K2打开关闭K1。
(2)乙装置中苯和液溴在Fe做催化剂的条件下发生反应生成溴苯和溴化氢,化学方程式为: +Br2
+Br2![]()
 +HBr、2Fe+3Br2=2FeBr3;
+HBr、2Fe+3Br2=2FeBr3;
(3)丁为吸收溴化氢气体的装置,用球形干燥管的作用是防止倒吸;
(4)丙装置的现象是:小试管中有气泡冒出,液体变成棕黄色,有白雾出现,广口瓶内溶液中有浅黄色沉淀生成;
(5)若实验时没有液溴,可将苯与溴水混合,将溴水中的溴萃取到苯中,再加Fe进行催化反应,即可发生反应。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素。稀土元素有“工业维生素”的美称,如今已成为极其重要的战略资源。
(1)钪(Sc)为21号元素,基态原子电子排布式为____。
(2)离子化合物Na3[Sc(OH)6]中,存在的化学键除离子键外还有__。
(3)Sm(钐)的单质与l,2-二碘乙烷可生成乙烯:Sm + ICH2CH2I →SmI2+ CH2=CH2。
则lmol CH2=CH2中含有的σ键数目为___。(用NA表示阿伏伽德罗常数的值)
(4)与N3-互为等电子体的分子有___(写其中一个的化学式即可)。
(5)Ce(铈)单质为面心立方晶体,其晶胞参数a=516pm。Ce(铈)原子的配位数为___,列式表示Ce(铈)单质的密度:___g/cm3(用NA表示阿伏伽德罗常数的值,不必计算出结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某反应过程中的能量变化如下图所示:
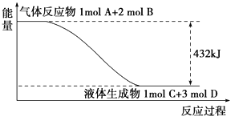
写出该反应的热化学方程式________。
(2)在溶液中进行的化学反应中的物质,其状态标为“aq”,已知1 molHCl在溶液中与足量氢氧化钠反应放出57.3 kJ的热量,用离子方程式写出该反应的热化学方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
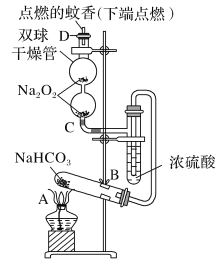
(1)在A试管内发生反应的化学方程式是_____。
(2)B装置的作用是_____。
(3)在双球干燥管内发生反应的化学方程式为____。
(4)双球干燥管内及D处观察到的实验现象是_____。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内及D处观察到的实验现象是:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述中,正确的是( )
A. 含20.0gNaOH的稀溶液与足量的稀硫酸完全中和,放出28.7kJ的热量,则表示中和热的热化学方程式为2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.8kJ·mol-1
B. 已知热化学方程式:SO2(g)+![]() O2(g)
O2(g)![]() SO3(g) △H=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为196.64kJ
SO3(g) △H=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为196.64kJ
C. 已知2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1,则H2的燃烧热为241.8kJ·mol-1
D. 已知石墨转化为金刚石为吸热,那么石墨比金刚石稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 24 g 镁与27 g铝中,含有相同的质子数
B. 同等质量的氧气和臭氧中,电子数相同
C. 1 mol重水与1 mol水中,中子数比为2∶1
D. 1 mol乙烷和1 mol乙烯中,化学键数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向一个3L的真空密闭容器中(预先装入催化剂)通入1 mol N2和3 mol H2,经过一段时间后,测得容器内压强是起始时的0.9倍。在此时间段内v(H2)为0.1 mol·L-1·min-1,则经过的时间为( )
A. 2 min B. 3 min C. 4 min D. 6 min
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1L的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
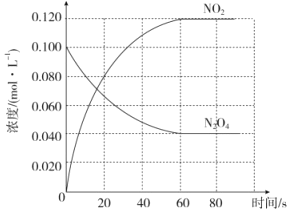
(1)反应的△H______0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为________molL-1s-1
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020molL-1s-1的平均速率降低,10s又达到平衡。T_______100℃(填“大于”“小于”)。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向_______(填“正反应”或“逆反应”)方向移动
(4)再次到达平衡后,向容器中加入合适的正催化剂,则v正_______v逆_______,(填“增大”、“减小”或“不变”),体系的颜色_______(填“变深” “变浅”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第____周期第_____族。
(2)N的基态原子核外电子排布式为_____;Cu的基态原子最外层有___个电子。
(3)用“>”或“<”填空:
原子半径 | 电负性 | 熔点 | 沸点 |
Al_____Si | N____O | 金刚石_____晶体硅 | CH4____SiH4 |
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
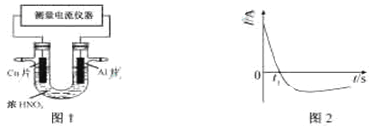
0-t1时,原电池的负极是Al片,此时,正极的电极反应式是_____,溶液中的H+向___极移动,t1时,原电池中电子流动方向发生改变,其原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com