【题目】H2NCOONH4(59℃时升华并分解)可用作磷化铝中间体及医药等。可由干燥的NH3与CO2在低温下(或冰水浴)制取,装置如图所示:
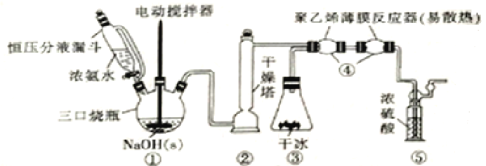
回答下列问题:
(1)装置①中用“恒压分液漏斗”代替普通的分液漏斗,其优点是_____________,滴入浓氨水并搅拌能产生大量NH3的原因是____________________,装置②干燥塔中盛放的合适干燥剂是_____________(填名称)。
(2)装置③用盛干冰装置代替实验室制备CO2的常见制备及纯化转置,其优点除装置简洁且可产生纯净干燥的CO2外,还具有的优点是____________________________________。
(3)装置④用“聚乙烯薄膜反应器”代替反应管的优点是____________,“聚乙烯薄膜反应器”中发生反应的化学方程式为_____________________________________________。
(4)从环境保护角度分析,装置⑤的作用是_____________,还可以通过观察气泡确定NH3和CO2的比例是否合适,判断的依据及不合适时的调节方案为________________。
【答案】便于液体顺利滴入三口烧瓶中 NH3(g)+H2O(1)![]() NH3·H2O(aq)
NH3·H2O(aq)![]() NH4+(aq)+OH-(aq),增大了OH-浓度使平衡逆向移动,且NaOH固体可以吸水,减少了游离水的量并放出了热量,这都有利于NH3逸出 碱石灰 干冰升华吸热,可维持反应在低温下进行 可轻轻揉搓得到粉末状的H2NCOONH4(或易散热,有利于提高H2NCOONH4的转化率并避免分解) 2NH3+CO2=H2NCOONH4 吸收未反应完的NH3 若无气泡产生,说明比例合适,若有气泡产生,可以通过调节恒压滴液漏斗的活塞控制浓氨水的加入速率
NH4+(aq)+OH-(aq),增大了OH-浓度使平衡逆向移动,且NaOH固体可以吸水,减少了游离水的量并放出了热量,这都有利于NH3逸出 碱石灰 干冰升华吸热,可维持反应在低温下进行 可轻轻揉搓得到粉末状的H2NCOONH4(或易散热,有利于提高H2NCOONH4的转化率并避免分解) 2NH3+CO2=H2NCOONH4 吸收未反应完的NH3 若无气泡产生,说明比例合适,若有气泡产生,可以通过调节恒压滴液漏斗的活塞控制浓氨水的加入速率
【解析】
装置①由浓氨水分解制NH3,经过②干燥,与③中干冰升华产生的CO2一起进入④中反应,得到产物H2NCOONH4,装置⑤中的浓H2SO4可以吸收多余的NH3。
(1)装置①中的“恒压分液漏斗”侧面有一根玻璃管连通上下,可以平衡漏斗中液体上下的气压,便于液体顺利滴入三口烧瓶中;浓氨水中存在反应NH3(g)+H2O(1)![]() NH3·H2O(aq)
NH3·H2O(aq)![]() NH4+(aq)+OH-(aq),NaOH遇水产生大量的热,并且有大量OH-,促使平衡向生成NH3的方向移动,从而产生大量NH3;NH3一般用碱石灰进行干燥;
NH4+(aq)+OH-(aq),NaOH遇水产生大量的热,并且有大量OH-,促使平衡向生成NH3的方向移动,从而产生大量NH3;NH3一般用碱石灰进行干燥;
(2)NH3与CO2在低温下反应制取,干冰升华吸热,可以维持低温环境;
(3)“聚乙烯薄膜反应器”比较柔软,可以隔着反应器揉搓得到粉末状的H2NCOONH4,而且薄膜容易散热,有利于提高H2NCOONH4的转化率并避免分解;反应的化学方程式为2NH3+CO2=H2NCOONH4;
(4)由于NH3有污染,浓H2SO4可以吸收多余的NH3;浓H2SO4可以吸收多余的NH3,但不会吸收CO2,若NH3与CO2比例刚好能完全反应,则不会有CO2剩余,那么浓H2SO4中就不会看到气泡,若能看到气泡,则说明CO2产生的较快,需要加快NH3的速率。

