2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第87页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
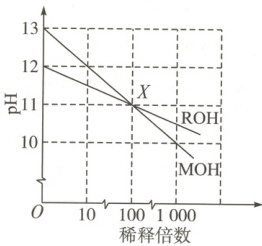
7. (双选)25℃,两种一元碱MOH和ROH的溶液分别加水稀释,溶液pH的变化如图所示。下列叙述正确的是(
A.MOH是一种弱碱
B.在X点:c(M⁺) = c(R⁺)
C.稀释前,c(MOH) < 10c(ROH)
D.稀释前,MOH溶液和ROH溶液中由水电离出的c(OH⁻):前者是后者的10倍
BC
)。
A.MOH是一种弱碱
B.在X点:c(M⁺) = c(R⁺)
C.稀释前,c(MOH) < 10c(ROH)
D.稀释前,MOH溶液和ROH溶液中由水电离出的c(OH⁻):前者是后者的10倍
答案:
BC 解析由题图可知,两溶液分别稀释100倍,$\mathrm{MOH}$溶液的pH减小2,$\mathrm{ROH}$溶液的pH减小1,则$\mathrm{MOH}$是强碱,$\mathrm{ROH}$是弱碱,A项错误。X点两溶液的pH相等,则两溶液中$c(\mathrm{H^+})$、$c(\mathrm{OH^-})$分别相等;据电荷守恒可得:$c(\mathrm{M^+}) + c(\mathrm{H^+}) = c(\mathrm{OH^-})$,$c(\mathrm{R^+}) + c(\mathrm{H^+}) = c(\mathrm{OH^-})$,从而推知X点时$c(\mathrm{M^+}) = c(\mathrm{R^+})$,B项正确。$\mathrm{MOH}$是强碱,起始溶液的pH = 13,则有$c(\mathrm{MOH}) = 0.1\ \mathrm{mol· L^{-1}}$;$\mathrm{ROH}$是弱碱,部分电离,起始溶液的pH = 12,则有$c(\mathrm{ROH})>0.01\ \mathrm{mol· L^{-1}}$,从而可知稀释前,$c(\mathrm{MOH})<10c(\mathrm{ROH})$,C项正确。稀释前,$\mathrm{MOH}$溶液的pH = 13,则由水电离出的$c(\mathrm{OH^-}) = 1×10^{-13}\ \mathrm{mol· L^{-1}}$;$\mathrm{ROH}$溶液的pH = 12,则由水电离出的$c(\mathrm{OH^-}) = 1×10^{-12}\ \mathrm{mol· L^{-1}}$,故稀释前$\mathrm{MOH}$溶液和$\mathrm{ROH}$溶液中由水电离出的$c(\mathrm{OH^-})$:后者是前者的10倍,D项错误。
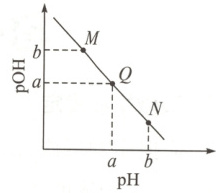
8. 常温下,向一定体积pH = 13的氢氧化钾溶液中逐滴加入pH = 1的稀盐酸,溶液的pH与pOH[pOH = -lg c(OH⁻)]的变化关系如图所示。下列有关说法错误的是(
A.Q点溶液呈中性,且a = 7
B.M点和N点水的电离程度不相等
C.Q点消耗稀盐酸的体积等于氢氧化钾溶液的体积
D.若b = 12,则N点消耗稀盐酸的体积与氢氧化钾溶液的体积之比为9 : 11
B
)。
A.Q点溶液呈中性,且a = 7
B.M点和N点水的电离程度不相等
C.Q点消耗稀盐酸的体积等于氢氧化钾溶液的体积
D.若b = 12,则N点消耗稀盐酸的体积与氢氧化钾溶液的体积之比为9 : 11
答案:
B 解析M点溶液的pOH与N点溶液的pH相等,即M点溶液(呈酸性)中氢离子和N点溶液(呈碱性)中氢氧根离子的浓度相等,二者对水的电离的抑制程度相等,所以水的电离程度相等,B项错误。
9. 如表是不同温度下水的离子积:
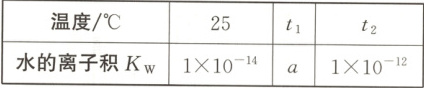
请回答以下问题。
(1) 若25 < t₁ < t₂,则a
(2) 25℃时,某Na₂SO₄溶液中c(SO₄²⁻) = 5×10⁻⁴mol·L⁻¹,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na⁺) : c(OH⁻) =
(3) 在t₂℃,pH = 10的NaOH溶液中,水电离产生的OH⁻浓度为
(4) 在t₂℃时由水电离出的c(H⁺) = 1×10⁻⁶mol·L⁻¹。若该温度下,某溶液的pH = 7,则该溶液
A. 呈中性
B. 呈碱性
C. 呈酸性
D. c(OH⁻) = 100c(H⁺)

请回答以下问题。
(1) 若25 < t₁ < t₂,则a
>
(填“>”“<”或“=”)1×10⁻¹⁴。(2) 25℃时,某Na₂SO₄溶液中c(SO₄²⁻) = 5×10⁻⁴mol·L⁻¹,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na⁺) : c(OH⁻) =
1000:1
。(3) 在t₂℃,pH = 10的NaOH溶液中,水电离产生的OH⁻浓度为
$1×10^{-10}\ \mathrm{mol· L^{-1}}$
。(4) 在t₂℃时由水电离出的c(H⁺) = 1×10⁻⁶mol·L⁻¹。若该温度下,某溶液的pH = 7,则该溶液
BD
(填字母)。A. 呈中性
B. 呈碱性
C. 呈酸性
D. c(OH⁻) = 100c(H⁺)
答案:
(1)>
(2)1000:1
(3)$1×10^{-10}\ \mathrm{mol· L^{-1}}$
(4)BD
(1)>
(2)1000:1
(3)$1×10^{-10}\ \mathrm{mol· L^{-1}}$
(4)BD
查看更多完整答案,请扫码查看


