2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第86页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
【对点训练3】常温下,pH = 11的X、Y两种碱溶液各1mL,分别稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是(
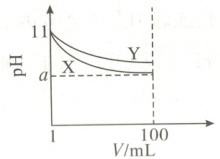
A.X、Y两种碱溶液中溶质的物质的量浓度一定相等
B.稀释后,X溶液的碱性比Y溶液的碱性强
C.分别完全中和X、Y这两种碱溶液时,消耗同浓度盐酸的体积:V(X) > V(Y)
D.若9 < a < 11,则X、Y都是弱碱
D
)。
A.X、Y两种碱溶液中溶质的物质的量浓度一定相等
B.稀释后,X溶液的碱性比Y溶液的碱性强
C.分别完全中和X、Y这两种碱溶液时,消耗同浓度盐酸的体积:V(X) > V(Y)
D.若9 < a < 11,则X、Y都是弱碱
答案:
D 解析因为pH = 11的X、Y两种碱溶液稀释到原溶液体积的100倍时,pH:Y>X,所以物质的量浓度:$c(Y)>c(X)$,稀释后溶液碱性:Y>X,A、B项均错误;因为$c(Y)>c(X)$且$V(Y) = V(X)$,故$n(Y)>n(X)$,所以消耗同浓度的盐酸时,Y消耗得多,C项错误;若9<a<11,说明稀释到原溶液体积的100倍时,X、Y的pH均减小不到2个单位,则X、Y都是弱碱,D项正确。
1. 40℃时水的离子积Kₙ = 2.9×10⁻¹⁴,则在40℃时,c(H⁺) = 1×10⁻⁷mol·L⁻¹的溶液(
A.呈酸性
B.呈碱性
C.呈中性
D.无法判断
B
)。A.呈酸性
B.呈碱性
C.呈中性
D.无法判断
答案:
B
2. 常温下,某溶液中由水电离出来的c(H⁺) = 1.0×10⁻¹¹mol·L⁻¹,该溶液可能是(
① 二氧化硫的水溶液 ② 氯化钠水溶液 ③ 硝酸钠水溶液 ④ 氢氧化钠水溶液
A.①④
B.①②
C.②③
D.③④
A
)。① 二氧化硫的水溶液 ② 氯化钠水溶液 ③ 硝酸钠水溶液 ④ 氢氧化钠水溶液
A.①④
B.①②
C.②③
D.③④
答案:
A 解析常温下溶液中由水电离出来的$c(\mathrm{H^+}) = 1.0×10^{-11}\ \mathrm{mol· L^{-1}}$,与纯水中的氢离子浓度比较可知,水的电离被抑制,溶液为酸溶液或碱溶液。二氧化硫溶于水生成了亚硫酸,亚硫酸电离出氢离子,会抑制水的电离,故①正确;氯化钠溶液为中性,水的电离程度不会减小,故②错误;硝酸钠溶液为中性,水的电离程度不会减小,故③错误;氢氧化钠为强碱,会抑制水的电离,故④正确。
3. 在体积都为1L,c(H⁺)都为0.01mol·L⁻¹的盐酸和醋酸中,投入0.65g锌粒,则下列图示符合客观事实的是(
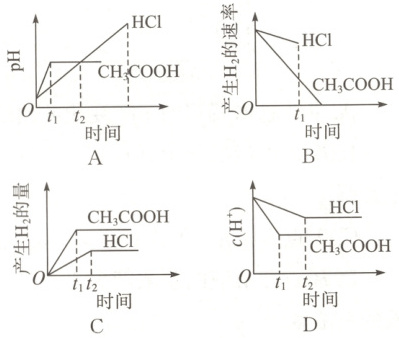
C
)。
答案:
C
4. 常温下,pH = 12的NaOH溶液与pH = 1的HCl溶液按一定比例混合,所得溶液pH = 2,则NaOH溶液与HCl溶液的体积比为(
A.1 : 9
B.2 : 9
C.9 : 2
D.10 : 1
C
)。A.1 : 9
B.2 : 9
C.9 : 2
D.10 : 1
答案:
C 解析$\mathrm{NaOH}$溶液中$c(\mathrm{OH^-}) = 1×10^{-2}\ \mathrm{mol· L^{-1}}$,盐酸中$c(\mathrm{H^+}) = 1×10^{-1}\ \mathrm{mol· L^{-1}}$,设$\mathrm{NaOH}$溶液与$\mathrm{HCl}$溶液的体积分别为$x\ \mathrm{L}$和$y\ \mathrm{L}$,根据混合溶液pH = 2,即混合溶液中$c(\mathrm{H^+}) = 1×10^{-2}\ \mathrm{mol· L^{-1}}$,得$\frac{1×10^{-1}y - 1×10^{-2}x}{x + y}\ \mathrm{mol· L^{-1}} = 1×10^{-2}\ \mathrm{mol· L^{-1}}$,解得$x:y = 9:2$,C项正确。
5. 一定温度下,水溶液中H⁺和OH⁻的浓度变化曲线如图,下列说法正确的是(
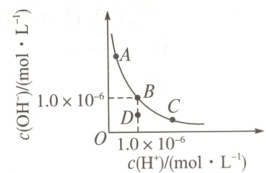
A.该温度下,A点溶液呈碱性
B.该温度下,0.01mol·L⁻¹NaOH溶液中c(H⁺) = 1.0×10⁻¹²mol·L⁻¹
C.该温度下,加入NaOH可能引起由D向B的变化
D.B点时,降低温度,可能引起由B向C的变化
A
)。
A.该温度下,A点溶液呈碱性
B.该温度下,0.01mol·L⁻¹NaOH溶液中c(H⁺) = 1.0×10⁻¹²mol·L⁻¹
C.该温度下,加入NaOH可能引起由D向B的变化
D.B点时,降低温度,可能引起由B向C的变化
答案:
A
6. 现有下列物质:①100℃纯水;②25℃0.1mol·L⁻¹HCl溶液;③25℃0.1mol·L⁻¹KOH溶液;④25℃0.1mol·L⁻¹Ba(OH)₂溶液。
(1) 这些物质与25℃纯水相比,能促进水的电离的是
(2) 从②和③溶液中水的电离程度相等,进而可推出的结论是:同一温度下,
(1) 这些物质与25℃纯水相比,能促进水的电离的是
①
(填序号,下同),能抑制水的电离的是②③④
,水电离的c(OH⁻)等于溶液中c(OH⁻)的是①②
,水电离的c(H⁺)等于溶液中c(H⁺)的是①③④
。(2) 从②和③溶液中水的电离程度相等,进而可推出的结论是:同一温度下,
酸溶液中的$c(\mathrm{H^+})$等于碱溶液中的$c(\mathrm{OH^-})$
时,水的电离程度相等。
答案:
(1)① ②③④ ①② ①③④
(2)酸溶液中的$c(\mathrm{H^+})$等于碱溶液中的$c(\mathrm{OH^-})$
(1)① ②③④ ①② ①③④
(2)酸溶液中的$c(\mathrm{H^+})$等于碱溶液中的$c(\mathrm{OH^-})$
查看更多完整答案,请扫码查看


