2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
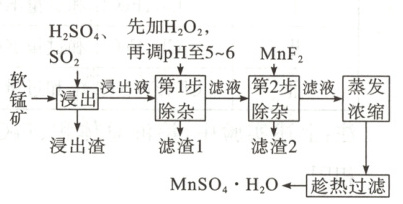
17. (10 分)软锰矿的主要成分为 $MnO_{2}$,还含有 $Fe_{2}O_{3}$、$MgO$、$Al_{2}O_{3}$、$CaO$、$SiO_{2}$ 等杂质,工业上用软锰矿制取 $MnSO_{4}· H_{2}O$ 的流程如图所示。
已知:部分金属阳离子完全沉淀时的 pH 如下表。

(1)“浸出”过程中 $MnO_{2}$ 转化为 $Mn^{2+}$ 的离子方程式为
(2)第 1 步除杂中形成滤渣 1 的主要成分为
a. $CaO$
b. $MgO$
c. $Al_{2}O_{3}$
d. 氨水
(3)第 2 步除杂,主要是将 $Ca^{2+}$、$Mg^{2+}$ 转化为相应氟化物沉淀除去,写出 $MnF_{2}$ 除去 $Mg^{2+}$ 的离子方程式:_,该反应的平衡常数为__________(结果保留一位小数)(已知:$MnF_{2}$ 的 $K_{sp}=5.3×10^{-3}$;$CaF_{2}$ 的 $K_{sp}=1.5×10^{-10}$;$MgF_{2}$ 的 $K_{sp}=7.4×10^{-11}$)。
(4)取少量 $MnSO_{4}· H_{2}O$ 溶于水,配成溶液,测其 pH 发现该溶液显酸性,原因是_(用离子方程式表示)。
已知:部分金属阳离子完全沉淀时的 pH 如下表。

(1)“浸出”过程中 $MnO_{2}$ 转化为 $Mn^{2+}$ 的离子方程式为
$\mathrm{MnO_2}+\mathrm{SO_2}\longrightarrow\mathrm{SO_4^{2-}}+\mathrm{Mn^{2+}}$
。(2)第 1 步除杂中形成滤渣 1 的主要成分为
$\mathrm{Al(OH)_3}$、$\mathrm{Fe(OH)_3}$
(填化学式),调 pH 至 5~6 所加的试剂,可选择ab
(填字母)。a. $CaO$
b. $MgO$
c. $Al_{2}O_{3}$
d. 氨水
(3)第 2 步除杂,主要是将 $Ca^{2+}$、$Mg^{2+}$ 转化为相应氟化物沉淀除去,写出 $MnF_{2}$ 除去 $Mg^{2+}$ 的离子方程式:_,该反应的平衡常数为__________(结果保留一位小数)(已知:$MnF_{2}$ 的 $K_{sp}=5.3×10^{-3}$;$CaF_{2}$ 的 $K_{sp}=1.5×10^{-10}$;$MgF_{2}$ 的 $K_{sp}=7.4×10^{-11}$)。
(4)取少量 $MnSO_{4}· H_{2}O$ 溶于水,配成溶液,测其 pH 发现该溶液显酸性,原因是_(用离子方程式表示)。

答案:
17.答案
(1)$\mathrm{MnO_2}+\mathrm{SO_2}\longrightarrow\mathrm{SO_4^{2-}}+\mathrm{Mn^{2+}}$
(2)$\mathrm{Al(OH)_3}$、$\mathrm{Fe(OH)_3}$ ab
(3)$\mathrm{MnF_2(s)}+\mathrm{Mg^{2+}(aq)}\rightleftharpoons\mathrm{Mn^{2+}(aq)}+\mathrm{MgF_2(s)}$;$K=\frac{c(\mathrm{Mn^{2+}})}{c(\mathrm{Mg^{2+}})}=\frac{c(\mathrm{Mn^{2+}})· c^2(\mathrm{F^-})}{c(\mathrm{Mg^{2+}})· c^2(\mathrm{F^-})}=\frac{K_{sp}(\mathrm{MnF_2})}{K_{sp}(\mathrm{MgF_2})}=\frac{5.3×10^{-3}}{7.4×10^{-11}}\approx7.2×10^7$。
(4)$\mathrm{MnSO_4}$是强酸弱碱盐,水解使溶液呈酸性,离子方程式为$\mathrm{Mn^{2+}}+2\mathrm{H_2O}\rightleftharpoons\mathrm{Mn(OH)_2}+2\mathrm{H^+}$。
(1)$\mathrm{MnO_2}+\mathrm{SO_2}\longrightarrow\mathrm{SO_4^{2-}}+\mathrm{Mn^{2+}}$
(2)$\mathrm{Al(OH)_3}$、$\mathrm{Fe(OH)_3}$ ab
(3)$\mathrm{MnF_2(s)}+\mathrm{Mg^{2+}(aq)}\rightleftharpoons\mathrm{Mn^{2+}(aq)}+\mathrm{MgF_2(s)}$;$K=\frac{c(\mathrm{Mn^{2+}})}{c(\mathrm{Mg^{2+}})}=\frac{c(\mathrm{Mn^{2+}})· c^2(\mathrm{F^-})}{c(\mathrm{Mg^{2+}})· c^2(\mathrm{F^-})}=\frac{K_{sp}(\mathrm{MnF_2})}{K_{sp}(\mathrm{MgF_2})}=\frac{5.3×10^{-3}}{7.4×10^{-11}}\approx7.2×10^7$。
(4)$\mathrm{MnSO_4}$是强酸弱碱盐,水解使溶液呈酸性,离子方程式为$\mathrm{Mn^{2+}}+2\mathrm{H_2O}\rightleftharpoons\mathrm{Mn(OH)_2}+2\mathrm{H^+}$。
18. (10 分)乙二酸俗称草酸,下面是化学学习小组的同学对草酸晶体 $(H_{2}C_{2}O_{4}· xH_{2}O)$ 进行的探究性学习过程,请你参与并协助他们完成相关学习任务。该组同学的研究课题是测定草酸晶体 $(H_{2}C_{2}O_{4}· xH_{2}O)$ 中的 $x$ 值。通过查阅资料得,草酸易溶于水,其水溶液可以用酸性 $KMnO_{4}$ 溶液进行滴定:$2MnO_{4}^{-}+5H_{2}C_{2}O_{4}+6H^{+}=2Mn^{2+}+10CO_{2}\uparrow +8H_{2}O$。学习小组的同学设计了如下实验步骤测定 $x$ 值。
①称取 $1.260\ g$ 纯草酸晶体,将其配成 $100.00\ mL$ 溶液作为待测液;
②取 $25.00\ mL$ 待测液放入锥形瓶中,再加入适量的稀硫酸;
③用浓度为 $0.1000\ mol· L^{-1}$ 的酸性 $KMnO_{4}$ 标准溶液进行滴定,达到终点时消耗标准液 $10.00\ mL$。
请回答下列问题。

(1)滴定时,将酸性 $KMnO_{4}$ 标准溶液装在图中的
(2)本实验滴定达到终点的标志是
(3)通过上述数据,求得 $x =$
①若滴定至终点时俯视滴定管读数,则由此测得的 $x$ 值会
②若滴定时所用的酸性 $KMnO_{4}$ 溶液因久置而导致浓度变小,则由此测得的 $x$ 值会
①称取 $1.260\ g$ 纯草酸晶体,将其配成 $100.00\ mL$ 溶液作为待测液;
②取 $25.00\ mL$ 待测液放入锥形瓶中,再加入适量的稀硫酸;
③用浓度为 $0.1000\ mol· L^{-1}$ 的酸性 $KMnO_{4}$ 标准溶液进行滴定,达到终点时消耗标准液 $10.00\ mL$。
请回答下列问题。

(1)滴定时,将酸性 $KMnO_{4}$ 标准溶液装在图中的
甲
(填“甲”或“乙”)滴定管中。(2)本实验滴定达到终点的标志是
当滴入最后半滴酸性$\mathrm{KMnO_4}$标准溶液时,溶液由无色变为紫红色,且半分钟内不褪色
。(3)通过上述数据,求得 $x =$
2
。①若滴定至终点时俯视滴定管读数,则由此测得的 $x$ 值会
偏大
(填“偏大”“偏小”或“不变”,下同)。②若滴定时所用的酸性 $KMnO_{4}$ 溶液因久置而导致浓度变小,则由此测得的 $x$ 值会
偏小
。
答案:
18.答案
(1)甲
(2)当滴入最后半滴酸性$\mathrm{KMnO_4}$标准溶液时,溶液由无色变为紫红色,且半分钟内不褪色
(3)2 ①偏大 ②偏小
解析
(3)由题给离子方程式及数据可知,$1.260\ \mathrm{g}$纯草酸晶体中所含$\mathrm{H_2C_2O_4}$的物质的量为$0.1000\ \mathrm{mol· L^{-1}}×10.00\ \mathrm{mL}×10^{-3}\ \mathrm{L· mL^{-1}}×\frac{5}{2}×\frac{100.00\ \mathrm{mL}}{25.00\ \mathrm{mL}}=0.0100\ \mathrm{mol}$,则$1.260\ \mathrm{g\ H_2C_2O_4· xH_2O}$中所含$\mathrm{H_2O}$的物质的量为$\frac{1.260\ \mathrm{g}-0.0100\ \mathrm{mol}×90\ \mathrm{g· mol^{-1}}}{18\ \mathrm{g· mol^{-1}}}=0.0200\ \mathrm{mol}$,则$x=2$。①若滴定至终点时俯视滴定管读数,则所测得的消耗的酸性$\mathrm{KMnO_4}$标准溶液的体积偏小,测得的$n(\mathrm{H_2C_2O_4})$偏小,则$n(\mathrm{H_2O})$偏大,$x$值偏大。②若酸性$\mathrm{KMnO_4}$溶液浓度偏小,则消耗的体积偏大,测得的$x$值偏小。
(1)甲
(2)当滴入最后半滴酸性$\mathrm{KMnO_4}$标准溶液时,溶液由无色变为紫红色,且半分钟内不褪色
(3)2 ①偏大 ②偏小
解析
(3)由题给离子方程式及数据可知,$1.260\ \mathrm{g}$纯草酸晶体中所含$\mathrm{H_2C_2O_4}$的物质的量为$0.1000\ \mathrm{mol· L^{-1}}×10.00\ \mathrm{mL}×10^{-3}\ \mathrm{L· mL^{-1}}×\frac{5}{2}×\frac{100.00\ \mathrm{mL}}{25.00\ \mathrm{mL}}=0.0100\ \mathrm{mol}$,则$1.260\ \mathrm{g\ H_2C_2O_4· xH_2O}$中所含$\mathrm{H_2O}$的物质的量为$\frac{1.260\ \mathrm{g}-0.0100\ \mathrm{mol}×90\ \mathrm{g· mol^{-1}}}{18\ \mathrm{g· mol^{-1}}}=0.0200\ \mathrm{mol}$,则$x=2$。①若滴定至终点时俯视滴定管读数,则所测得的消耗的酸性$\mathrm{KMnO_4}$标准溶液的体积偏小,测得的$n(\mathrm{H_2C_2O_4})$偏小,则$n(\mathrm{H_2O})$偏大,$x$值偏大。②若酸性$\mathrm{KMnO_4}$溶液浓度偏小,则消耗的体积偏大,测得的$x$值偏小。
查看更多完整答案,请扫码查看


