2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第25页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
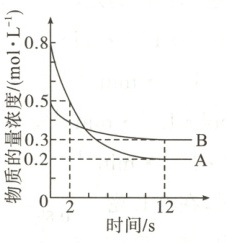
【例1】某温度下,在2 L密闭容器中投入一定量的A、B发生反应:$3A(g)+bB(g)\rightleftharpoons cC(g)$ $\Delta H=-QkJ· mol^{-1}$($Q>0$)。12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是(
A.前12 s内,A的平均反应速率为$0.025mol· L^{-1}· s^{-1}$
B.前12 s内,C的平均反应速率为$0.05mol· L^{-1}· s^{-1}$
C.化学计量数之比$b:c=1:2$
D.12 s内,A与B反应放出的热量为$0.2QkJ$
C
)。
A.前12 s内,A的平均反应速率为$0.025mol· L^{-1}· s^{-1}$
B.前12 s内,C的平均反应速率为$0.05mol· L^{-1}· s^{-1}$
C.化学计量数之比$b:c=1:2$
D.12 s内,A与B反应放出的热量为$0.2QkJ$
答案:
【例1】C 解析 由图像分析可知,前12s内A的浓度变化为$\Delta c(A)=0.2\ mol · L^{-1} - 0.8\ mol · L^{-1} = -0.6\ mol · L^{-1}$,反应速率$v(A)=-\frac{\Delta c(A)}{\Delta t} = \frac{0.6\ mol · L^{-1}}{12\ s} = 0.05\ mol · L^{-1} · s^{-1}$,A项错误。前12s内B的浓度变化为$\Delta c(B)=0.3\ mol · L^{-1} - 0.5\ mol · L^{-1} = -0.2\ mol · L^{-1}$,反应速率$v(B)=-\frac{\Delta c(B)}{\Delta t} = \frac{0.2\ mol · L^{-1}}{12\ s} = \frac{1}{60}\ mol · L^{-1} · s^{-1}$,依据题意$v(C)=\frac{\Delta n(C)}{\Delta t} = \frac{\frac{\Delta n(C)}{2\ L}}{12\ s} = \frac{1}{30}\ mol · L^{-1} · s^{-1}$,速率之比等于化学计量数之比,则$3:b:c = 0.05:\frac{1}{60}:\frac{1}{30}$,$b = 1$,$c = 2$,$b:c = 1:2$,C项正确,B项错误。3mol A完全反应放热QkJ,12s内A反应的物质的量为$(0.8\ mol · L^{-1} - 0.2\ mol · L^{-1}) × 2\ L = 1.2\ mol$,则1.2mol A反应放出热量0.4QkJ,D项错误。
【例2】关于$A(g)+2B(g)\xlongequal{}3C(g)$的化学反应,下列表示的反应速率最大的是(
A.$v(A)=0.6mol· L^{-1}· min^{-1}$
B.$v(B)=1.2mol· L^{-1}· min^{-1}$
C.$v(C)=1.2mol· L^{-1}· min^{-1}$
D.$v(B)=0.03mol· L^{-1}· s^{-1}$
D
)。A.$v(A)=0.6mol· L^{-1}· min^{-1}$
B.$v(B)=1.2mol· L^{-1}· min^{-1}$
C.$v(C)=1.2mol· L^{-1}· min^{-1}$
D.$v(B)=0.03mol· L^{-1}· s^{-1}$
答案:
【例2】D 解析 A项,$v(A)=0.6\ mol · L^{-1} · min^{-1}$;B项,$v(B)=1.2\ mol · L^{-1} · min^{-1}$,转化成用A表示的速率为$1.2\ mol · L^{-1} · min^{-1} ÷ 2 = 0.6\ mol · L^{-1} · min^{-1}$;C项,$v(C)=1.2\ mol · L^{-1} · min^{-1}$,转化成用A表示的速率为$1.2\ mol · L^{-1} · min^{-1} ÷ 3 = 0.4\ mol · L^{-1} · min^{-1}$;D项,$v(B)=0.03\ mol · L^{-1} · s^{-1}$,先统一单位$v(B)=0.03\ mol · L^{-1} · s^{-1} × 60\ s · min^{-1} = 1.8\ mol · L^{-1} · min^{-1}$,再转化成用A表示的速率为$1.8\ mol · L^{-1} · min^{-1} ÷ 2 = 0.9\ mol · L^{-1} · min^{-1}$。故选D项。
【对点训练1】反应$4A(s)+3B(g)\rightleftharpoons 2C(g)+D(g)$,经2 min,B的浓度减少了$0.6mol· L^{-1}$。对此反应速率的正确表示是(
A.用A表示的反应速率是$0.4mol· L^{-1}· min^{-1}$
B.用B表示的反应速率是$0.3mol· L^{-1}· min^{-1}$
C.2 min末时的反应速率用B表示是$0.3mol· L^{-1}· min^{-1}$
D.在这2 min内用B表示的反应速率的值是减小的,用C表示的反应速率的值逐渐增大
B
)。A.用A表示的反应速率是$0.4mol· L^{-1}· min^{-1}$
B.用B表示的反应速率是$0.3mol· L^{-1}· min^{-1}$
C.2 min末时的反应速率用B表示是$0.3mol· L^{-1}· min^{-1}$
D.在这2 min内用B表示的反应速率的值是减小的,用C表示的反应速率的值逐渐增大
答案:
【对点训练1】B 解析 A是固体,不能用A的浓度变化表示反应速率,故A项不正确;在这2min内用B表示的平均反应速率是$0.3\ mol · L^{-1} · min^{-1}$,但2min末的反应速率小于$0.3\ mol · L^{-1} · min^{-1}$,故B项正确,C项不正确;$v(B):v(C)=3:2$,随反应的进行,B的浓度减小,反应速率逐渐减小,单位时间内生成的C也逐渐减少,故D项不正确。
【对点训练2】反应$A(g)+3B(g)\rightleftharpoons 2C(g)+2D(g)$在四种不同情况下的反应速率分别为
①$v(A)=0.15mol· L^{-1}· s^{-1}$
②$v(B)=0.6mol· L^{-1}· s^{-1}$
③$v(C)=0.4mol· L^{-1}· s^{-1}$
④$v(D)=0.45mol· L^{-1}· s^{-1}$
该
A.④>②=③>①
B.④>②>③>①
C.①>②=③>④
D.①>②>③>④
①$v(A)=0.15mol· L^{-1}· s^{-1}$
②$v(B)=0.6mol· L^{-1}· s^{-1}$
③$v(C)=0.4mol· L^{-1}· s^{-1}$
④$v(D)=0.45mol· L^{-1}· s^{-1}$
该
反
应进行的快慢顺序为(A
)。A.④>②=③>①
B.④>②>③>①
C.①>②=③>④
D.①>②>③>④
答案:
【对点训练2】A 解析 将各项换算成用A表示的反应速率分别为①$0.15\ mol · L^{-1} · s^{-1}$、②$0.2\ mol · L^{-1} · s^{-1}$、③$0.2\ mol · L^{-1} · s^{-1}$、④$0.225\ mol · L^{-1} · s^{-1}$,故④>②=③>①。
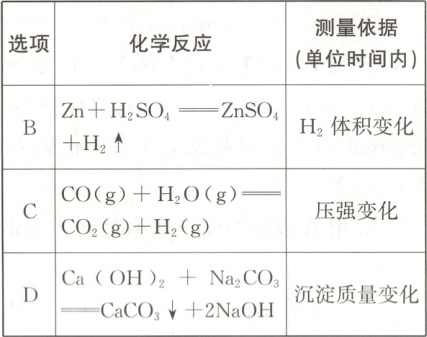
1. 下列化学反应速率的测量中,测量依据不可行的是(

C
)。

答案:
1.C 解析 该反应是气体体积不变的反应,反应前后压强不变,C项错误。
查看更多完整答案,请扫码查看


