2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
12. $CH_{4}$与$CO_{2}$的干法重整$(DRM)$反应为$CH_{4}(g) + CO_{2}(g)\rightleftharpoons 2CO(g) + 2H_{2}(g)$。向容积为$1 L$的恒容密闭容器中通入$CH_{4}(g)$和$CO_{2}(g)$各$1.0 mol$,在不同温度$T_{1}$、$T_{2}$下测得$n(H_{2})$随时间变化的曲线如图。下列说法错误的是(
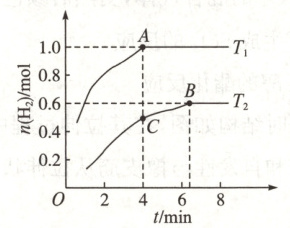
A.该反应是吸热反应
B.$A$、$B$点化学平衡常数:$K(A) < K(B)$
C.$T_{2}$时,$CO_{2}$的平衡转化率是$30\%$
D.化学反应速率:$v_{逆}(B) > v_{正}(C)$
BD
)。
A.该反应是吸热反应
B.$A$、$B$点化学平衡常数:$K(A) < K(B)$
C.$T_{2}$时,$CO_{2}$的平衡转化率是$30\%$
D.化学反应速率:$v_{逆}(B) > v_{正}(C)$
答案:
12. BD 解析 其他条件相同时,温度越高化学反应速率越大,反应先达到平衡状态,装置中氢气的物质的量不再发生变化,所以温度 T₁>T₂,由于平衡时 T₂ 下产生的氢气更多,则该反应是吸热反应,A 项正确;化学平衡常数只与温度有关,升高温度平衡向吸热反应方向,即正向移动,化学平衡常数增大,A、B 点平衡常数:K(A)>K(B),B项错误;T₂ 时列出三段式,
CH₄(g)+CO₂(g)⇌2CO(g)+2H₂(g)
起始/mol 1.0 1.0 0 0
转化/mol 0.3 0.3 0.6 0.6
平衡/mol 0.7 0.7 0.6 0.6
CO₂ 的平衡转化率是0.3/1.0×100%=30%,C项正确;C 点反应正向进行,正反应速率大于逆反应速率,随着反应进行,正反应速率减小,逆反应速率增大,直到正、逆反应速率相等,所以化学反应速率:vₑ(B)<vₐ(C),D项错误。
CH₄(g)+CO₂(g)⇌2CO(g)+2H₂(g)
起始/mol 1.0 1.0 0 0
转化/mol 0.3 0.3 0.6 0.6
平衡/mol 0.7 0.7 0.6 0.6
CO₂ 的平衡转化率是0.3/1.0×100%=30%,C项正确;C 点反应正向进行,正反应速率大于逆反应速率,随着反应进行,正反应速率减小,逆反应速率增大,直到正、逆反应速率相等,所以化学反应速率:vₑ(B)<vₐ(C),D项错误。
13. 一定温度下,在三个容积均为$1 L$的恒容密闭容器中发生反应:$2CH_{3}OH(g)\rightleftharpoons CH_{3}OCH_{3}(g) + H_{2}O(g)$。

下列说法正确的是(
A.该反应的正反应为放热反应
B.达到平衡时,容器①中的$CH_{3}OH$体积分数比容器②中的小
C.若容器①中反应达到平衡后,缩小容器容积,$\frac{c(CH_{3}OH)}{c(CH_{3}OCH_{3})}$不变
D.若起始向容器①中充入$0.10 mol CH_{3}OH$、$0.10 mol CH_{3}OCH_{3}$、$0.10 mol H_{2}O$,反应将向逆反应方向进行

下列说法正确的是(
AC
)。A.该反应的正反应为放热反应
B.达到平衡时,容器①中的$CH_{3}OH$体积分数比容器②中的小
C.若容器①中反应达到平衡后,缩小容器容积,$\frac{c(CH_{3}OH)}{c(CH_{3}OCH_{3})}$不变
D.若起始向容器①中充入$0.10 mol CH_{3}OH$、$0.10 mol CH_{3}OCH_{3}$、$0.10 mol H_{2}O$,反应将向逆反应方向进行
答案:
13. AC 解析 对比①③数据可知,当其他条件不变时,升高温度,平衡时生成物的物质的量减少,说明升高温度平衡逆向移动,则正反应为放热反应,A项正确;恒容条件下,①②温度相同,由于反应前后气体的总分子数不变,增大反应物浓度相当于增大压强,平衡不移动,因此平衡时容器①中的 CH₃OH 体积分数与容器②中的相等,B项错误;该反应为气体分子数不变的反应,若容器①中反应达到平衡后,缩小容器容积,压强增大,平衡不移动,且容器容积减小,各物质的浓度同比例增大,则c(CH₃OH)/c(CH₃OCH₃)不变,C项正确;容器①平衡时,c(CH₃OH)=0.20 mol·L⁻¹−2×0.08 mol·L⁻¹=0.04 mol·L⁻¹,c(CH₃OCH₃)=0.08 mol·L⁻¹,c(H₂O)=0.08 mol·L⁻¹,平衡常数为 K=c(H₂O)·c(CH₃OCH₃)/c²(CH₃OH)=0.08×0.08/0.04²=4,若起始向容器①中充入 0.10 mol CH₃OH、0.10 mol CH₃OCH₃、0.10 mol H₂O,浓度商为 Q=c(H₂O)·c(CH₃OCH₃)/c²(CH₃OH)=0.10×0.10/0.10²=1<K=4,平衡向正反应方向移动,D项错误。
14. 研究表明,用可控$Cu/Cu_{2}O$界面材料可催化$CO_{2}$还原合成甲醇:$CO_{2}(g) + 3H_{2}(g)\rightleftharpoons CH_{3}OH(g) + H_{2}O(g)$ $\Delta H < 0$。将$6 mol CO_{2}$和$8 mol H_{2}$充入容积为$2 L$的恒温恒容密闭容器中发生该反应,测得起始压强为$35 MPa$,$H_{2}$的物质的量随时间的变化如图中实线所示。下列说法正确的是(
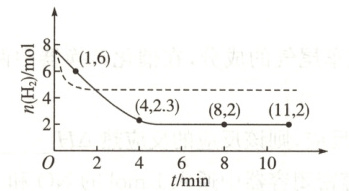
A.$1\sim 4 min$(实线)内,$v(CO_{2})$约为$0.62 mol· L^{-1}· min^{-1}$
B.该条件下的实线对应的$K_{p}$为$0.02 MPa^{-2}$
C.要变成虚线,可能的条件是升高温度或加入催化剂
D.当气体的平均摩尔质量或密度一定时,化学反应达平衡状态
B
)。
A.$1\sim 4 min$(实线)内,$v(CO_{2})$约为$0.62 mol· L^{-1}· min^{-1}$
B.该条件下的实线对应的$K_{p}$为$0.02 MPa^{-2}$
C.要变成虚线,可能的条件是升高温度或加入催化剂
D.当气体的平均摩尔质量或密度一定时,化学反应达平衡状态
答案:
14. B
查看更多完整答案,请扫码查看


