2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版B山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第117页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
5. (双选)已知锌及其化合物的性质与铝及其化合物的性质相似。如图,横坐标为溶液的pH,纵坐标为Zn²⁺或[Zn(OH)₄]²⁻物质的量浓度的对数(假设Zn²⁺浓度为1×10⁻⁵mol·L⁻¹时,Zn²⁺已沉淀完全)。下列说法不正确的是(
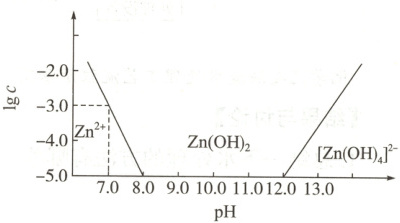
A.往ZnCl₂溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为Zn²⁺+4OH⁻=[Zn(OH)₄]²⁻
B.从图中数据计算可得Zn(OH)₂的溶度积K_sp=1×10⁻¹⁸
C.某废液中含Zn²⁺,沉淀Zn²⁺可以控制溶液pH的范围是8.0~12.0
D.向1L1mol·L⁻¹ZnCl₂溶液中加入NaOH固体至pH=6.0,需NaOH0.2mol
B D
)。
A.往ZnCl₂溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为Zn²⁺+4OH⁻=[Zn(OH)₄]²⁻
B.从图中数据计算可得Zn(OH)₂的溶度积K_sp=1×10⁻¹⁸
C.某废液中含Zn²⁺,沉淀Zn²⁺可以控制溶液pH的范围是8.0~12.0
D.向1L1mol·L⁻¹ZnCl₂溶液中加入NaOH固体至pH=6.0,需NaOH0.2mol
答案:
BD 解析A项,当溶液pH>12.0时,$Zn^{2+}$转化成 $[Zn(OH)_4]^{2-}$,正确。B项,依据pH=7时,$c(Zn^{2+}) = 1 ×$ $10^{-3}\ mol · L^{-1}$计算,此时有沉淀溶解平衡存在,$K_sp = 1 ×$ $10^{-3} × (1 × 10^{-7})^2 = 1 × 10^{-17}$,不正确。C项,当$c(Zn^{2+}) = 1 ×$ $10^{-5}\ mol · L^{-1}$时认为废液中$Zn^{2+}$已完全沉淀,所以控制 pH在8.0~12.0范围内可将$Zn^{2+}$沉淀完全,正确。D项, 当pH=6.0,即$c(OH^-) = 1 × 10^{-8}\ mol · L^{-1}$时,由$K_sp$ 可知此时$c(Zn^{2+}) = 1 × 10^{-1}\ mol · L^{-1}$,即有 0.9 mol $Zn^{2+}$转化为$Zn(OH)_2$,需$NaOH$为1.8 mol,不 正确。
6. 氯化铜晶体(CuCl₂·xH₂O)是重要的化工原料,可用作反应的催化剂、消毒剂等。由孔雀石[主要含Cu₂(OH)₂CO₃,还含少量FeCO₃、SiO₂]制备氯化铜晶体的方案如下。
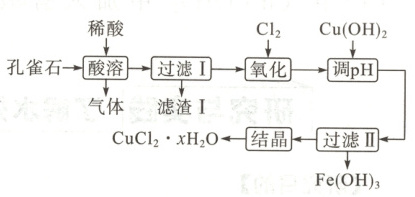
下列有关说法不正确的是(
A.酸溶时适当升高温度并不断搅拌,有利于提高铜的浸取率
B.滤渣Ⅰ为SiO₂
C.一定温度下,已知K_sp[Fe(OH)₃]=4.0×10⁻³⁸,欲使调pH后溶液中c(Fe³⁺)≤4.0×10⁻⁵mol·L⁻¹,必须控制溶液pH≥3
D.在坩埚中加热CuCl₂·xH₂O晶体可得到纯净的无水CuCl₂

下列有关说法不正确的是(
D
)。A.酸溶时适当升高温度并不断搅拌,有利于提高铜的浸取率
B.滤渣Ⅰ为SiO₂
C.一定温度下,已知K_sp[Fe(OH)₃]=4.0×10⁻³⁸,欲使调pH后溶液中c(Fe³⁺)≤4.0×10⁻⁵mol·L⁻¹,必须控制溶液pH≥3
D.在坩埚中加热CuCl₂·xH₂O晶体可得到纯净的无水CuCl₂
答案:
D 解析孔雀石加入稀酸进行酸浸,根据孔雀石的 成分可知产生的气体为$CO_2$,过滤得到的滤渣Ⅰ为难溶物 $SiO_2$,滤液中含有$Cu^{2+}$、$Fe^{2+}$等,通入氯气将$Fe^{2+}$氧化为 $Fe^{3+}$,为了不引入新的杂质,加入$Cu(OH)_2$调节pH,过滤 得到$Fe(OH)_3$沉淀,结晶得到$CuCl_2 · xH_2O$。酸溶时适 当升高温度并不断搅拌,可以加快反应速率,并使反应充 分进行,有利于提高铜的浸取率,A项正确;当$c(Fe^{3+}) =$ $4.0 × 10^{-5}\ mol · L^{-1}$时,溶液中$c(OH^-) = \sqrt[3]{\frac{4.0 × 10^{-38}}{4.0 × 10^{-5}}}$ $mol · L^{-1} = 1.0 × 10^{-11}\ mol · L^{-1}$,则此时溶液中$c(H^+) =$ $1.0 × 10^{-3}\ mol · L^{-1}$,所以需要控制溶液pH≥3,C项正 确;加热$CuCl_2 · xH_2O$晶体时会促进$Cu^{2+}$的水解,HCl 挥发,会有$Cu(OH)_2$生成,$Cu(OH)_2$受热分解生成$CuO$, 所以最终得到的固体为$CuO$,D项错误。
7. 工业上制取CuCl₂的工艺流程如下。
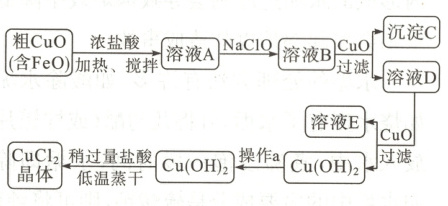
请结合下表数据,回答问题。
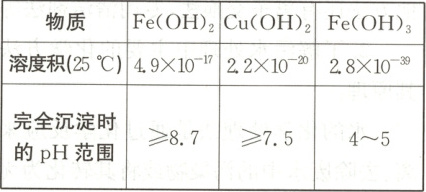
(1) 在溶液A中加入NaClO的目的是_。
(2) 在溶液B中加入CuO的作用是_。
(3) 操作a的目的是_。
(4) 在Cu(OH)₂中加入盐酸使Cu(OH)₂转化为CuCl₂,采用稍过量盐酸和低温蒸干的目的是_。

请结合下表数据,回答问题。

(1) 在溶液A中加入NaClO的目的是_。
将Fe²⁺氧化为Fe³⁺,使后续分离更加完全
(2) 在溶液B中加入CuO的作用是_。
调节溶液的pH为4~5,使Fe³⁺完全转化为Fe(OH)₃沉淀
(3) 操作a的目的是_。
洗涤Cu(OH)₂表面的可溶性杂质
(4) 在Cu(OH)₂中加入盐酸使Cu(OH)₂转化为CuCl₂,采用稍过量盐酸和低温蒸干的目的是_。
抑制Cu²⁺的水解
答案:
6. 答案
(1)将$Fe^{2+}$氧化为$Fe^{3+}$,使后续分离更加完全
(2)调节溶液的pH为4~5,使$Fe^{3+}$完全转化为 $Fe(OH)_3$沉淀
(3)洗涤$Cu(OH)_2$表面的可溶性杂质
(4)抑制$Cu^{2+}$的水解
(1)将$Fe^{2+}$氧化为$Fe^{3+}$,使后续分离更加完全
(2)调节溶液的pH为4~5,使$Fe^{3+}$完全转化为 $Fe(OH)_3$沉淀
(3)洗涤$Cu(OH)_2$表面的可溶性杂质
(4)抑制$Cu^{2+}$的水解
查看更多完整答案,请扫码查看


