2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版A山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版A山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第47页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
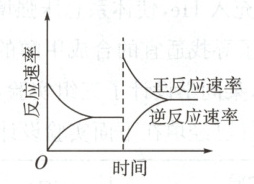
5. 如图是关于反应$A_2(g) + 3B_2(g) \rightleftharpoons 2C(g)$ $\Delta H < 0$的平衡移动图像,影响平衡移动的原因可能是(
A.升高温度,同时增大压强
B.降低温度,同时减小压强
C.增大$A_2$的浓度,同时减小C的浓度
D.增大$B_2$的浓度,同时使用催化剂
C
)。
A.升高温度,同时增大压强
B.降低温度,同时减小压强
C.增大$A_2$的浓度,同时减小C的浓度
D.增大$B_2$的浓度,同时使用催化剂
答案:
5.C 解析 升高温度和增大压强会使正、逆反应速率都增大,A项错误;降低温度和减小压强会使正、逆反应速率都减小,B项错误;增大反应物浓度和使用催化剂会使正、逆反应速率都增大,D项错误。
6. 一密封体系中发生下列反应:$N_2(g) + 3H_2(g) \rightleftharpoons 2NH_3(g)$ $\Delta H < 0$,下图是某一时间段中反应速率与反应进程的曲线关系图:
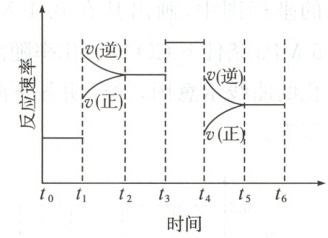
回答下列问题。
(1)处于平衡状态的时间段是、、。
(2)$t_1$、$t_3$、$t_4$时刻体系中分别是什么条件发生了变化:____、____、____。
(3)下列各时间段时,氨的含量最高的是。
A. $t_0 \sim t_1$
B. $t_2 \sim t_3$
C. $t_3 \sim t_4$
D. $t_5 \sim t_6$

回答下列问题。
(1)处于平衡状态的时间段是、、。
(2)$t_1$、$t_3$、$t_4$时刻体系中分别是什么条件发生了变化:____、____、____。
(3)下列各时间段时,氨的含量最高的是。
A. $t_0 \sim t_1$
B. $t_2 \sim t_3$
C. $t_3 \sim t_4$
D. $t_5 \sim t_6$
答案:
6.答案
(1)t₀~t₁ t₂~t₄ t₅~t₆
(2)升高温度 加催化剂 减小压强
(3)A
解析
(1)处于平衡状态时,正、逆反应速率必定相等,从图中可看出,t₀~t₁、t₂~t₄、t₅~t₆时间段时反应处于平衡状态。
(2)t₁时刻,条件变化使v(正)、v(逆)都增大,且v(逆)>v(正),平衡向逆反应方向移动,对照化学方程式可看出条件变化应是升高温度。t₃时刻,v(正)、v(逆)都同幅度增大,应是加催化剂。t₄时刻,v(正)、v(逆)都减小,且v(正)<v(逆),平衡逆移,所以是由减小压强引起的。
(3)由于t₁~t₂时间段和t₄~t₅时间段中,平衡都向逆反应方向移动,氨含量都减小,所以应是t₀~t₁时间段中氨含量最高。
(1)t₀~t₁ t₂~t₄ t₅~t₆
(2)升高温度 加催化剂 减小压强
(3)A
解析
(1)处于平衡状态时,正、逆反应速率必定相等,从图中可看出,t₀~t₁、t₂~t₄、t₅~t₆时间段时反应处于平衡状态。
(2)t₁时刻,条件变化使v(正)、v(逆)都增大,且v(逆)>v(正),平衡向逆反应方向移动,对照化学方程式可看出条件变化应是升高温度。t₃时刻,v(正)、v(逆)都同幅度增大,应是加催化剂。t₄时刻,v(正)、v(逆)都减小,且v(正)<v(逆),平衡逆移,所以是由减小压强引起的。
(3)由于t₁~t₂时间段和t₄~t₅时间段中,平衡都向逆反应方向移动,氨含量都减小,所以应是t₀~t₁时间段中氨含量最高。
1. 在一个不导热的密闭反应器中,只发生两个反应:①$a(g) + b(g) \rightleftharpoons 2c(g)$ $\Delta H_1 < 0$,②$x(g) + 3y(g) \rightleftharpoons 2z(g)$ $\Delta H_2 > 0$。进行相关操作且达到平衡后,下列叙述错误的是(
A.等压时,通入稀有气体,c的物质的量不变
B.等压时,通入z气体,反应器中温度升高
C.等容时,通入稀有气体,各反应速率不变
D.等容时,通入x气体,a的物质的量浓度减小
A
)。A.等压时,通入稀有气体,c的物质的量不变
B.等压时,通入z气体,反应器中温度升高
C.等容时,通入稀有气体,各反应速率不变
D.等容时,通入x气体,a的物质的量浓度减小
答案:
1.A 解析 等压时,通入稀有气体,相当于减小压强,平衡①不移动,平衡②逆向移动,该反应逆反应为放热反应,相当于给体系加热,平衡①逆向移动,c的物质的量减小,A项错误;等压时,通入z气体,平衡②逆向移动,反应放热,B项正确;等容时,通入稀有气体,反应体系中各气体浓度不变,各组分的反应速率不变,C项正确;等容时,通入x气体,平衡②正向移动,反应吸热,体系温度降低,平衡①正向移动,a的物质的量浓度减小,D项正确。
2. (双选)在一定条件下,$CH_4$与$H_2O(g)$发生反应:$CH_4(g) + H_2O(g) \rightleftharpoons CO(g) + 3H_2(g)$。设起始$\frac{n(H_2O)}{n(CH_4)} = Z$,在恒压下,平衡时$CH_4$的体积分数$\varphi(CH_4)$与$Z$和$T$(温度)的关系如图所示。下列说法正确的是(
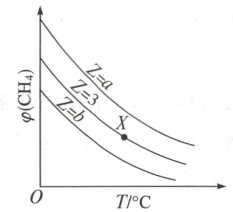
A.该反应的焓变$\Delta H > 0$
B.图中$Z$的大小为$a > 3 > b$
C.图中$X$点对应平衡混合物中$\frac{n(H_2O)}{n(CH_4)} = 3$
D.温度不变时,图中$X$点对应的平衡在加压后$\varphi(CH_4)$增大
AD
)。
A.该反应的焓变$\Delta H > 0$
B.图中$Z$的大小为$a > 3 > b$
C.图中$X$点对应平衡混合物中$\frac{n(H_2O)}{n(CH_4)} = 3$
D.温度不变时,图中$X$点对应的平衡在加压后$\varphi(CH_4)$增大
答案:
2.AD 解析 由图可知,随温度的升高,CH₄的体积分数减小,说明平衡向正反应方向移动,正反应为吸热反应,A项正确;Z越大,即$\frac{n(H₂O)}{n(CH₄)}$越大,相当于增加H₂O的量,平衡正向移动,CH₄的体积分数减小,所以b>3>a,B项错误;设起始时n(H₂O)=3x mol,n(CH₄)=x mol,达到平衡时消耗n(CH₄)=n(H₂O)=y mol,则平衡时$\frac{n(H₂O)}{n(CH₄)}=\frac{3x - y}{x - y}≠3$,C项错误;加压,平衡向逆反应方向移动,CH₄体积分数增大,D项正确。
查看更多完整答案,请扫码查看


