2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版A山东专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年同步练习册人民教育出版社高中化学选择性必修第一册人教版A山东专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
9. 通常把拆开$1\ mol$某化学键所吸收的能量或形成$1\ mol$某化学键所释放的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热$(\Delta H)$,化学反应的$\Delta H$等于反应物中的化学键键能之和与生成物中的化学键键能之和的差。
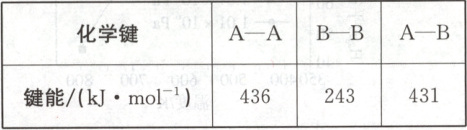
$A. \Delta H=-91.5\ kJ·mol^{-1}$
B.$A_2(g)+B_2(g)\longrightarrow2AB(g)$ $\Delta H=-183\ kJ·mol^{-1}$
$C. \Delta H=+91.5\ kJ·mol^{-1}$
$D. \Delta H=+183\ kJ·mol^{-1}$

C
)。$A. \Delta H=-91.5\ kJ·mol^{-1}$
B.$A_2(g)+B_2(g)\longrightarrow2AB(g)$ $\Delta H=-183\ kJ·mol^{-1}$
$C. \Delta H=+91.5\ kJ·mol^{-1}$
$D. \Delta H=+183\ kJ·mol^{-1}$
答案:
9.C 解析反应$A_2(g)+B_2(g)=2AB(g)$的$\Delta H=(436\ kJ· mol^{-1}+243\ kJ· mol^{-1})-2×431\ kJ· mol^{-1}=-183\ kJ· mol^{-1}$,说明$A_2(g)$与$B_2(g)$反应生成$AB(g)$是一个放热反应,由此可知A、B、D三项正确,C选项热化学方程式错误。
10. 某温度下,在一固定容积的密闭容器中,反应$aA(g)+bB(g)\longrightarrow dD(g)$达到平衡后,$A、B、D$的物质的量分别为$a\ mol、b\ mol$和$d\ mol$。已知$a+b=2d$,若保持温度不变,将三者的物质的量均增大一倍,则下列判断正确的是(
A.平衡不移动
B.混合气体的密度不变
C.B的体积分数减小
D.$a\ mol·L^{-1}<c(A)<2a\ mol·L^{-1}$
C
)。A.平衡不移动
B.混合气体的密度不变
C.B的体积分数减小
D.$a\ mol·L^{-1}<c(A)<2a\ mol·L^{-1}$
答案:
10.C 解析由$a+b=2d$知$a+b>d$,正反应是气体体积缩小的反应,恒温恒容下,将三者的物质的量增大一倍,相当于增大压强,平衡向正反应方向移动,B的体积分数减小,A项错误,C项正确;混合气体的质量增大,体积不变,则密度增大,B项错误;只能确定$a\ mol<n(A)<2a\ mol$,因容器的容积未知,不能确定$c(A)$,D项错误。
$11. $已知下列热化学方程式:
$①CH_3COOH(l)+2O_2(g)\longrightarrow2CO_2(g)+2H_2O(l) \Delta H_1=-870.3\ kJ·mol^{-1}$
$② \Delta H_2=-393.5\ kJ·mol^{-1}$
$③ \Delta H_3=-285.8\ kJ·mol^{-1}$
则反应的$\Delta H$为$($
A.$-488.3\ kJ·mol^{-1}$
B.$-244.15\ kJ·mol^{-1}$
C.$+488.3\ kJ·mol^{-1}$
D.$+244.15\ kJ·mol^{-1}$
$①CH_3COOH(l)+2O_2(g)\longrightarrow2CO_2(g)+2H_2O(l) \Delta H_1=-870.3\ kJ·mol^{-1}$
$② \Delta H_2=-393.5\ kJ·mol^{-1}$
$③ \Delta H_3=-285.8\ kJ·mol^{-1}$
则反应的$\Delta H$为$($
$A$
$)。$ A.$-488.3\ kJ·mol^{-1}$
B.$-244.15\ kJ·mol^{-1}$
C.$+488.3\ kJ·mol^{-1}$
D.$+244.15\ kJ·mol^{-1}$
答案:
11.A 解析根据盖斯定律,$③×2+②×2-①$,得$2C(s)+2H_2(g)+O_2(g)=CH_3COOH(l)$,该反应的$\Delta H=(-285.8\ kJ· mol^{-1})×2+(-393.5\ kJ· mol^{-1})×2-(-870.3\ kJ· mol^{-1})=-488.3\ kJ· mol^{-1}$。
12. 对于可逆反应:$A_2(?)+B_2(?)\longrightarrow2AB(?)$,当温度和压强改变时,$n(AB)$的变化如下图所示,下列叙述正确的是(
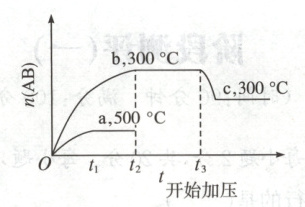
A.$A_2、B_2$及$AB$均为气体,$\Delta H<0$
B.$AB$为气体,$A_2、B_2$至少有一种为非气体,$\Delta H<0$
C.$AB$为气体,$A_2、B_2$有一种为非气体,$\Delta H>0$
D.$AB$为固体,$A_2、B_2$有一种为非气体,$\Delta H>0$
B
)。
A.$A_2、B_2$及$AB$均为气体,$\Delta H<0$
B.$AB$为气体,$A_2、B_2$至少有一种为非气体,$\Delta H<0$
C.$AB$为气体,$A_2、B_2$有一种为非气体,$\Delta H>0$
D.$AB$为固体,$A_2、B_2$有一种为非气体,$\Delta H>0$
答案:
12.B 解析由图可知压强相等时,升高温度,AB的物质的量减小,可知温度升高平衡向逆反应方向移动,逆反应是吸热反应,正反应是放热反应,$\Delta H<0$;$t_3$开始温度不变,压强增大,AB的物质的量减小,说明平衡向逆反应方向移动,逆反应是气体体积减小的方向,说明AB必为气体,$A_2$、$B_2$至少有一种为非气体,不能同时为气体。
查看更多完整答案,请扫码查看


