2026年大联考单元期末测试卷九年级化学全一册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年大联考单元期末测试卷九年级化学全一册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第53页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
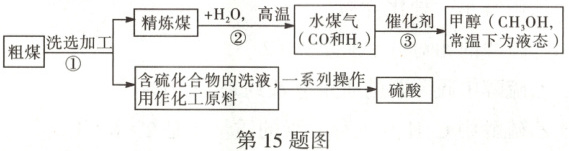
15. (6 分) 煤是社会生产、生活中最重要的能源,其主要成分是碳。工业上常把煤进行气化和液化处理,使煤变成清洁能源。煤气化和液化的流程如图所示,回答下列问题。
(1) 粗煤属于
(2) 步骤①中分离操作的名称是
(3) 步骤③中发生反应的化学方程式为
(4) 相比于直接用煤作燃料,“煤的气化和液化”的优点是 (写一点即可)。
(1) 粗煤属于
混合物
(选填“纯净物”或“混合物”);步骤①②③中,不发生化学变化的是步骤①
。(2) 步骤①中分离操作的名称是
过滤
。(3) 步骤③中发生反应的化学方程式为
CO + 2H₂$\stackrel{催化剂}{=\!=\!=}$CH₃OH
。(4) 相比于直接用煤作燃料,“煤的气化和液化”的优点是 (写一点即可)。

答案:
15.
(1)混合物 ①
(2)过滤
(3)$CO + 2H_{2}\stackrel{催化剂}{=\!=\!=}CH_{3}OH$
(4)实现了煤的综合利用,更环保(合理即可)
【解析】本题主要考查煤的气化和液化及综合利用。
(1)粗煤由多种物质组成,属于混合物。步骤①是洗涤除去杂质,没有新物质生成,是物理变化。步骤②、步骤③后都有新物质生成,是化学变化。所以不发生化学变化的是步骤①。
(2)粗煤经过步骤①得到精炼煤和含硫化合物的洗液,由此知步骤①是实现固液分离的操作,故步骤①中分离操作的名称是过滤。
(3)步骤③中发生反应的反应物是水煤气($CO$和$H_{2}$),生成物是甲醇($CH_{3}OH$),条件是催化剂,故化学方程式为$CO + 2H_{2}\stackrel{催化剂}{=\!=\!=}CH_{3}OH$。
(4)与直接用煤作燃料相比,“煤的气化和液化”产生的气态和液态燃料不仅是重要的化工原料,还比煤更易充分燃烧,产生的污染物更少,故“煤的气化和液化”的优点是实现了煤的综合利用,更环保(合理即可)。
(1)混合物 ①
(2)过滤
(3)$CO + 2H_{2}\stackrel{催化剂}{=\!=\!=}CH_{3}OH$
(4)实现了煤的综合利用,更环保(合理即可)
【解析】本题主要考查煤的气化和液化及综合利用。
(1)粗煤由多种物质组成,属于混合物。步骤①是洗涤除去杂质,没有新物质生成,是物理变化。步骤②、步骤③后都有新物质生成,是化学变化。所以不发生化学变化的是步骤①。
(2)粗煤经过步骤①得到精炼煤和含硫化合物的洗液,由此知步骤①是实现固液分离的操作,故步骤①中分离操作的名称是过滤。
(3)步骤③中发生反应的反应物是水煤气($CO$和$H_{2}$),生成物是甲醇($CH_{3}OH$),条件是催化剂,故化学方程式为$CO + 2H_{2}\stackrel{催化剂}{=\!=\!=}CH_{3}OH$。
(4)与直接用煤作燃料相比,“煤的气化和液化”产生的气态和液态燃料不仅是重要的化工原料,还比煤更易充分燃烧,产生的污染物更少,故“煤的气化和液化”的优点是实现了煤的综合利用,更环保(合理即可)。
16. (6 分) 核心素养·科学探究与实践关于燃烧的研究是一项重要的课题。某小组以“探究燃烧的奥秘”为主题开展项目式学习。
任务一: 认识燃烧
(1) 酒精、煤(含硫)、天然气是生活中常见的燃料,下列不属于三者燃烧共有的现象的是
A. 发光
B. 产生有刺激性气味的气体
C. 放热
D. 产生使澄清石灰水变浑浊的气体
(2) 写出酒精(${C_{2}H_{5}OH}$)完全燃烧的化学方程式:
任务二: 探究燃烧的条件及质量变化
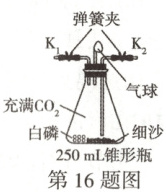
(3) 该小组同学按下列实验步骤开展探究。
步骤 1: 室温下,按如图所示组装装置,装入试剂,称量装置的总质量为 $m_{1}\ {g}$。
步骤 2: 将锥形瓶浸入 $80\ {{\hspace{0pt}}^{\circ }C}$ 的热水中,观察现象。
步骤 3: 取出装置,恢复至室温并擦干锥形瓶;打开弹簧夹 ${K_{1}}$ 和 ${K_{2}}$,从 ${K_{1}}$ 处缓慢通入约 $50\ {mL}$ 氧气,再关闭 ${K_{1}}$ 和 ${K_{2}}$,称量装置的总质量为 $m_{2}\ {g}$。
步骤 4: 将锥形瓶再次浸入 $80\ {{\hspace{0pt}}^{\circ }C}$ 的热水中,观察现象。
步骤 5: 取出装置,恢复至室温并擦干锥形瓶,称量装置的总质量为 $m_{3}\ {g}$。
① 通过上述实验,能证明燃烧需要氧气的实验现象是
② $m_{1}$、$m_{2}$、$m_{3}$ 的大小关系是
任务三: 调控燃烧
(4) 报道显示: 国内外一些煤田因发生煤层自燃,带来了资源浪费和环境污染。一旦煤层自燃,请给出一条合理的灭火建议:
注意: 若答对第(5)小题奖励 3 分,化学总得分不超过 40 分。
任务四: 再探铁的燃烧
(5) 查阅文献: 颗粒直径为 $20~30\ {nm}$ 的铁粉在空气中会发生自燃生成氧化铁。
结合已有知识,回答下列问题:
① 影响铁燃烧的因素有 、 。
② 铁与氧气反应的条件不同,产物不同。若 $5.6\ {g}$ 铁与氧气反应可得 $a\ {g}$ 产物,且铁无剩余,则 $a$ 的取值范围是
任务一: 认识燃烧
(1) 酒精、煤(含硫)、天然气是生活中常见的燃料,下列不属于三者燃烧共有的现象的是
B
(填字母)。A. 发光
B. 产生有刺激性气味的气体
C. 放热
D. 产生使澄清石灰水变浑浊的气体
(2) 写出酒精(${C_{2}H_{5}OH}$)完全燃烧的化学方程式:
C₂H₅OH + 3O₂$\stackrel{点燃}{=\!=\!=}$2CO₂ + 3H₂O
。任务二: 探究燃烧的条件及质量变化

(3) 该小组同学按下列实验步骤开展探究。
步骤 1: 室温下,按如图所示组装装置,装入试剂,称量装置的总质量为 $m_{1}\ {g}$。
步骤 2: 将锥形瓶浸入 $80\ {{\hspace{0pt}}^{\circ }C}$ 的热水中,观察现象。
步骤 3: 取出装置,恢复至室温并擦干锥形瓶;打开弹簧夹 ${K_{1}}$ 和 ${K_{2}}$,从 ${K_{1}}$ 处缓慢通入约 $50\ {mL}$ 氧气,再关闭 ${K_{1}}$ 和 ${K_{2}}$,称量装置的总质量为 $m_{2}\ {g}$。
步骤 4: 将锥形瓶再次浸入 $80\ {{\hspace{0pt}}^{\circ }C}$ 的热水中,观察现象。
步骤 5: 取出装置,恢复至室温并擦干锥形瓶,称量装置的总质量为 $m_{3}\ {g}$。
① 通过上述实验,能证明燃烧需要氧气的实验现象是
步骤2中白磷未燃烧,步骤4中白磷燃烧,产生大量白烟
。② $m_{1}$、$m_{2}$、$m_{3}$ 的大小关系是
m₁ > m₂ = m₃
。任务三: 调控燃烧
(4) 报道显示: 国内外一些煤田因发生煤层自燃,带来了资源浪费和环境污染。一旦煤层自燃,请给出一条合理的灭火建议:
取土填埋,隔绝空气(合理即可)
。注意: 若答对第(5)小题奖励 3 分,化学总得分不超过 40 分。
任务四: 再探铁的燃烧
(5) 查阅文献: 颗粒直径为 $20~30\ {nm}$ 的铁粉在空气中会发生自燃生成氧化铁。
结合已有知识,回答下列问题:
① 影响铁燃烧的因素有 、 。
② 铁与氧气反应的条件不同,产物不同。若 $5.6\ {g}$ 铁与氧气反应可得 $a\ {g}$ 产物,且铁无剩余,则 $a$ 的取值范围是
7.2≤a≤8.0
。
答案:
16.
(1)B
(2)$C_{2}H_{5}OH + 3O_{2}\stackrel{点燃}{=\!=\!=}2CO_{2} + 3H_{2}O$
(3)①步骤2中白磷未燃烧,步骤4中白磷燃烧,产生大量白烟 ②$m_{1} > m_{2} = m_{3}$
(4)取土填埋,隔绝空气(合理即可)
(5)①铁的表面积 氧气的浓度(或温度,合理即可) ②$7.2\leqslant a\leqslant8.0$
【解析】本题主要考查燃烧、燃烧的条件和调控。
(1)酒精、煤(含硫)、天然气三种常见燃料燃烧时,都发光、放热,都含有碳元素,燃烧都产生使澄清石灰水变浑浊的气体$CO_{2}$;煤(含硫)燃烧会产生有刺激性气味的气体$SO_{2}$,而另外两种燃料燃烧不会有刺激性气味的气体产生。
(2)酒精完全燃烧只生成$CO_{2}$和$H_{2}O$,燃烧的化学方程式为$C_{2}H_{5}OH + 3O_{2}\stackrel{点燃}{=\!=\!=}2CO_{2} + 3H_{2}O$。
(3)①步骤2中充满$CO_{2}$的锥形瓶浸入$80^{\circ}C$的热水中,锥形瓶内的白磷不燃烧;在步骤3中向锥形瓶中充入氧气,步骤4中将充入氧气的锥形瓶浸入$80^{\circ}C$的热水中,锥形瓶内的白磷燃烧,说明燃烧需要氧气,故能证明燃烧需要氧气的实验现象是步骤2中白磷未燃烧,步骤4中白磷燃烧,产生大量白烟。
②由于等体积的二氧化碳的质量大于氧气,故通入$50mL$氧气后,装置的总质量变小,但由于燃烧反应在密闭容器中进行,故反应前后质量不发生变化,即$m_{1} > m_{2} = m_{3}$。
(4)破坏燃烧所需的三个条件之一即可灭火,即清除可燃物或使可燃物与其他物品隔离、隔绝氧气或空气、降低温度至着火点以下。煤的主要成分是碳,其发生自燃时,不能用水灭火,否则碳和水在高温条件下会发生反应生成一氧化碳和氢气,使燃烧更旺,甚至发生爆炸,可以通过取土填埋等隔绝空气的方法来灭火。
(5)①根据文献资料,颗粒直径为$20\sim30nm$的铁粉总表面积很大,该铁粉能在空气中发生自燃说明铁的表面积影响铁的燃烧。除此之外,还有氧气的浓度、温度等也会影响铁的燃烧。
②铁与氧气反应全部生成$FeO$时,产物的质量最小,设生成物的质量为$x$。
$2Fe + O_{2}\stackrel{点燃}{=\!=\!=}2FeO$
$112$ $144$
$5.6g$ $x$
$\frac{112}{144}=\frac{5.6g}{x}$
$x = 7.2g$。
铁与氧气反应全部生成$Fe_{2}O_{3}$时,产物的质量最大,设生成物的质量为$y$。
$4Fe + 3O_{2}\stackrel{点燃}{=\!=\!=}2Fe_{2}O_{3}$
$224$ $320$
$5.6g$ $y$
$\frac{224}{320}=\frac{5.6g}{y}$
$y = 8.0g$。
综上所述,$a$的取值范围是$7.2\leqslant a\leqslant8.0$。
(1)B
(2)$C_{2}H_{5}OH + 3O_{2}\stackrel{点燃}{=\!=\!=}2CO_{2} + 3H_{2}O$
(3)①步骤2中白磷未燃烧,步骤4中白磷燃烧,产生大量白烟 ②$m_{1} > m_{2} = m_{3}$
(4)取土填埋,隔绝空气(合理即可)
(5)①铁的表面积 氧气的浓度(或温度,合理即可) ②$7.2\leqslant a\leqslant8.0$
【解析】本题主要考查燃烧、燃烧的条件和调控。
(1)酒精、煤(含硫)、天然气三种常见燃料燃烧时,都发光、放热,都含有碳元素,燃烧都产生使澄清石灰水变浑浊的气体$CO_{2}$;煤(含硫)燃烧会产生有刺激性气味的气体$SO_{2}$,而另外两种燃料燃烧不会有刺激性气味的气体产生。
(2)酒精完全燃烧只生成$CO_{2}$和$H_{2}O$,燃烧的化学方程式为$C_{2}H_{5}OH + 3O_{2}\stackrel{点燃}{=\!=\!=}2CO_{2} + 3H_{2}O$。
(3)①步骤2中充满$CO_{2}$的锥形瓶浸入$80^{\circ}C$的热水中,锥形瓶内的白磷不燃烧;在步骤3中向锥形瓶中充入氧气,步骤4中将充入氧气的锥形瓶浸入$80^{\circ}C$的热水中,锥形瓶内的白磷燃烧,说明燃烧需要氧气,故能证明燃烧需要氧气的实验现象是步骤2中白磷未燃烧,步骤4中白磷燃烧,产生大量白烟。
②由于等体积的二氧化碳的质量大于氧气,故通入$50mL$氧气后,装置的总质量变小,但由于燃烧反应在密闭容器中进行,故反应前后质量不发生变化,即$m_{1} > m_{2} = m_{3}$。
(4)破坏燃烧所需的三个条件之一即可灭火,即清除可燃物或使可燃物与其他物品隔离、隔绝氧气或空气、降低温度至着火点以下。煤的主要成分是碳,其发生自燃时,不能用水灭火,否则碳和水在高温条件下会发生反应生成一氧化碳和氢气,使燃烧更旺,甚至发生爆炸,可以通过取土填埋等隔绝空气的方法来灭火。
(5)①根据文献资料,颗粒直径为$20\sim30nm$的铁粉总表面积很大,该铁粉能在空气中发生自燃说明铁的表面积影响铁的燃烧。除此之外,还有氧气的浓度、温度等也会影响铁的燃烧。
②铁与氧气反应全部生成$FeO$时,产物的质量最小,设生成物的质量为$x$。
$2Fe + O_{2}\stackrel{点燃}{=\!=\!=}2FeO$
$112$ $144$
$5.6g$ $x$
$\frac{112}{144}=\frac{5.6g}{x}$
$x = 7.2g$。
铁与氧气反应全部生成$Fe_{2}O_{3}$时,产物的质量最大,设生成物的质量为$y$。
$4Fe + 3O_{2}\stackrel{点燃}{=\!=\!=}2Fe_{2}O_{3}$
$224$ $320$
$5.6g$ $y$
$\frac{224}{320}=\frac{5.6g}{y}$
$y = 8.0g$。
综上所述,$a$的取值范围是$7.2\leqslant a\leqslant8.0$。
查看更多完整答案,请扫码查看


