2025年人教金学典同步解析与测评高中化学选择性必修1人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年人教金学典同步解析与测评高中化学选择性必修1人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第12页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
【例题 2】下表给出了一些物质的燃烧热。
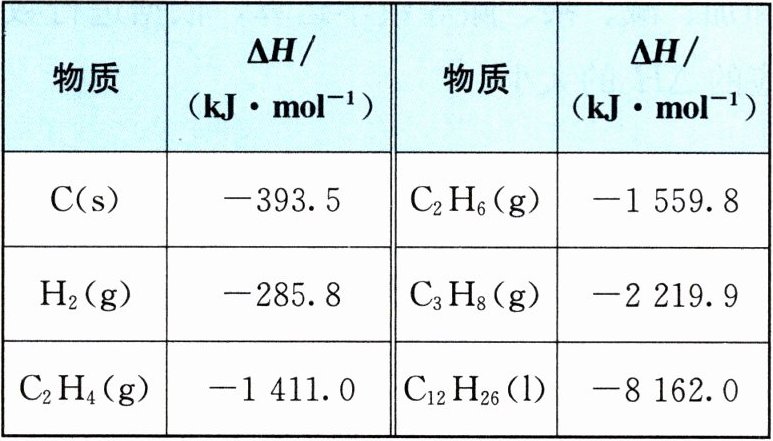
(1) 分析上表数据可知:
①分别完全燃烧 C(s) 和 C₃H₈(g),使其提供相同的热量,其中______产生的温室气体较多。
②不同烃燃烧的热值(单位质量燃料完全燃烧所放出的热量多少)与元素含量之间的关系是______。
(2) 根据上表数据计算,C₂H₄(g) + H₂(g) = C₂H₆(g) 的 ΔH = ______。

(1) 分析上表数据可知:
①分别完全燃烧 C(s) 和 C₃H₈(g),使其提供相同的热量,其中______产生的温室气体较多。
②不同烃燃烧的热值(单位质量燃料完全燃烧所放出的热量多少)与元素含量之间的关系是______。
(2) 根据上表数据计算,C₂H₄(g) + H₂(g) = C₂H₆(g) 的 ΔH = ______。
答案:
(2) 结合题意,在表中可以查得 C₂H₄(g)、H₂(g) 和 C₂H₆(g) 的燃烧热。
(2) - 137.0 kJ/mol
【解析】
(1) ①假设均产生 2219.9 kJ 的热量,则需要 1 mol C₃H₈(g),能产生 3 mol CO₂;而需要 C(s) 为 2219.9 kJ / 393.5 kJ·mol⁻¹ ≈ 5.64 mol,能产生 5.64 mol CO₂,故 C(s) 产生的温室气体较多。
(1) ①假设均产生 2219.9 kJ 的热量,则需要 1 mol C₃H₈(g),能产生 3 mol CO₂;而需要 C(s) 为 2219.9 kJ / 393.5 kJ·mol⁻¹ ≈ 5.64 mol,能产生 5.64 mol CO₂,故 C(s) 产生的温室气体较多。
②将表格中 CₓHᵧ 的燃烧热转化为 CHᵧ/ₓ 的燃烧热可知,烃分子中氢元素的质量分数越大,烃的热值越大。
(2) 结合题意,在表中可以查得 C₂H₄(g)、H₂(g) 和 C₂H₆(g) 的燃烧热。
C₂H₄(g) + 3O₂(g) = 2CO₂(g) + 2H₂O(l) ΔH₁ = - 1411.0 kJ/mol ①
H₂(g) + 1/2 O₂(g) = H₂O(l) ΔH₂ = - 285.8 kJ/mol ②
C₂H₆(g) + 7/2 O₂(g) = 2CO₂(g) + 3H₂O(l) ΔH₃ = - 1559.8 kJ/mol ③
根据盖斯定律,① + ② - ③ 可得:C₂H₄(g) + H₂(g) = C₂H₆(g)
ΔH = ΔH₁ + ΔH₂ - ΔH₃
= (- 1411.0 kJ/mol) + (- 285.8 kJ/mol) - (- 1559.8 kJ/mol)
= - 137.0 kJ/mol
【答案】
(1) ① C(s) ② 烃中氢元素的质量分数越大,烃的热值越大
(1) ① C(s) ② 烃中氢元素的质量分数越大,烃的热值越大
(2) - 137.0 kJ/mol
1. 下列关于图 1 - 15 所示转化关系(X 表示卤素)的说法中,不正确的是( )。

A.2H(g) + 2X(g) = 2HX(g) ΔH₃ < 0
B.生成 HX 的反应热与途径无关,所以 ΔH₁ = ΔH₂ + ΔH₃
C.Cl、Br、I 的非金属性依次减弱,所以途径Ⅱ所示反应中吸收的热量依次增多
D.生成 HCl 放出的热量比生成 HBr 的多,说明 HCl 比 HBr 稳定

A.2H(g) + 2X(g) = 2HX(g) ΔH₃ < 0
B.生成 HX 的反应热与途径无关,所以 ΔH₁ = ΔH₂ + ΔH₃
C.Cl、Br、I 的非金属性依次减弱,所以途径Ⅱ所示反应中吸收的热量依次增多
D.生成 HCl 放出的热量比生成 HBr 的多,说明 HCl 比 HBr 稳定
答案:
C
查看更多完整答案,请扫码查看


