2025年天星教育试题调研化学第9辑
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年天星教育试题调研化学第9辑 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第76页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
热考指数 ★★★★★
原创预测 碳酸镍具有良好的催化性能,在化学和工业领域应用广泛。利用废镍催化剂(主要成分为 Ni 及其氧化物、Al 和 Fe 的氧化物)获得碳酸镍的流程如图 1 所示。
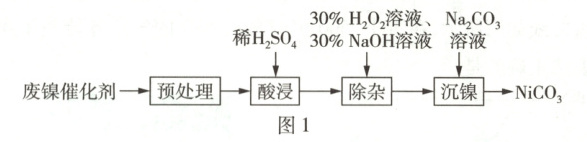
已知:常温下,溶液中金属离子开始沉淀和完全沉淀的 pH 如表所示。
(1)“酸浸”时,选择稀硫酸而非稀硝酸的原因是.7 ≤ pH < 6.7。
②该过程还可用 NaClO 替代 H₂O₂,调节 pH 为 3.5,该反应的离子方程式为________。
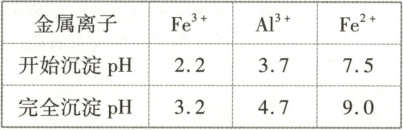
(3)H₂O₂ 在催化剂中 Fe 元素的作用下可以产生具有极强氧化活性的·OH,H₂O₂ 在固态催化剂表面转化的过程如图 2 所示。
过程①中每产生 1 mol O 空位,需要转移mol 电子;相同条件下,催化效果:LaFeO₂.₆,晶胞密度 ρ =(476 × 10²¹)/(Nₐa²b)g·cm⁻³(用含 a、b 的式子表示,已知:阿伏加德罗常数的值为 Nₐ,Ni 的相对原子质量为 59)。
原创预测 碳酸镍具有良好的催化性能,在化学和工业领域应用广泛。利用废镍催化剂(主要成分为 Ni 及其氧化物、Al 和 Fe 的氧化物)获得碳酸镍的流程如图 1 所示。

已知:常温下,溶液中金属离子开始沉淀和完全沉淀的 pH 如表所示。

(1)“酸浸”时,选择稀硫酸而非稀硝酸的原因是.7 ≤ pH < 6.7。
②该过程还可用 NaClO 替代 H₂O₂,调节 pH 为 3.5,该反应的离子方程式为________。
(3)H₂O₂ 在催化剂中 Fe 元素的作用下可以产生具有极强氧化活性的·OH,H₂O₂ 在固态催化剂表面转化的过程如图 2 所示。

过程①中每产生 1 mol O 空位,需要转移mol 电子;相同条件下,催化效果:LaFeO₂.₆,晶胞密度 ρ =(476 × 10²¹)/(Nₐa²b)g·cm⁻³(用含 a、b 的式子表示,已知:阿伏加德罗常数的值为 Nₐ,Ni 的相对原子质量为 59)。
答案:
解析
(1)“酸浸”时,废镍催化剂中镍和二价铁的氧化物均具有还原性,会把稀硝酸还原为氮氧化物,污染大气,所以选择稀硫酸而非稀硝酸。
(2)①已知 Kₛₚ[Ni(OH)₂] = 10⁻¹⁵.⁶,若溶液中 Ni²⁺浓度为 0.10 mol·L⁻¹,则当 Ni²⁺开始沉淀时 c(OH⁻) = √(10⁻¹⁵.⁶ / 0.10) mol·L⁻¹ = 10⁻⁷.³ mol·L⁻¹,则应控制溶液 pH < 6.7;又因为除杂时需除掉 Fe³⁺和 Al³⁺,结合题表数据可知 Fe³⁺完全沉淀时的 pH 为 3.2,Al³⁺完全沉淀时的 pH 为 4.7,所以需控制溶液 pH 的范围是 4.7 ≤ pH < 6.7。②该过程中用 NaClO 替代 H₂O₂,将 Fe²⁺氧化为 Fe³⁺,调节 pH 为 3.5,则 Fe³⁺转化为 Fe(OH)₃ 的离子方程式为 ClO⁻ + 2Fe²⁺ + 5H₂O = Cl⁻ + 2Fe(OH)₃↓ + 4H⁺。
(3)固态催化剂中含有 Fe³⁺、Fe²⁺,过程①中 H₂O₂ 转化为 H₂O 和 O₂,Fe³⁺得到电子被还原为 Fe²⁺,晶体中失去部分 O²⁻转化为 O₂,形成 O 空位,1 mol O²⁻形成 1 mol O 空位,转移 2 mol 电子;设 LaFeO₂.₆ 中 Fe³⁺的个数为 x,Fe²⁺的个数为 1 - x,已知 La 的化合价为 +3,根据化合物中各元素正、负化合价的代数和为 0 可知,3 + 3x + 2(1 - x) - 2×2.6 = 0,解得 x = 0.2,则 LaFeO₂.₆ 中 n(Fe³⁺) : n(Fe²⁺) = 0.2 : (1 - 0.2) = 1 : 4,同理可知,LaFeO₂.₈ 中 n(Fe³⁺) : n(Fe²⁺) = 3 : 2,晶体 LaFeO₂.₈ 中 Fe²⁺的数目相对较少,过程②为 H₂O₂ 被还原,Fe²⁺被氧化,晶胞中 Fe²⁺数目越多,与 H₂O₂ 反应时生成的具有极强氧化活性的·OH 越多,所以 LaFeO₂.₆ 的催化效果强于 LaFeO₂.₈ 的。
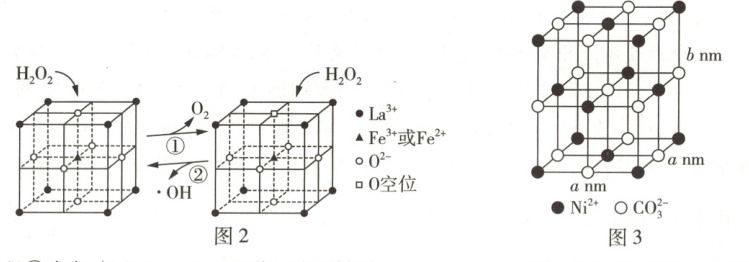
(4)由题图 3 可知,Ni²⁺的配位数为 6;由“均摊法”可知,1 个晶胞中 Ni²⁺的个数为 8×(1/8) + 6×(1/2) = 4,1 个晶胞中 CO₃²⁻ 的个数为 12×(1/4) + 1 = 4,即 1 个晶胞中含有 4 个 NiCO₃,该晶胞密度 ρ = m / V = ( (119 / Nₐ) × 4 g ) / (a²b × 10⁻²¹ cm³) = (476 × 10²¹) / (Nₐa²b) g·cm⁻³。
速解
与 LaFeO₂.₈ 相比,LaFeO₂.₆ 中 O 的个数少,根据化合物中各元素正、负化合价代数和为 0 可知,LaFeO₂.₆ 中的 Fe²⁺数目相对较多,Fe³⁺数目相对较少,Fe²⁺可将 H₂O₂ 还原为具有极强氧化活性的·OH,故 Fe²⁺数目多的催化效果好。
答案
(1) Ni 和二价铁的氧化物会与稀硝酸反应生成污染环境的氮氧化物
(2)①4.7 ≤ pH < 6.7 ②ClO⁻ + 2Fe²⁺ + 5H₂O = Cl⁻ + 2Fe(OH)₃↓ + 4H⁺
(3)2 >
(4)6 (476 × 10²¹) / (Nₐa²b)
(1)“酸浸”时,废镍催化剂中镍和二价铁的氧化物均具有还原性,会把稀硝酸还原为氮氧化物,污染大气,所以选择稀硫酸而非稀硝酸。
(2)①已知 Kₛₚ[Ni(OH)₂] = 10⁻¹⁵.⁶,若溶液中 Ni²⁺浓度为 0.10 mol·L⁻¹,则当 Ni²⁺开始沉淀时 c(OH⁻) = √(10⁻¹⁵.⁶ / 0.10) mol·L⁻¹ = 10⁻⁷.³ mol·L⁻¹,则应控制溶液 pH < 6.7;又因为除杂时需除掉 Fe³⁺和 Al³⁺,结合题表数据可知 Fe³⁺完全沉淀时的 pH 为 3.2,Al³⁺完全沉淀时的 pH 为 4.7,所以需控制溶液 pH 的范围是 4.7 ≤ pH < 6.7。②该过程中用 NaClO 替代 H₂O₂,将 Fe²⁺氧化为 Fe³⁺,调节 pH 为 3.5,则 Fe³⁺转化为 Fe(OH)₃ 的离子方程式为 ClO⁻ + 2Fe²⁺ + 5H₂O = Cl⁻ + 2Fe(OH)₃↓ + 4H⁺。
(3)固态催化剂中含有 Fe³⁺、Fe²⁺,过程①中 H₂O₂ 转化为 H₂O 和 O₂,Fe³⁺得到电子被还原为 Fe²⁺,晶体中失去部分 O²⁻转化为 O₂,形成 O 空位,1 mol O²⁻形成 1 mol O 空位,转移 2 mol 电子;设 LaFeO₂.₆ 中 Fe³⁺的个数为 x,Fe²⁺的个数为 1 - x,已知 La 的化合价为 +3,根据化合物中各元素正、负化合价的代数和为 0 可知,3 + 3x + 2(1 - x) - 2×2.6 = 0,解得 x = 0.2,则 LaFeO₂.₆ 中 n(Fe³⁺) : n(Fe²⁺) = 0.2 : (1 - 0.2) = 1 : 4,同理可知,LaFeO₂.₈ 中 n(Fe³⁺) : n(Fe²⁺) = 3 : 2,晶体 LaFeO₂.₈ 中 Fe²⁺的数目相对较少,过程②为 H₂O₂ 被还原,Fe²⁺被氧化,晶胞中 Fe²⁺数目越多,与 H₂O₂ 反应时生成的具有极强氧化活性的·OH 越多,所以 LaFeO₂.₆ 的催化效果强于 LaFeO₂.₈ 的。
(4)由题图 3 可知,Ni²⁺的配位数为 6;由“均摊法”可知,1 个晶胞中 Ni²⁺的个数为 8×(1/8) + 6×(1/2) = 4,1 个晶胞中 CO₃²⁻ 的个数为 12×(1/4) + 1 = 4,即 1 个晶胞中含有 4 个 NiCO₃,该晶胞密度 ρ = m / V = ( (119 / Nₐ) × 4 g ) / (a²b × 10⁻²¹ cm³) = (476 × 10²¹) / (Nₐa²b) g·cm⁻³。
速解
与 LaFeO₂.₈ 相比,LaFeO₂.₆ 中 O 的个数少,根据化合物中各元素正、负化合价代数和为 0 可知,LaFeO₂.₆ 中的 Fe²⁺数目相对较多,Fe³⁺数目相对较少,Fe²⁺可将 H₂O₂ 还原为具有极强氧化活性的·OH,故 Fe²⁺数目多的催化效果好。
答案
(1) Ni 和二价铁的氧化物会与稀硝酸反应生成污染环境的氮氧化物
(2)①4.7 ≤ pH < 6.7 ②ClO⁻ + 2Fe²⁺ + 5H₂O = Cl⁻ + 2Fe(OH)₃↓ + 4H⁺
(3)2 >
(4)6 (476 × 10²¹) / (Nₐa²b)
查看更多完整答案,请扫码查看


