2025年新坐标同步练习高中化学选择性必修第三册人教版青海专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新坐标同步练习高中化学选择性必修第三册人教版青海专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第65页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
4. 物理性质
(1) 溶解性
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水⒀
(2) 熔点和沸点
羧酸的熔点和沸点随分子中碳原子数的增加而⒃
(1) 溶解性
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水⒀
互溶
。随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速⒁减小
,甚至不溶于水。高级脂肪酸是⒂不溶于
水的蜡状固体。(2) 熔点和沸点
羧酸的熔点和沸点随分子中碳原子数的增加而⒃
升高
,且与相对分子质量相当的其他有机化合物相比,沸点⒄较高
,这与羧酸分子间可以形成⒅氢键
有关。
答案:
1. 对于溶解性:
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水$\boldsymbol{13}$互溶。
随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速$\boldsymbol{14}$减小。
高级脂肪酸是$\boldsymbol{15}$不溶于水的蜡状固体。
2. 对于熔点和沸点:
羧酸的熔点和沸点随分子中碳原子数的增加而$\boldsymbol{16}$升高。
且与相对分子质量相当的其他有机化合物相比,沸点$\boldsymbol{17}$较高。
这与羧酸分子间可以形成$\boldsymbol{18}$氢键有关。
对于“用什么试剂可以鉴别甲酸和乙酸”:
解:甲酸分子中含有醛基$(-CHO)$,乙酸分子中没有醛基。可以用新制氢氧化铜悬浊液(或银氨溶液)鉴别。
取少量两种溶液于试管中,分别加入新制氢氧化铜悬浊液,加热。
有砖红色沉淀生成的是甲酸,无明显现象的是乙酸(若用银氨溶液,有银镜生成的是甲酸,无银镜生成的是乙酸)。
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水$\boldsymbol{13}$互溶。
随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速$\boldsymbol{14}$减小。
高级脂肪酸是$\boldsymbol{15}$不溶于水的蜡状固体。
2. 对于熔点和沸点:
羧酸的熔点和沸点随分子中碳原子数的增加而$\boldsymbol{16}$升高。
且与相对分子质量相当的其他有机化合物相比,沸点$\boldsymbol{17}$较高。
这与羧酸分子间可以形成$\boldsymbol{18}$氢键有关。
对于“用什么试剂可以鉴别甲酸和乙酸”:
解:甲酸分子中含有醛基$(-CHO)$,乙酸分子中没有醛基。可以用新制氢氧化铜悬浊液(或银氨溶液)鉴别。
取少量两种溶液于试管中,分别加入新制氢氧化铜悬浊液,加热。
有砖红色沉淀生成的是甲酸,无明显现象的是乙酸(若用银氨溶液,有银镜生成的是甲酸,无银镜生成的是乙酸)。
(1) 苯甲酸钠可以用作食品防腐剂 (
(2) 羧酸的沸点比相对分子质量相近的醇的沸点低 (
(3) 乙酸的分子式为$C_{2}H_{4}O_{2}$,所以乙酸属于四元酸 (
(4) 乙酸、草酸、硬脂酸和石炭酸均属于羧酸类有机化合物 (
(5) 软脂酸$(C_{15}H_{31}COOH)和油酸(C_{17}H_{33}COOH)$都属于饱和高级脂肪酸 (
√
)(2) 羧酸的沸点比相对分子质量相近的醇的沸点低 (
×
)(3) 乙酸的分子式为$C_{2}H_{4}O_{2}$,所以乙酸属于四元酸 (
×
)(4) 乙酸、草酸、硬脂酸和石炭酸均属于羧酸类有机化合物 (
×
)(5) 软脂酸$(C_{15}H_{31}COOH)和油酸(C_{17}H_{33}COOH)$都属于饱和高级脂肪酸 (
×
)
答案:
(1)√
(2)×
(3)×
(4)×
(5)×
(1)√
(2)×
(3)×
(4)×
(5)×
1. (教材习题改编) 苯甲酸常用作食品添加剂。下列有关苯甲酸的说法正确的是 (
A.其同系物中相对分子质量最小的是$C_{7}H_{6}O_{2}$
B.其分子中所有原子一定共面
C.可用重结晶法提纯苯甲酸
D.其钠盐可用作奶粉中的抗氧化剂
C
)A.其同系物中相对分子质量最小的是$C_{7}H_{6}O_{2}$
B.其分子中所有原子一定共面
C.可用重结晶法提纯苯甲酸
D.其钠盐可用作奶粉中的抗氧化剂
答案:
解析:选C。苯甲酸的同系物中相对分子质量最小的是C₇H₆O₂,A错误;苯甲酸分子中所有原子不一定共面,B错误;苯甲酸的溶解度随温度变化较大,可用重结晶法提纯,C正确;苯甲酸钠是常用的食品防腐剂,不能用作抗氧化剂,D错误。
2. 下列有关常见羧酸的说法正确的是 ( )
A.常温下,甲酸是一种无色、有刺激性气味的气体,能与水互溶
B.乙酸的沸点低于丙醇,高于乙醇
C.苯甲酸与 互为同系物
互为同系物
D.乙二酸具有还原性,可以使酸性$KMnO_{4}$溶液褪色
A.常温下,甲酸是一种无色、有刺激性气味的气体,能与水互溶
B.乙酸的沸点低于丙醇,高于乙醇
C.苯甲酸与
 互为同系物
互为同系物D.乙二酸具有还原性,可以使酸性$KMnO_{4}$溶液褪色
答案:
解析:选D。A.常温下,甲酸是一种无色、有刺激性气味的液体,能与水互溶,A不正确;B.乙酸的沸点高于丙醇的沸点,B不正确;C.苯甲酸与 COOH官能团个数不同,二者不互为同系物,C不正确;D.乙二酸具有还原性,酸性高锰酸钾具有氧化性,二者能发生氧化还原反应,可以使酸性KMnO₄溶液褪色,D正确。
COOH官能团个数不同,二者不互为同系物,C不正确;D.乙二酸具有还原性,酸性高锰酸钾具有氧化性,二者能发生氧化还原反应,可以使酸性KMnO₄溶液褪色,D正确。
解析:选D。A.常温下,甲酸是一种无色、有刺激性气味的液体,能与水互溶,A不正确;B.乙酸的沸点高于丙醇的沸点,B不正确;C.苯甲酸与
 COOH官能团个数不同,二者不互为同系物,C不正确;D.乙二酸具有还原性,酸性高锰酸钾具有氧化性,二者能发生氧化还原反应,可以使酸性KMnO₄溶液褪色,D正确。
COOH官能团个数不同,二者不互为同系物,C不正确;D.乙二酸具有还原性,酸性高锰酸钾具有氧化性,二者能发生氧化还原反应,可以使酸性KMnO₄溶液褪色,D正确。 3. 写出下列酸的名称:
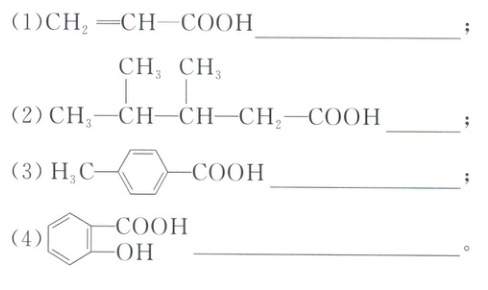

(1)丙烯酸 (2)3,4-二甲基戊酸 (3)对甲基苯甲酸 (4)邻羟基苯甲酸
答案:
(1)丙烯酸
(2)3,4-二甲基戊酸
(3)对甲基苯甲酸
(4)邻羟基苯甲酸
(1)丙烯酸
(2)3,4-二甲基戊酸
(3)对甲基苯甲酸
(4)邻羟基苯甲酸
羧酸的化学性质主要取决于①
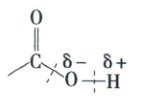
当$O - H$断裂时,会解离出$H^{+}$,使羧酸表现出酸性;当$C - O$断裂时,—OH可以被其他基团取代,生成酯、酰胺等羧酸衍生物。
羧基
官能团。由于受氧原子电负性较大等因素的影响,当羧酸发生化学反应时,羧基结构中如下图虚线所示部位的化学键容易断裂。
当$O - H$断裂时,会解离出$H^{+}$,使羧酸表现出酸性;当$C - O$断裂时,—OH可以被其他基团取代,生成酯、酰胺等羧酸衍生物。
答案:
①羧基
1. 酸性
羧酸是一类弱酸,具有酸类的共同性质。
(1) 实验探究羧酸的酸性
提供试剂:浓度均为$0.01mol·L^{-1}$的甲酸、苯甲酸和乙二酸、$0.01mol·L^{-1}的NaOH$溶液、酚酞、紫色石蕊溶液、$pH$试纸。

(2) 实验探究羧酸酸性的强弱
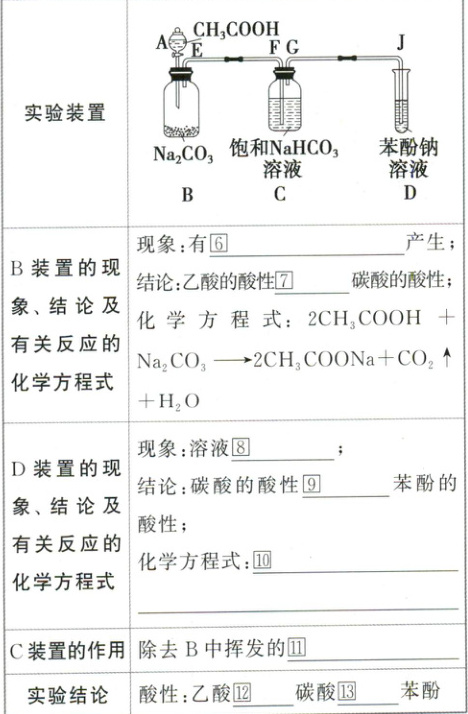
羧酸是一类弱酸,具有酸类的共同性质。
(1) 实验探究羧酸的酸性
提供试剂:浓度均为$0.01mol·L^{-1}$的甲酸、苯甲酸和乙二酸、$0.01mol·L^{-1}的NaOH$溶液、酚酞、紫色石蕊溶液、$pH$试纸。

(2) 实验探究羧酸酸性的强弱

答案:
②褪去 ③红色 ④pH均大于2 ⑤甲酸、苯甲酸和乙二酸均具有弱酸性 ⑥无色气体 ⑦> ⑧变浑浊 ⑨> ⑩ ⑪乙酸 ⑫> ⑬>
⑪乙酸 ⑫> ⑬>
②褪去 ③红色 ④pH均大于2 ⑤甲酸、苯甲酸和乙二酸均具有弱酸性 ⑥无色气体 ⑦> ⑧变浑浊 ⑨> ⑩
 ⑪乙酸 ⑫> ⑬>
⑪乙酸 ⑫> ⑬> 查看更多完整答案,请扫码查看


