12. (9分)为应对气候变化,我国力争到2060年前,实现碳中和。
(1)吸附法是利用固态吸附剂对气体进行有选择性的可逆吸附来分离回收$CO_2,$该吸附剂可能具有
(2)利用海洋封存$CO_2,$会引起海水酸化,解释引起海水酸化的原因:
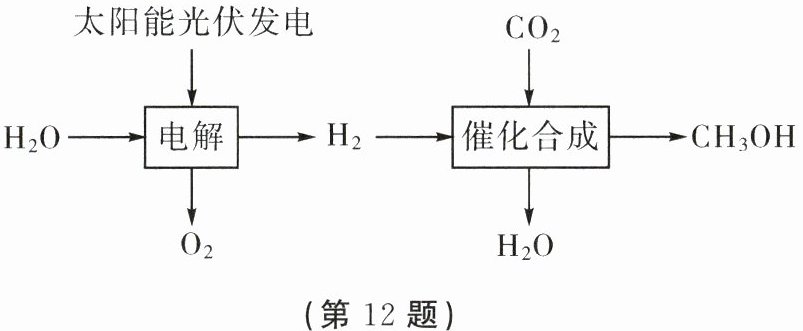
(3)我国自主研发的“液态太阳能燃料合成技术”可将$CO_2$转化为$CH_3OH($甲醇)等物质,生产流程如图所示:
①该流程中可循环利用的物质是
②“电解”得到的$H_2$和$O_2$的质量之比为
③“催化合成”阶段$,CO_2$在一定条件下转化为$CH_3OH$的反应原理为
(1)吸附法是利用固态吸附剂对气体进行有选择性的可逆吸附来分离回收$CO_2,$该吸附剂可能具有
疏松多孔
的结构。将捕集到的$CO_2$转化成流体态(气态、超临界态和液态共存)输送到封存地点,此过程中二氧化碳分子没有
(填“有”或“没有”)改变。(2)利用海洋封存$CO_2,$会引起海水酸化,解释引起海水酸化的原因:
二氧化碳与水反应生成碳酸,碳酸溶液显酸性
。(3)我国自主研发的“液态太阳能燃料合成技术”可将$CO_2$转化为$CH_3OH($甲醇)等物质,生产流程如图所示:
①该流程中可循环利用的物质是
${H_{2}O}$
。②“电解”得到的$H_2$和$O_2$的质量之比为
$1:8$
。③“催化合成”阶段$,CO_2$在一定条件下转化为$CH_3OH$的反应原理为
${CO_{2} + 3H_{2}\xlongequal{一定条件}CH_{3}OH + H_{2}O}$
(用化学方程式表示)。
答案:
(1)疏松多孔 没有
(2)二氧化碳与水反应生成碳酸,碳酸溶液显酸性(2分)
(3)①${H_{2}O}$ ②$1:8$(2分)
③${CO_{2} + 3H_{2}\xlongequal{一定条件}CH_{3}OH + H_{2}O}$(2分)
(1)疏松多孔 没有
(2)二氧化碳与水反应生成碳酸,碳酸溶液显酸性(2分)
(3)①${H_{2}O}$ ②$1:8$(2分)
③${CO_{2} + 3H_{2}\xlongequal{一定条件}CH_{3}OH + H_{2}O}$(2分)
13. (11分)同学们围绕常见气体的制取开展了实验活动,请你一起参与。
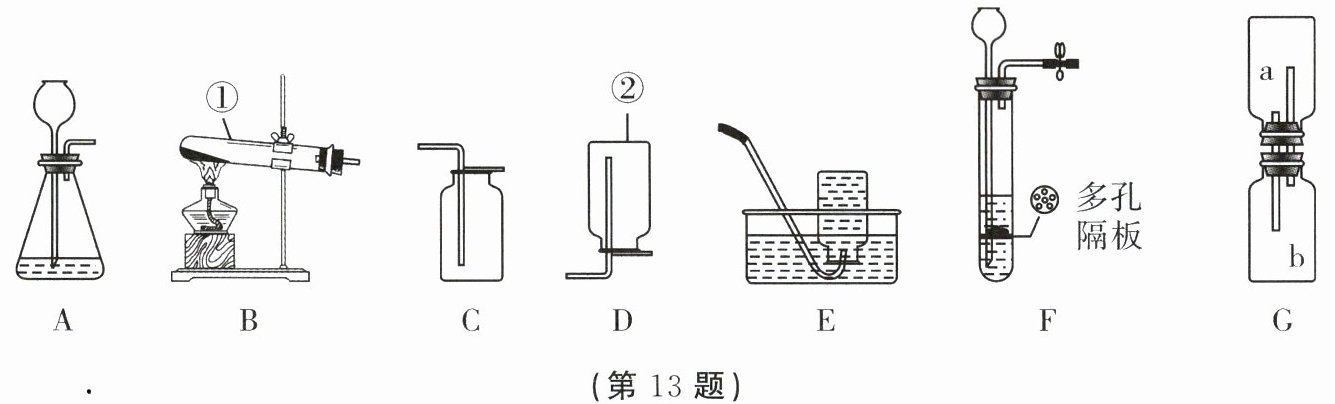
(1)写出标号仪器的名称:①
(2)实验室制取二氧化碳可选用的装置为
(3)装置G中,集气瓶a内充满二氧化碳,集气瓶b内为空气,按图连接好装置,静置10min后分别将燃着的木条伸入集气瓶a、b中,可以观察到的现象是
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味,密度比空气小,极易溶于水的气体。制取并收集氨气,应从图中A~E中选择的装置是

(1)写出标号仪器的名称:①
试管
,②集气瓶
。(2)实验室制取二氧化碳可选用的装置为
A
和C
(从A~E中选取,填序号)。反应的化学方程式为${CaCO_{3} + 2HCl\xlongequal{}CaCl_{2} + H_{2}O + CO_{2}\uparrow }$
。若用装置F作为发生装置,该装置的优点是可以随时控制反应的发生和停止
。关闭止水夹后,F装置内气体压强变大
(填“变大”、“变小”或“不变”)。(3)装置G中,集气瓶a内充满二氧化碳,集气瓶b内为空气,按图连接好装置,静置10min后分别将燃着的木条伸入集气瓶a、b中,可以观察到的现象是
伸入集气瓶a中的木条继续燃烧,伸入集气瓶b中的木条熄灭
。(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色、有刺激性气味,密度比空气小,极易溶于水的气体。制取并收集氨气,应从图中A~E中选择的装置是
B
和D
(填字母)。
答案:
(1)①试管 ②集气瓶
(2)A C ${CaCO_{3} + 2HCl\xlongequal{}CaCl_{2} + H_{2}O + CO_{2}\uparrow }$(2分) 可以随时控制反应的发生和停止 变大
(3)伸入集气瓶a中的木条继续燃烧,伸入集气瓶b中的木条熄灭
(4)B D
(1)①试管 ②集气瓶
(2)A C ${CaCO_{3} + 2HCl\xlongequal{}CaCl_{2} + H_{2}O + CO_{2}\uparrow }$(2分) 可以随时控制反应的发生和停止 变大
(3)伸入集气瓶a中的木条继续燃烧,伸入集气瓶b中的木条熄灭
(4)B D
查看更多完整答案,请扫码查看


