第84页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
探究 质量守恒定律的实验探究
问题情境
1. 化学反应前后各物质的质量总和有没有发生改变?
你的猜想:反应前后物质总质量可能______。
设计并进行如下实验验证猜想。
|实验方案|将铜粉平铺于锥形瓶的底部,把上端系有小气球的玻璃导管插入单孔橡胶塞,用橡胶塞塞紧锥形瓶口。将装置放在天平上称量,记录所称的质量 $ m_1 $。再将锥形瓶置于陶土网上,用酒精灯加热,观察实验现象。反应一段时间后停止加热,待装置冷却后再次称量,记录所称的质量 $ m_2 $|在锥形瓶中加入用砂纸打磨干净的铁丝,再小心地放入盛有硫酸铜溶液的小试管,塞好橡胶塞。将装置放在天平上称量,记录所称的质量 $ m_1 $。取下锥形瓶并将其倾斜,使小试管中的硫酸铜溶液进入锥形瓶,观察实验现象。反应一段时间后再次称量,记录所称的质量 $ m_2 $|
|实验现象|紫红色粉末逐渐变成______色,气球先______后______;反应后天平______|铁钉表面______,溶液由______变成______;反应后天平______|
|实验分析|反应前:铜粉、空气、锥形瓶、气球反应后:氧化铜、空气中剩余的气体、锥形瓶、气球|反应前:铁丝、硫酸铜溶液、小试管、锥形瓶、橡胶塞反应后:铜、硫酸亚铁、剩余铁丝或剩余硫酸铜溶液、小试管、锥形瓶、橡胶塞|
|化学反应符号表达式| | |
|实验结论|______的各物质的______,等于反应后______的各物质的______|
2. 方案中气球和橡胶塞的作用是什么?气球先变大后变小的原因是什么?
3. 冰融化后,得到水的质量与原来冰的质量相等,这个变化能否用质量守恒定律进行解释?
4. 是否存在违背质量守恒定律的化学反应呢?
|实验内容|在烧杯中加入碳酸钠,再小心地放入盛有盐酸的小试管,将装置放在天平上,记录所称的质量。取下烧杯并将其倾斜,使小试管中的盐酸进入烧杯,观察现象,反应一段时间后再次称量。比较反应前后的称量结果|取一根用砂纸打磨干净的长镁条和一个陶土网,将它们一起放在天平上称量,记录所称的质量。在陶土网上方将镁条点燃,观察现象。将镁条燃烧后所得固体与陶土网一起放在天平上称量,比较反应前后的称量结果|
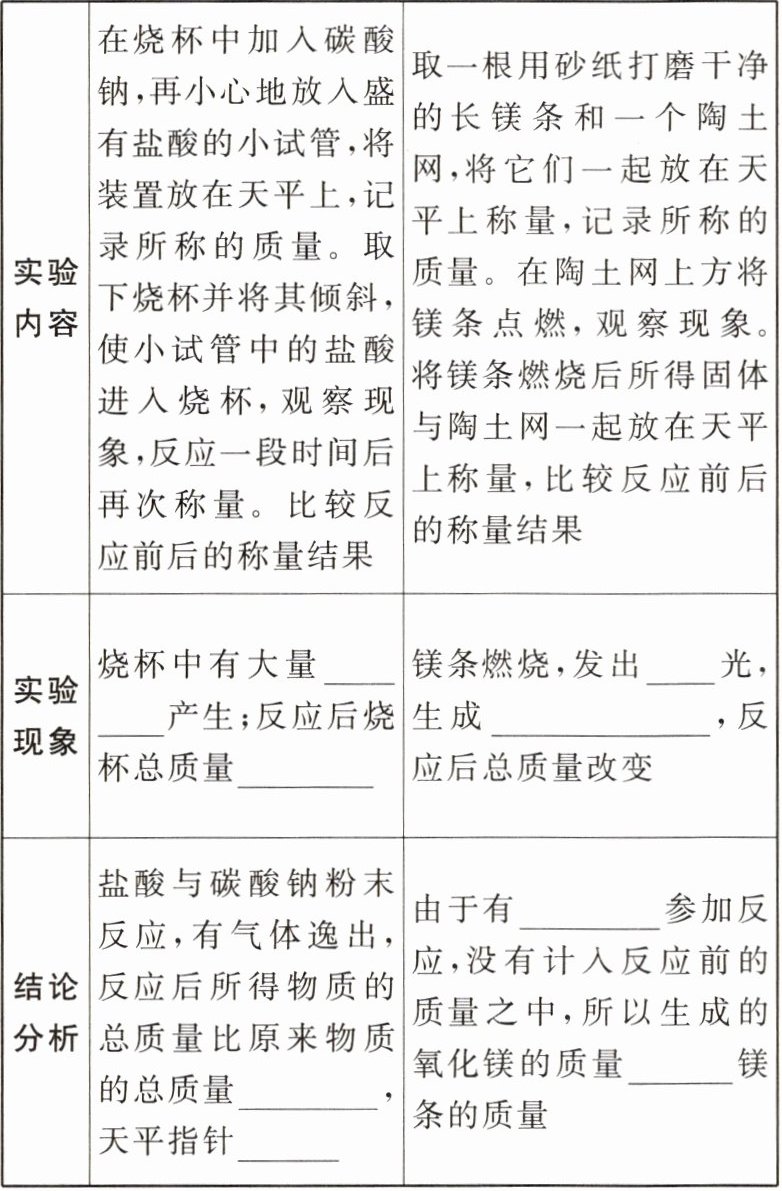
|实验现象|烧杯中有大量______产生;反应后烧杯总质量______|镁条燃烧,发出______光,生成______,反应后总质量改变|
|结论分析|盐酸与碳酸钠粉末反应,有气体逸出,反应后所得物质的总质量比原来物质的总质量______,天平指针______|由于有______参加反应,没有计入反应前的质量之中,所以生成的氧化镁的质量______镁条的质量|
5. 实验中两次称量的结果与你的预计是否一致?为什么会出现这样的实验结果?这两个反应遵循质量守恒定律吗?
6. 设计实验探究质量守恒定律需要注意哪些问题呢?
问题情境
1. 化学反应前后各物质的质量总和有没有发生改变?
你的猜想:反应前后物质总质量可能______。
设计并进行如下实验验证猜想。
|实验方案|将铜粉平铺于锥形瓶的底部,把上端系有小气球的玻璃导管插入单孔橡胶塞,用橡胶塞塞紧锥形瓶口。将装置放在天平上称量,记录所称的质量 $ m_1 $。再将锥形瓶置于陶土网上,用酒精灯加热,观察实验现象。反应一段时间后停止加热,待装置冷却后再次称量,记录所称的质量 $ m_2 $|在锥形瓶中加入用砂纸打磨干净的铁丝,再小心地放入盛有硫酸铜溶液的小试管,塞好橡胶塞。将装置放在天平上称量,记录所称的质量 $ m_1 $。取下锥形瓶并将其倾斜,使小试管中的硫酸铜溶液进入锥形瓶,观察实验现象。反应一段时间后再次称量,记录所称的质量 $ m_2 $|
|实验现象|紫红色粉末逐渐变成______色,气球先______后______;反应后天平______|铁钉表面______,溶液由______变成______;反应后天平______|
|实验分析|反应前:铜粉、空气、锥形瓶、气球反应后:氧化铜、空气中剩余的气体、锥形瓶、气球|反应前:铁丝、硫酸铜溶液、小试管、锥形瓶、橡胶塞反应后:铜、硫酸亚铁、剩余铁丝或剩余硫酸铜溶液、小试管、锥形瓶、橡胶塞|
|化学反应符号表达式| | |
|实验结论|______的各物质的______,等于反应后______的各物质的______|
2. 方案中气球和橡胶塞的作用是什么?气球先变大后变小的原因是什么?
3. 冰融化后,得到水的质量与原来冰的质量相等,这个变化能否用质量守恒定律进行解释?
4. 是否存在违背质量守恒定律的化学反应呢?
|实验内容|在烧杯中加入碳酸钠,再小心地放入盛有盐酸的小试管,将装置放在天平上,记录所称的质量。取下烧杯并将其倾斜,使小试管中的盐酸进入烧杯,观察现象,反应一段时间后再次称量。比较反应前后的称量结果|取一根用砂纸打磨干净的长镁条和一个陶土网,将它们一起放在天平上称量,记录所称的质量。在陶土网上方将镁条点燃,观察现象。将镁条燃烧后所得固体与陶土网一起放在天平上称量,比较反应前后的称量结果|

|实验现象|烧杯中有大量______产生;反应后烧杯总质量______|镁条燃烧,发出______光,生成______,反应后总质量改变|
|结论分析|盐酸与碳酸钠粉末反应,有气体逸出,反应后所得物质的总质量比原来物质的总质量______,天平指针______|由于有______参加反应,没有计入反应前的质量之中,所以生成的氧化镁的质量______镁条的质量|
5. 实验中两次称量的结果与你的预计是否一致?为什么会出现这样的实验结果?这两个反应遵循质量守恒定律吗?
6. 设计实验探究质量守恒定律需要注意哪些问题呢?
答案:
提示 变大、变小或不变 黑 膨胀 变瘪 平衡 有一层红色物质析出 蓝色 浅绿色 平衡 ${Cu + O_{2}}$$\xrightarrow{加热}$${CuO}$ ${Fe + CuSO_{4} \to Cu + FeSO_{4}}$ 参加化学反应 质量之和 生成 质量之和 气球和橡胶塞的作用是使装置密封,避免装置中的物质与外界交换。开始加热铜粉时,装置中温度升高,瓶内的压强增大,故气球膨胀;反应过程中消耗了氧气,瓶内气体减少,压强降低,故气球变小。 不能,因为冰融化成水的过程中没有发生化学变化。 气泡 减小 白 白色固体 减小 偏右 氧气 不一定等于 两次称量的结果与预计不一致。镁条燃烧后称量的质量可能会出现三种情况:①质量减少,因产生白烟,造成氧化镁散失太多;②质量增大,因为镁条足够长,多数氧化镁附着于镁条上面;③质量不变,以上两种因素综合的结果。但是这两个反应都遵循质量守恒定律。 对于有气体参与或生成的化学反应,在验证质量守恒定律时,必须在密闭容器中进行。
查看更多完整答案,请扫码查看


