第54页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
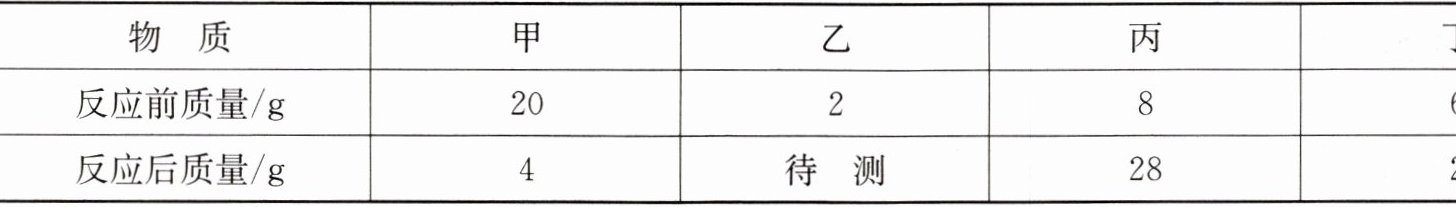
9. 一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如表所示。下列说法正确的是(
|物质|甲|乙|丙|丁|
|反应前质量/g|20|2|8|6|
|反应后质量/g|4|待测|28|2|
A.反应中甲和丁的质量之比为$2:1$
B.丙可能是一种单质
C.该反应可能是$2Cu + O_2\stackrel{\triangle}{=\!=\!=}2CuO$
D.丙和丁的相对分子质量之比一定为$5:1$
C
)|物质|甲|乙|丙|丁|
|反应前质量/g|20|2|8|6|
|反应后质量/g|4|待测|28|2|

A.反应中甲和丁的质量之比为$2:1$
B.丙可能是一种单质
C.该反应可能是$2Cu + O_2\stackrel{\triangle}{=\!=\!=}2CuO$
D.丙和丁的相对分子质量之比一定为$5:1$
答案:
C
10. 一定量甲烷$(CH_4)$在氧气中不完全燃烧,生成一氧化碳、二氧化碳和水的分子个数之比可能为(
A.$1:1:2$
B.$2:1:4$
C.$2:3:6$
D.$3:1:8$
D
)A.$1:1:2$
B.$2:1:4$
C.$2:3:6$
D.$3:1:8$
答案:
D
11. (1)硫在氧气中燃烧的化学方程式是$S + O_2\stackrel{点燃}{=\!=\!=}SO_2$,表示参与反应的各物质之间的质量关系,即在点燃条件下,每
(2)化学反应前后必定不发生改变的是
① 原子数目 ② 分子数目 ③ 元素种类 ④ 物质种类 ⑤ 原子种类 ⑥ 物质的总质量
A. ①④⑥
B. ①③⑤⑥
C. ①②⑥
D. ②③⑤
(3)某纯净物$X$在空气中完全燃烧,反应的化学方程式为$2X + 3O_2\stackrel{点燃}{=\!=\!=}2CO_2 + 4H_2O$,则$X$的化学式为
(4)密闭容器中有甲、乙两种物质各$10g$,加热一段时间后测得容器中各物质的质量如下表。
|物质|甲|乙|丙|丁|
|反应后质量/g|1.5|x|0.8|2.2|

下列说法正确的是
A. 该反应为化合反应
B. $x = 5.4$
C. 丙、丁一定是单质
D. 甲一定是化合物
32
份质量的硫与32
份质量的氧气恰好完全反应生成64
份质量的二氧化硫。(2)化学反应前后必定不发生改变的是
B
(填字母)。① 原子数目 ② 分子数目 ③ 元素种类 ④ 物质种类 ⑤ 原子种类 ⑥ 物质的总质量
A. ①④⑥
B. ①③⑤⑥
C. ①②⑥
D. ②③⑤
(3)某纯净物$X$在空气中完全燃烧,反应的化学方程式为$2X + 3O_2\stackrel{点燃}{=\!=\!=}2CO_2 + 4H_2O$,则$X$的化学式为
$\mathrm {CH}_{4}\mathrm {O}$
。(4)密闭容器中有甲、乙两种物质各$10g$,加热一段时间后测得容器中各物质的质量如下表。
|物质|甲|乙|丙|丁|
|反应后质量/g|1.5|x|0.8|2.2|

下列说法正确的是
D
(填字母)。A. 该反应为化合反应
B. $x = 5.4$
C. 丙、丁一定是单质
D. 甲一定是化合物
答案:
32
32
64
B
$\mathrm {CH}_{4}\mathrm {O}$
D
32
64
B
$\mathrm {CH}_{4}\mathrm {O}$
D
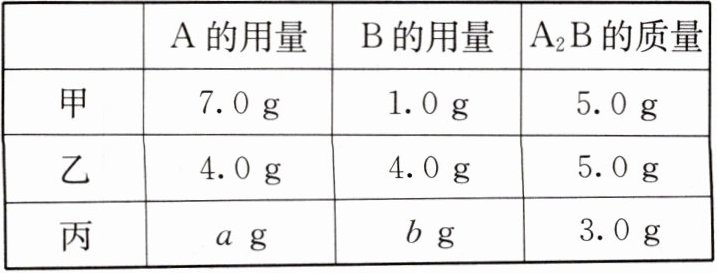
12. 金属单质$A和非金属单质B可生成化合物A_2B$,反应的化学方程式为$2A + B\stackrel{\triangle}{=\!=\!=}A_2B$。某兴趣小组的甲、乙、丙三名同学分别在实验室内做该实验,充分反应时,所用$A和B$的质量各不相同,但总质量相等,都是$8.0g$。有关实验数据记录如下,则丙同学实验中$a:b$的值可能是多少?
| | $A$的用量 | $B$的用量 | $A_2B$的质量 |
|甲| $7.0g$ | $1.0g$ | $5.0g$ |
|乙| $4.0g$ | $4.0g$ | $5.0g$ |
|丙| $a g$ | $b g$ | $3.0g$ |
| | $A$的用量 | $B$的用量 | $A_2B$的质量 |
|甲| $7.0g$ | $1.0g$ | $5.0g$ |
|乙| $4.0g$ | $4.0g$ | $5.0g$ |
|丙| $a g$ | $b g$ | $3.0g$ |

答案:
解:对比甲、乙两同学所用$\mathrm {A}$和$\mathrm {B}$的质量及生成$\mathrm {A}_{2}\mathrm {B}$的质量:
同样生成$5.0\mathrm {gA}_{2}\mathrm {B},$甲实验$\mathrm {B}$的用量为$1.0\mathrm {g}、$乙实验$\mathrm {B}$的用量
为$4.0\mathrm {g},$则可得反应生成$5.0\mathrm {gA}_{2}\mathrm {B}$时需要消耗$\mathrm {B}$的质量为$1.0\mathrm {g}。$
利用质量守恒定律,可判断生成$5.0\mathrm {gA}_{2}\mathrm {B}$时消耗$\mathrm {B}$的质量为
$1.0\mathrm {g},$则消耗$\mathrm {A}$的质量$=5.0\mathrm {g}-1.0\mathrm {g}=4.0\mathrm {g},$则两物质恰好完全
反应时,$\mathrm {A}、$$\mathrm {B}$两物质的用量比为4∶1
根据反应中反应物$\mathrm {A}、$$\mathrm {B}$两物质的质量比为4∶1及质量守恒
定律,由于丙同学实验中生成$\mathrm {A}_{2}\mathrm {B}$的质量$3.0\mathrm {g}$
若$\mathrm {A}$的用量$=3.0\mathrm {g}×45=2.4\mathrm {g},$此时$\mathrm {B}$的用量$=8.0\mathrm {g}-2.4\mathrm {g}=5.6\mathrm {g} $
若$\mathrm {B}$的用量$=3.0\mathrm {g}×15=0.6\mathrm {g},$此时$\mathrm {A}$的用量$=8.0\mathrm {g}-0.6\mathrm {g}=7.4\mathrm {g} $
因此丙学生实验中$\mathrm {a}∶\mathrm {b}$的值为2.4∶5.6=3∶7或7.4∶0.6=37∶3
答:丙学生实验中$\mathrm {a}∶\mathrm {b}$的值可能是3∶7或37∶3.
同样生成$5.0\mathrm {gA}_{2}\mathrm {B},$甲实验$\mathrm {B}$的用量为$1.0\mathrm {g}、$乙实验$\mathrm {B}$的用量
为$4.0\mathrm {g},$则可得反应生成$5.0\mathrm {gA}_{2}\mathrm {B}$时需要消耗$\mathrm {B}$的质量为$1.0\mathrm {g}。$
利用质量守恒定律,可判断生成$5.0\mathrm {gA}_{2}\mathrm {B}$时消耗$\mathrm {B}$的质量为
$1.0\mathrm {g},$则消耗$\mathrm {A}$的质量$=5.0\mathrm {g}-1.0\mathrm {g}=4.0\mathrm {g},$则两物质恰好完全
反应时,$\mathrm {A}、$$\mathrm {B}$两物质的用量比为4∶1
根据反应中反应物$\mathrm {A}、$$\mathrm {B}$两物质的质量比为4∶1及质量守恒
定律,由于丙同学实验中生成$\mathrm {A}_{2}\mathrm {B}$的质量$3.0\mathrm {g}$
若$\mathrm {A}$的用量$=3.0\mathrm {g}×45=2.4\mathrm {g},$此时$\mathrm {B}$的用量$=8.0\mathrm {g}-2.4\mathrm {g}=5.6\mathrm {g} $
若$\mathrm {B}$的用量$=3.0\mathrm {g}×15=0.6\mathrm {g},$此时$\mathrm {A}$的用量$=8.0\mathrm {g}-0.6\mathrm {g}=7.4\mathrm {g} $
因此丙学生实验中$\mathrm {a}∶\mathrm {b}$的值为2.4∶5.6=3∶7或7.4∶0.6=37∶3
答:丙学生实验中$\mathrm {a}∶\mathrm {b}$的值可能是3∶7或37∶3.
查看更多完整答案,请扫码查看


