第28页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
4.(2024年·成都)氧气的制取和性质实验如图。下列说法正确的是(
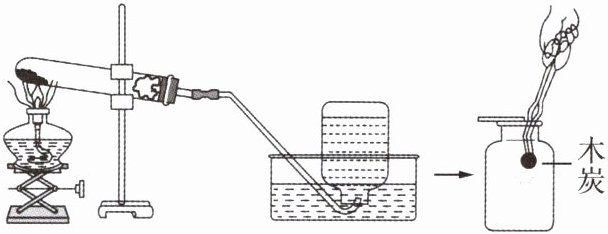
A.发生装置仅由药品状态决定
B.该装置能收集到纯净的氧气
C.红热木炭应迅速伸入集气瓶瓶底
D.制取氧气的原料一定含有氧元素
D
)。
A.发生装置仅由药品状态决定
B.该装置能收集到纯净的氧气
C.红热木炭应迅速伸入集气瓶瓶底
D.制取氧气的原料一定含有氧元素
答案:
D
5.(2024年·河南)氧气性质活泼,能支持燃烧。下列物质在氧气中燃烧,能生成无色、无味气体的是(
A.铁丝
B.硫粉
C.红磷
D.木炭
D
)。A.铁丝
B.硫粉
C.红磷
D.木炭
答案:
D
6.(2024年·重庆改编)正确认识及调控化学反应是化学实验顺利开展的保障。
过氧化氢溶液制氧气
 ①仪器a的名称是
①仪器a的名称是
②利用二氧化锰催化过氧化氢的反应文字表达式为
③为了产生平稳的气流并实时观察气流速率,可选择的发生装置和收集装置是
过氧化氢溶液制氧气
 ①仪器a的名称是
①仪器a的名称是集气瓶
。②利用二氧化锰催化过氧化氢的反应文字表达式为
过氧化氢$\xrightarrow{二氧化锰}$水 + 氧气
。③为了产生平稳的气流并实时观察气流速率,可选择的发生装置和收集装置是
BD
(填字母)。
答案:
①集气瓶
②过氧化氢$\xrightarrow{二氧化锰}$水 + 氧气
③BD
②过氧化氢$\xrightarrow{二氧化锰}$水 + 氧气
③BD
7.(2024年·重庆改编)${O2}$在医疗技术、化工生产等领域都有重要应用。
(1)从元素守恒角度看,下列物质不能用于制取氧气的是(
A.${CH4}$
B.${KMnO4}$
C.${NaCl}$
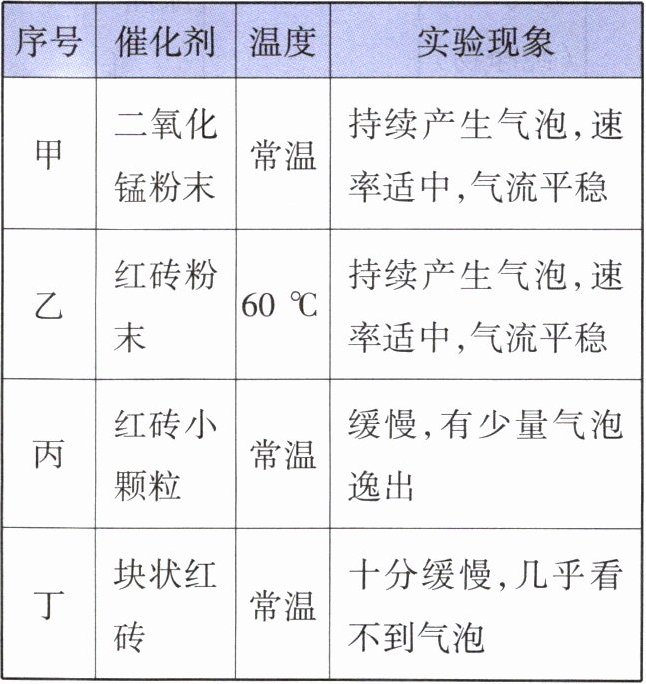
(2)某探究小组进行了“催化剂等因素对过氧化氢分解的影响”的系列探究,该小组分别取1g不同的催化剂,再加入溶质质量分数5%的过氧化氢溶液20mL,进行了如下实验:
|序号|催化剂|温度|实验现象|
|甲|二氧化锰粉末|常温|持续产生气泡,速率适中,气流平稳|
|乙|红砖粉末|$60\ {^{\circ}C}$|持续产生气泡,速率适中,气流平稳|
|丙|红砖小颗粒|常温|缓慢,有少量气泡逸出|
|丁|块状红砖|常温|十分缓慢,几乎看不到气泡|
①写出实验甲中发生反应的文字表达式:
②二氧化锰粉末与红砖粉末对过氧化氢溶液分解具有相同的催化效果,你认为此结论是否科学?
③能说明催化剂的催化效果与其形态有关的实验组合是
④在一定温度下,另取2g红砖小颗粒,向其中加入8%的过氧化氢溶液20mL,继续实验,发现产生气泡的速率明显比实验丙快。请分析可能的原因(至少写两条)
(1)从元素守恒角度看,下列物质不能用于制取氧气的是(
AC
)(填字母)。A.${CH4}$
B.${KMnO4}$
C.${NaCl}$
(2)某探究小组进行了“催化剂等因素对过氧化氢分解的影响”的系列探究,该小组分别取1g不同的催化剂,再加入溶质质量分数5%的过氧化氢溶液20mL,进行了如下实验:
|序号|催化剂|温度|实验现象|
|甲|二氧化锰粉末|常温|持续产生气泡,速率适中,气流平稳|
|乙|红砖粉末|$60\ {^{\circ}C}$|持续产生气泡,速率适中,气流平稳|
|丙|红砖小颗粒|常温|缓慢,有少量气泡逸出|
|丁|块状红砖|常温|十分缓慢,几乎看不到气泡|

①写出实验甲中发生反应的文字表达式:
过氧化氢$\xrightarrow{二氧化锰}$水+氧气
。②二氧化锰粉末与红砖粉末对过氧化氢溶液分解具有相同的催化效果,你认为此结论是否科学?
否
(填“是”或“否”)。理由是实验甲和乙的温度不同,没有控制单一变量
。③能说明催化剂的催化效果与其形态有关的实验组合是
丙、丁
(填实验序号)。④在一定温度下,另取2g红砖小颗粒,向其中加入8%的过氧化氢溶液20mL,继续实验,发现产生气泡的速率明显比实验丙快。请分析可能的原因(至少写两条)
过氧化氢溶液的溶质质量分数增大;催化剂的质量增加
。
答案:
(1)AC;
(2)①过氧化氢$\xrightarrow{二氧化锰}$水+氧气;②否;实验甲和乙的温度不同,没有控制单一变量;③丙、丁;④过氧化氢溶液的溶质质量分数增大;催化剂的质量增加
(1)AC;
(2)①过氧化氢$\xrightarrow{二氧化锰}$水+氧气;②否;实验甲和乙的温度不同,没有控制单一变量;③丙、丁;④过氧化氢溶液的溶质质量分数增大;催化剂的质量增加
查看更多完整答案,请扫码查看


