第57页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
1. 下列各组金属中,按金属活动性由强到弱顺序排列的是(
A.Na、Fe、Mg
B.K、Cu、Fe
C.Ca、Ag、Zn
D.Al、Zn、Hg
D
)。A.Na、Fe、Mg
B.K、Cu、Fe
C.Ca、Ag、Zn
D.Al、Zn、Hg
答案:
D
2. 若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是(
A.$Mn + H_2SO_4= MnSO_4 + H_2↑$
B.$Mg + MnSO_4= MgSO_4 + Mn$
C.$Fe + MnSO_4= FeSO_4 + Mn$
D.$Mn + CuSO_4= MnSO_4 + Cu$
C
)。A.$Mn + H_2SO_4= MnSO_4 + H_2↑$
B.$Mg + MnSO_4= MgSO_4 + Mn$
C.$Fe + MnSO_4= FeSO_4 + Mn$
D.$Mn + CuSO_4= MnSO_4 + Cu$
答案:
C
3. 化学实验小组为探究金属的活动性强弱,用右图所示装置进行实验。下列说法不正确的是(
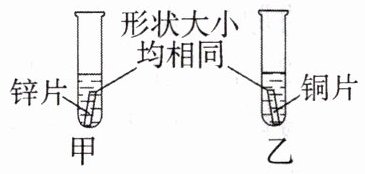
A.实验前需要打磨金属片,除去表面的氧化膜
B.若向甲、乙试管加入稀盐酸,只有锌片表面能产生气泡
C.若向乙试管加入$ ZnSO_4$溶液,能得出锌的金属活动性比铜强
D.若向甲、乙试管加入$ AgNO_3$溶液,能得出三种金属的活动性:Zn>Cu>Ag
D
)。
A.实验前需要打磨金属片,除去表面的氧化膜
B.若向甲、乙试管加入稀盐酸,只有锌片表面能产生气泡
C.若向乙试管加入$ ZnSO_4$溶液,能得出锌的金属活动性比铜强
D.若向甲、乙试管加入$ AgNO_3$溶液,能得出三种金属的活动性:Zn>Cu>Ag
答案:
D
4. 有 X、Y、Z 三种金属,其中 Y 能与稀硫酸反应,而 X、Z 不能与稀硫酸反应。将 Z 浸入$ X(NO_3)_2$的溶液中,在 Z 的表面有 X 析出。则 X、Y、Z 的金属活动性由强到弱的顺序是(
A.X、Y、Z
B.Y、Z、X
C.Y、X、Z
D.Z、X、Y
B
)。A.X、Y、Z
B.Y、Z、X
C.Y、X、Z
D.Z、X、Y
答案:
B
5. 为了探究铁、铜、银的金属活动性顺序,同学们在实验室进行了下图所示的实验。
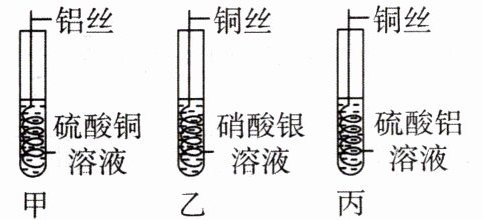
(1)甲实验中看到的实验现象是
(2)甲、乙实验中化学反应的特点是
(3)丙实验无明显现象,原因是
(4)通过上述实验,可以得出的实验结论是

(1)甲实验中看到的实验现象是
铝丝表面有红色固体产生,溶液由蓝色变成无色
,乙实验中发生反应的化学方程式为Cu+2AgNO₃=2Ag+Cu(NO₃)₂
。(2)甲、乙实验中化学反应的特点是
都是一种单质和一种化合物生成另一种单质和另一种化合物
,它们属于置换反应
(填基本反应类型)。(3)丙实验无明显现象,原因是
铜的金属活动性比铝弱
。(4)通过上述实验,可以得出的实验结论是
金属活动性顺序为铝>铜>银
。
答案:
(1)铝丝表面有红色固体产生,溶液由蓝色变成无色 Cu+2AgNO₃=2Ag+Cu(NO₃)₂(2)都是一种单质和一种化合物生成另一种单质和另一种化合物 置换反应(3)铜的金属活动性比铝弱(4)金属活动性顺序为铝>铜>银
6. 化学小组设计图 1 实验来验证铁、铜、银的金属活动性顺序,并在实验后按照图 2 所示流程从试管 B 的溶液中回收铜和银。
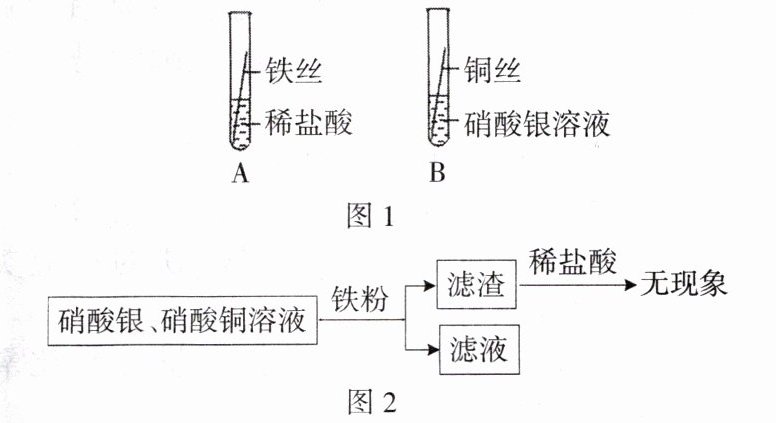
(1)针对图 1 中的方案,只利用所给的四种试剂,再补充一个实验,即可达到实验目的,写出补充实验的步骤、现象及结论。

(2)分析图 2 的处理流程,滤渣里一定含有的物质是______。判断所加铁粉已达成实验目的的方法是______。

(1)针对图 1 中的方案,只利用所给的四种试剂,再补充一个实验,即可达到实验目的,写出补充实验的步骤、现象及结论。

(2)分析图 2 的处理流程,滤渣里一定含有的物质是______。判断所加铁粉已达成实验目的的方法是______。
(1)取少量稀盐酸于试管中插入铜丝 铜丝表面无变化 证明铜的金属活动性小于氢(2)银 取少量滤液于试管中,加入铁粉,无红色固体产生,说明已经达到目的
答案:
(1)取少量稀盐酸于试管中插入铜丝 铜丝表面无变化 证明铜的金属活动性小于氢(2)银 取少量滤液于试管中,加入铁粉,无红色固体产生,说明已经达到目的
7. 同学们为了验证铝和铜的金属活动性顺序,设计了以下实验方案。
【方案一】将铝片和铜片相互刻画,金属片上出现划痕者更活泼。
【方案二】将铝丝和铜丝表面打磨后,同时放入 5 mL 相同的稀盐酸中,金属丝表面产生气泡者更活泼。
【方案三】将铝丝和铜丝表面打磨后,同时放入 5 mL 相同的硝酸银溶液中,金属丝表面有银白色物质析出者更活泼。
以上方案中,你认为能达到实验目的的是方案
【方案一】将铝片和铜片相互刻画,金属片上出现划痕者更活泼。
【方案二】将铝丝和铜丝表面打磨后,同时放入 5 mL 相同的稀盐酸中,金属丝表面产生气泡者更活泼。
【方案三】将铝丝和铜丝表面打磨后,同时放入 5 mL 相同的硝酸银溶液中,金属丝表面有银白色物质析出者更活泼。
以上方案中,你认为能达到实验目的的是方案
方案二
,该方案中发生反应的化学方程式为2Al+6HCl=2AlCl₃+3H₂↑
。
答案:
方案二 2Al+6HCl=2AlCl₃+3H₂↑
查看更多完整答案,请扫码查看


